



版权说明:本文档由用户提供并上传,收益归属内容提供方,若内容存在侵权,请进行举报或认领
文档简介
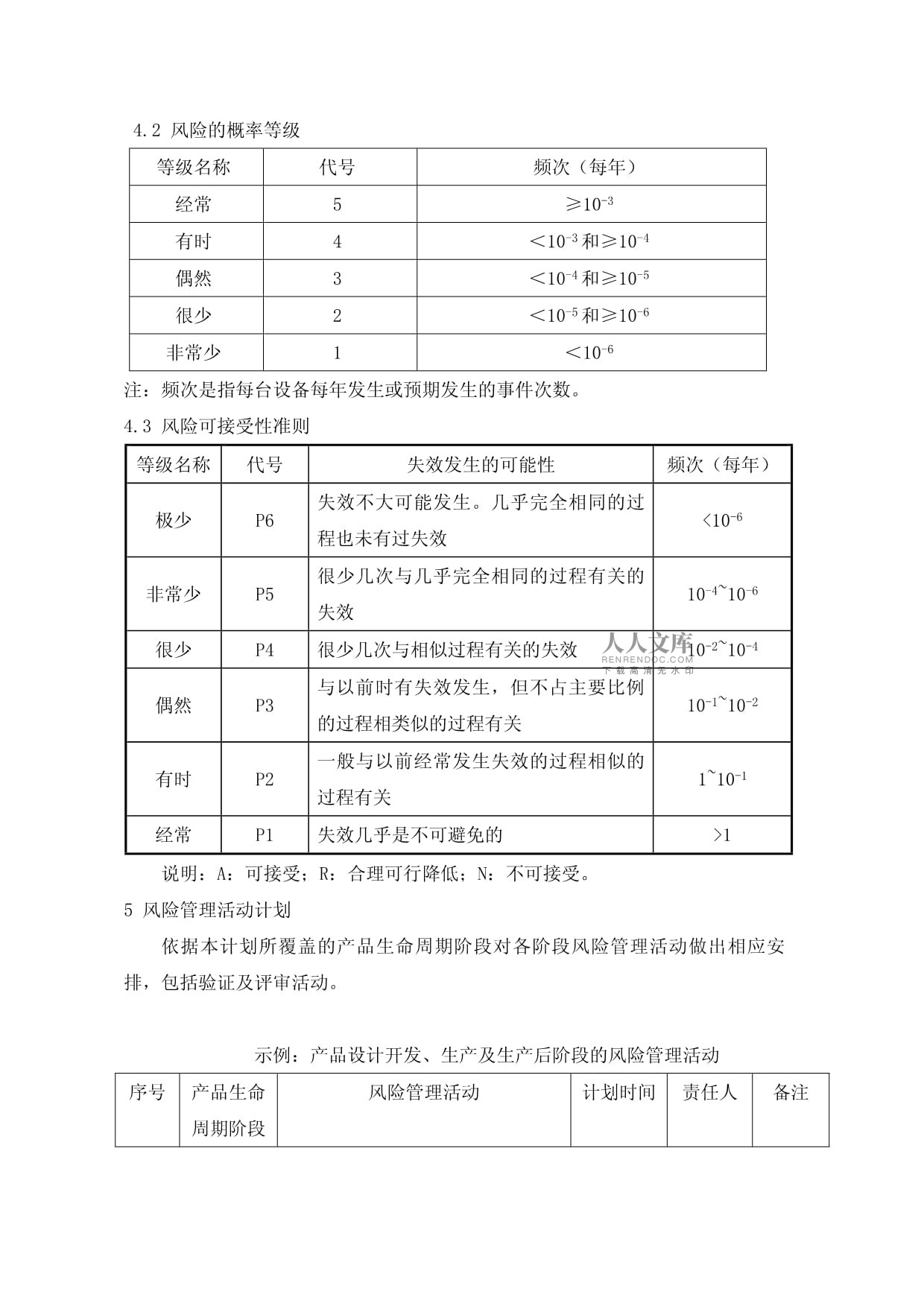
医疗器械风险管理计划1产品简介(对产品工作原理、组成、功能和预期用途的描述。)2范围(简要说明本计划所覆盖的产品生命周期。风险管理的范围包括医疗器械生命周期的所有阶段。医疗器械的生命周期一般包括设计开发策划、设计开发、制造、安装、销售、使用、售后服务和报废处置。)3职责(参加风险管理活动人员的职责,如项目经理、技术、检验、制造、临床和风险管理评审人员等)如:xxx(项目经理、风险管理组长):xxx(机械工程师):xxx(电气工程师):xxx(制造部门负责人):xxx(检验人员):……4风险接受性准则(对特定的产品,可直接采用公司《医疗器械风险管理制度》中规定的可接受性准则,也可对公司规定的可接受性准则的适宜性进行评价,根据公司风险管理活动方针制定适用于特定产品的风险可接受性准则。)示例:风险管理小组对公司《医疗器械风险管理制度》制定的风险可接收性准则进行了评价,认为XXX产品完全适用。4.1风险的严重度水平分级等级名称代号定义灾难性的5导致患者死亡危重的4导致永久性损伤或危及生命的伤害严重3导致要求专业医疗介入的伤害或损伤轻度2导致不要求专业医疗介入的伤害或损伤可忽略1不便或暂时不适4.2风险的概率等级等级名称代号频次(每年)经常5≥10-3有时4<10-3和≥10-4偶然3<10-4和≥10-5很少2<10-5和≥10-6非常少1<10-6注:频次是指每台设备每年发生或预期发生的事件次数。4.3风险可接受性准则等级名称代号失效发生的可能性频次(每年)极少P6失效不大可能发生。几乎完全相同的过程也未有过失效<10-6非常少P5很少几次与几乎完全相同的过程有关的失效10-4~10-6很少P4很少几次与相似过程有关的失效10-2~10-4偶然P3与以前时有失效发生,但不占主要比例的过程相类似的过程有关10-1~10-2有时P2一般与以前经常发生失效的过程相似的过程有关1~10-1经常P1失效几乎是不可避免的>1说明:A:可接受;R:合理可行降低;N:不可接受。5风险管理活动计划依据本计划所覆盖的产品生命周期阶段对各阶段风险管理活动做出相应安排,包括验证及评审活动。示例:产品设计开发、生产及生产后阶段的风险管理活动序号产品生命周期阶段风险管理活动计划时间责任人备注1技术质量部、风险管理小组2技术质量部3技术质量部、风险管理小组4技术质量部5技术质量部、风险管理小组6技术质量部、制造部7技术质量部、风险管理小组8技术质量部、风险管理小组9技术质量部、风
温馨提示
- 1. 本站所有资源如无特殊说明,都需要本地电脑安装OFFICE2007和PDF阅读器。图纸软件为CAD,CAXA,PROE,UG,SolidWorks等.压缩文件请下载最新的WinRAR软件解压。
- 2. 本站的文档不包含任何第三方提供的附件图纸等,如果需要附件,请联系上传者。文件的所有权益归上传用户所有。
- 3. 本站RAR压缩包中若带图纸,网页内容里面会有图纸预览,若没有图纸预览就没有图纸。
- 4. 未经权益所有人同意不得将文件中的内容挪作商业或盈利用途。
- 5. 人人文库网仅提供信息存储空间,仅对用户上传内容的表现方式做保护处理,对用户上传分享的文档内容本身不做任何修改或编辑,并不能对任何下载内容负责。
- 6. 下载文件中如有侵权或不适当内容,请与我们联系,我们立即纠正。
- 7. 本站不保证下载资源的准确性、安全性和完整性, 同时也不承担用户因使用这些下载资源对自己和他人造成任何形式的伤害或损失。
最新文档
- 外墙项目维修合同范本
- 卷板机销售合同范本
- 解除劳务施工合同范本
- 江门预售房合同范本
- 项目类预算培训
- 少数民族教育调研
- 2024年单招考试职业适应性测试题库(物理)
- 预制厂安全教育培训
- 物业客户服务意识
- 辽阳职业技术学院《智能交通系统》2023-2024学年第二学期期末试卷
- 2025年甘肃甘南州国控资产投资管理集团有限公司面向社会招聘工作人员12人笔试参考题库附带答案详解
- 2025年安徽省滁州市凤阳县部分事业单位招聘历年自考难、易点模拟试卷(共500题附带答案详解)
- 2025年辽宁省交通高等专科学校单招职业适应性测试题库必考题
- 2024年临港新片区文员招聘笔试真题
- 2024年食品微生物检验技术试题库及答案(含各题型)
- 2025广东深圳证券信息有限公司人员招聘笔试参考题库附带答案详解
- 合金污水管施工方案
- 统编历史七年级下册(2024版)第8课-北宋的政治【课件】j
- 2025年安徽国防科技职业学院单招职业技能考试题库必考题
- 高等数学(慕课版)教案 教学设计-1.3 极限的运算法则;1.4 极限存在准则与两个重要极限
- 5.1《水经注》序教案-【中职专用】高二语文同步教学(高教版2023·拓展模块下册)

评论
0/150
提交评论