



版权说明:本文档由用户提供并上传,收益归属内容提供方,若内容存在侵权,请进行举报或认领
文档简介
1、课时 2 原电池化学电源课时跟踪训练一、选择题1. (2017 洛阳期末)下列有关电池的说法不正确的是()A. 太阳能电池的主要材料是高纯度的二氧化硅B. 铜锌原电池工作时,电子沿外电路从锌电极流向铜电极C. 氢氧燃料电池工作时,氢气在负极被氧化D. 原电池中一定发生了氧化还原反应解析 太阳能电池的主要材料是高纯度的晶体硅,A 项错误;铜锌原电池工作时,电子沿外电路由负极(锌)流向正极(铜),B 项正确;氢氧燃料电池工作时,氢气在负极失去电子被氧 化,C项正确;由原电池的工作原理可知原电池中一定发生了氧化还原反应,D 项正确。答案 A2.下列示意图中能构成原电池的是()导线解析 Cu、C 与稀
2、硫酸不反应,A 装置不能构成原电池; Al 与氢氧化钠溶液发生氧化还原反 应,B 装置能构成原电池;C 装置中的“导线”不是盐桥,不能构成原电池;D 装置中缺少盐桥。答案 B3下列事实不能用原电池原理解释的是()A. 将镁粉、铁粉和食盐一块加到水中迅速反应放热B. 铁被钝化处理后不易腐蚀C.纯锌与稀硫酸反应时,滴入少量CuSQ 溶液后反应速率加快D. 镀层破损后,镀锌铁比镀锡铁更耐用解析 将镁粉、铁粉和食盐一块加到水中,构成原电池装置,金属镁是负极,镁和水的反应 是放热反应,形成原电池可以加快化学反应速率,能用原电池原理解释,A 不符合题意;铁被钝化后,在金属表面会形成一层致密的金属氧化膜,保
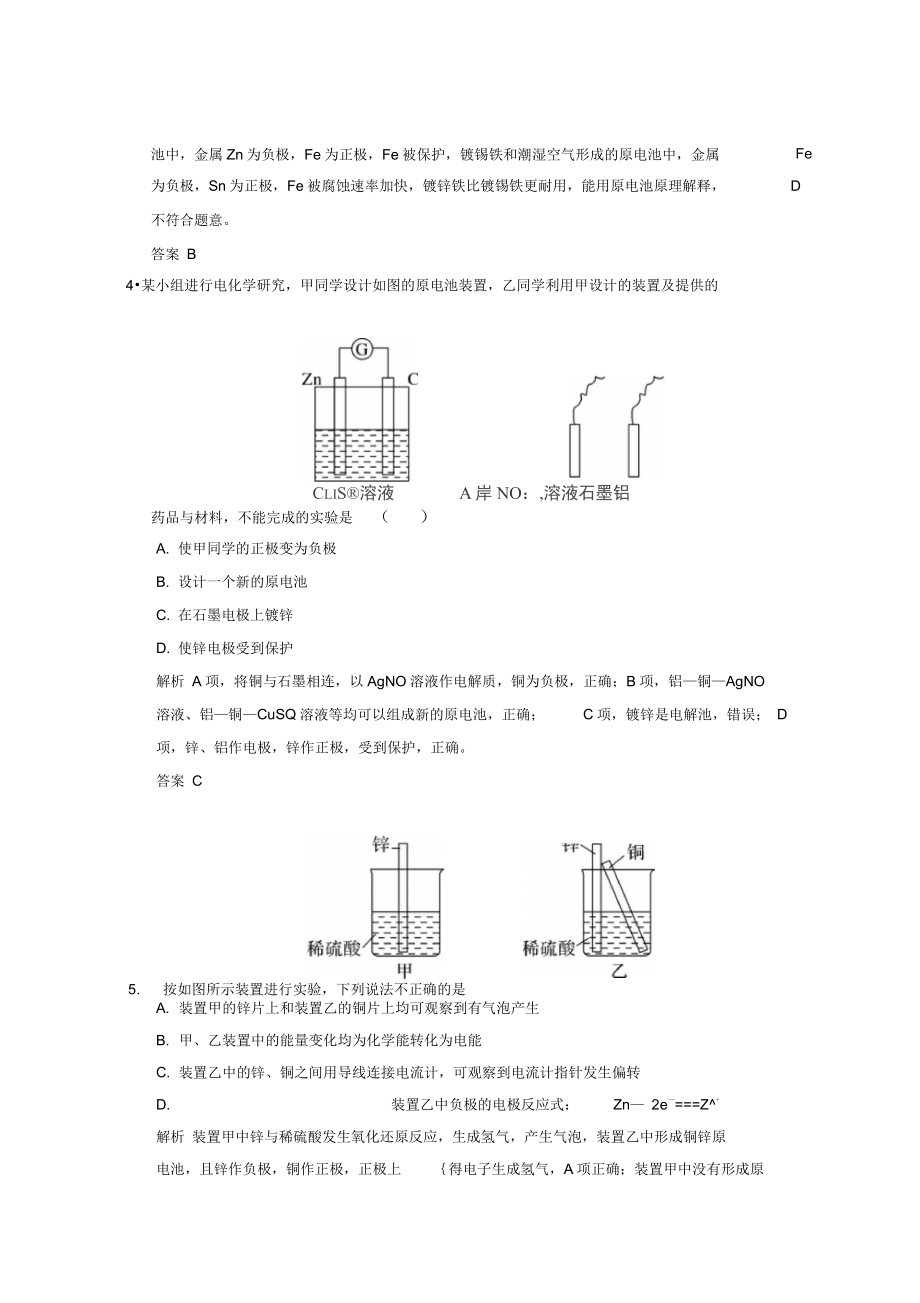
3、护内部金属不易被腐蚀,不能用原电池原理解释,B 符合题意;纯锌与稀硫酸反应时,滴入少量 CuSQ 溶液后,金属锌可以和硫 酸铜反应置换出铜,Zn、Cu 硫酸会构成原电池装置, Zn 为负极,使得 Zn 和硫酸的反应速 率加快,能用原电池原理解释, C 不符合题意;镀层破损后,镀锌铁和潮湿空气形成的原电池中,金属 Zn 为负极,Fe 为正极,Fe 被保护,镀锡铁和潮湿空气形成的原电池中,金属为负极,Sn 为正极,Fe 被腐蚀速率加快,镀锌铁比镀锡铁更耐用,能用原电池原理解释,D不符合题意。答案 B4某小组进行电化学研究,甲同学设计如图的原电池装置,乙同学利用甲设计的装置及提供的药品与材料,不能完
4、成的实验是()A. 使甲同学的正极变为负极B. 设计一个新的原电池C. 在石墨电极上镀锌D. 使锌电极受到保护解析 A 项,将铜与石墨相连,以 AgNO 溶液作电解质,铜为负极,正确;B 项,铝铜AgNO溶液、铝铜CuSQ 溶液等均可以组成新的原电池,正确;C 项,镀锌是电解池,错误; D项,锌、铝作电极,锌作正极,受到保护,正确。答案 C5.按如图所示装置进行实验,下列说法不正确的是A. 装置甲的锌片上和装置乙的铜片上均可观察到有气泡产生B. 甲、乙装置中的能量变化均为化学能转化为电能C. 装置乙中的锌、铜之间用导线连接电流计,可观察到电流计指针发生偏转D.装置乙中负极的电极反应式:Zn 2
5、e=Z+解析 装置甲中锌与稀硫酸发生氧化还原反应,生成氢气,产生气泡,装置乙中形成铜锌原电池,且锌作负极,铜作正极,正极上得电子生成氢气,A 项正确;装置甲中没有形成原FeCLIS溶液A岸 NO:,溶液石墨铝电池,不存在化学能与电能的转化,B 项错误;装置乙形成了原电池,锌、铜之间用导线连接电流计,可观察到电流计指针发生偏转,C 项正确;装置乙中负极的电极反应式为Zn 2e2+ _=Zn , D 项正确。答案 B6. (2016 湖北联考)将编号为的四种金属片两两相连浸入稀硫酸中都可组成原电池。相连时,外电路电流从流向,相连时,为正极;相连时,上有气泡逸出,相连时,的质量减少;据此判断这四种金
6、属活动性由大到小的顺序是()A.B.C.D.解析 相连时,外电路电流从流向,说明是正极;比较活泼;相连时,为正极,说明比活泼;相连时,上有气泡逸出,说明是正极,比活泼; 相连时,的质量减少,说明是负极,比活泼,所以金属的活动性顺序为:。答案 B7. (2017 广州模拟)某小组为研究原电池原理,设计如图装置,下列叙述正确的是Fe 比 Cu 活泼,Fe 作负极,电子从 Fe 流向 Cu,故 A、B 两项错误;若 X 为 Fe, Y 为 C,电解质溶液为硫酸铜,则正极C 上析出 Cu,故 C 正确;Zn 比 Cu 活泼,Zn 作负极发生氧化反应,故 D 错误。答案 C&如图是某同学设计的原
7、电池装置,下列叙述中正确的是()电极 I(旳、盐桥1 ir=打1电极 U$ (Cu)A.Fe,B.Fe,C.Fe,D.X 为 Cu,Y 为 Cu,铁为正极Y 为 Cu,电子由铜片流向铁片Y 为 C,碳棒上有红色固体析出Y 为 Zn,锌片发生还原反应解析FeCI.CuCI5:溶液溶液、- 1 J _-L L -1 |11A. 氧化剂和还原剂必须直接接触才能发生反应B. 电极n上发生还原反应,作原电池的正极C.该原电池的总反应式为:2Fe3+ Cu=C 茁+ 2Fe2+D.盐桥中装有含氯化钾的琼脂, K*移向负极区解析 该原电池反应中氧化反应和还原反应在两个不同的烧杯中进行,因此氧化剂和还原剂没有
8、直接接触,A 项错误;B 项,Cu 电极为原电池的负极,发生氧化反应,电极反应式为:Cu 2e_=Cu+,错误;D 项,正极发生反应:2Fe3+ 2e_=2F+,正电荷数减小, K*移向 正极补充正电荷,错误。答案 C9. (2016 大连检测)电化学在日常生活中用途广泛,下图是镁一次氯酸钠燃料电池,电池总反应为:Mg+ ClO+ H2O=C+ Mg(OH) 下列说法不正确的是()A. 惰性电极上发生氧化反应B. 镁电极是该电池的负极C. 正极反应式为 CIO+ H2O+ 2e=CI+ 2OHD. 进料口加入 NaCIO 溶液,出口流出的为 NaCI 溶液解析 由总反应可知镁发生氧化反应,“负
9、氧正还原”,镁为负极,惰性电极上发生还原反应,A 项错误,B 项正确;负极反应为:Mg 2e+ 2OH =Mg(OH)J,正极反应为:CIO+ 2e+ HbO=C+ 2OH, C D 项正确。答案 A10.MCF(型燃料电池可同时供应电和水蒸气,其工作温度为600700C,所用燃料为 耳,电解质为熔融的 KzCQo 已知该电池的总反应为2H2+ C2=2HO,下列有关该电池的说法正确的是( )A. 该电池的正极反应式为 4OH + 4e=Of+ 2H2OB.该电池的负极反应式为H2 2e=2HfC. 放电时 OH 向负极移动D. 当生成 1 moI H2O 时,转移 2 moI 电子解析 该燃
10、料电池的燃料为 H2,电解质为熔融的 K?CO,总反应为 2H +O2=2HO,负极反应式惰性电极(內壁附着催化剂)镁电极进料口为 2Ha + 2CO 4e=2HO+ 2CQ,正极反应式为 Q+ 2CQ+ 4e=2CO,故AB 均错误;电解质中移动的阴离子为 CO,不是 0H,故 C 错误;根据负极反应式知,生成1 mol HO 时转移 2 mol 电子,故 D 正确。答案 D11. (2017 兰州模拟)关于如图微生物燃料电池结构示意图的说法:微生物促进了电子的转移微生物所在电极区放电时发生还原反应放电过程中, J 从正极区移向负极区 正极I_2I.反应式为:MnOI4H + 2e =Mn
11、+ 2H2O 正确的是()质子(H+)交换膜A.C.解析 在微生物作用下 G(H2O)n转化为 CO 促进电子的转移,正确;微生物在右侧,右侧电极为电源的负极,所以微生物所在电极区放电时发生氧化反应,错误;根据电流的方向,放电过程中, H 从负极区移向正极区,错误;电池左侧为电池的正极区,MnO 在条件下发生得电子反应,所以正极反应式为:MnOI4H+ 2e=Mn+ 2fO,正确。答案 C12.钠离子电池具有资源广泛、价格低廉、环境友好、安全可靠的特点,特别适合于固定式大规模储能应用的需求。一种以NaSQ 水溶液为电解液的钠离子电池的总反应为:NaTi2(PO4)3+n、川代表其价态)。下列说
12、法不正确的是()A. 放电时 NaTi2(PO)3在正极发生还原反应B.放电时负极材料中的 Na 脱离电极进入溶液,同时溶液中的Na1嵌入到正极材料中C.该电池在较长时间的使用过程中电解质溶液中Na 的浓度基本保持不变D.充电过程中阳极反应式为:2NaNiFem(CN“+ 2Na + 2e=2NCu,但在稀硝酸中却出现了反常,结合稀硝酸的氧化性,不难推测铬被稀硝酸钝化,导致活性降低。答案2H+ 2e=Hf Al 3e+ 4OH=AlQ+ 2HzQ 铁 Q+ 2HzQ+ 4e=4QH(2)金属铬的活泼性比铜强且能和稀硫酸反应生成H2、金属铬易被稀硝酸钝化14.(2016 深圳模拟)如图所示,是原
13、电池的装置图。请回答:空NoOH溶液NaCIJi夜Crl+(aq)稀硫酸稀硝酸(1)若 C 为稀 HSQ 溶液,电流表指针发生偏转,B电极材料为 Fe 且做负极,则 A 电极上发生的电极反应式为 _ ;反应进行一段时间后溶液 C 的 pH 将_ (填“升高” “降低”或“基本不变”)若需将反应:Cu+ 2Fe3+=CiJ+ 2Fe2+设计成如上图所示的原电池装置,则A(负极)极材料为_ , B(正极)极材料为_ ,溶液 C 为_。若 C 为 CuCl2溶液,Zn 是_ 极,Cu 极发生_反应,电极反应为_。反应过程溶液中 c(Cu2+)_ (填“变大”“变小”或“不 变”)。(4)C0 与 H
14、2反应还可制备 CH3OH CH3OH 可作为燃料使用,用 CH3OH 和 Q 组合形成的质子交换 膜燃料电池的结构示意图如下:电池总反应为 2CH0出3Q=2C0 4fO,贝 U c 电极是_ (填“正极”或“负极”),c电极的反应方程式为_。若线路中转移 2 mol 电子,则上述 CHQH 燃料电池,消耗的 O 在标准状况下的体积为 _ L。解析(1)铁作负极,则该原电池反应是铁与稀硫酸置换氢气的反应,所以正极反应是氢离子得电子生成氢气,电极反应式为2H+ 2e=Hf ;溶液中氢离子放电,导致溶液中氢离子浓度减小,pH 升高;(2) Cu + 2Fe3+=C(j+ 2Fe2+设计成如题图所
15、示的原电池装置,根据方程式中物质发生的反应类型判断,Cu 发生氧化反应,作原电池的负极,所以A 材料是 Cu, B 极材料是比 Cu 不活泼的导电物质如石墨、 Ag 等即可。溶液 C 中含有 Fe3+,如 FeCb 溶液;(3) Zn 比较活泼,在原电池中做负极,Cu 做正极,正极发生还原反应,Cu2+在正极得到电子质子交换B变成 Cu,电极反应为 Cu2+ 2e_=Cu Cu2+发生了反应,则 c(Cu2+)变小;根据图中的电子流向知 c 是负极,是甲醇发生氧化反应:CHOH- 6e+ 0=0,线 路中转移 2 mol电子时消耗氧气 0.5 mol,标况下体积为 11.2 L。答案(1)2H
16、+ 2e=Hf升高(2) Cu 石墨 FeCb 溶液(3) 负极 还原 Cu2+ 2e_=Cu 变小(4)负极 CHOH- 6e+ H2O=C2 6H+11.215.(能力挑战题)(2017 郑州模拟)某实验小组同学对电化学原理进行了一系列探究活动。(1)如图为某实验小组依据的氧化还原反应:(用离子方程式表示)_ 。设计的原电池装置,反应前,电极质量相等,一段时间后,两电极质量相差12 g,导线中通过_mol 电子。其他条件不变,若将 CuCl2溶液换为 NHCI 溶液,石墨电极反应式为_,这是由于 NHCI溶液显_(填“酸性” “碱性”或“中性”),用离子方程式表示溶液显此性的原因,用吸管吸
17、出铁片附近溶液少许置于试管中,向其中滴加少量新制饱和氯水,写出发生反应的离子方程式, 然后滴加几滴硫氰化钾溶液,溶液变红,继续 滴加过量新制饱和氯水,颜色褪去,同学们对此做了多种假设,某同学的假设是:“溶液中 的+ 3 价铁被氧化为更高的价态。”如果+3价铁被氧化为 FeC,试写出该反应的离子方程式_。(3)如图其他条件不变,若将盐桥换成弯铜导线与石墨相连成n 型,如图所示,一段时间后,在甲装置铜丝附近滴加酚酞试液,现象是_,电极反应为_;乙装置中石墨(1)为_极(填“正”“负”“阴”或“阳”),乙装置中与铜丝相连石墨(2)电极上发生的反应式为 _ ,产物常用 _检验,反应的离子方程式为解析(
18、1)若一段时间后,两电极质量相差 12 g,消耗负极 0.1 mol Fe,同时正极生成 0.1 mol Cu,导线中通过 0.2 mol 电子。(2)其他条件不变,若将 CuCl2溶液换为 NHCI 溶液,由于 NhT水解,N 宵+ HQW3H2CWH,所以 NHCI 溶液显酸性,石墨电极上H 得到电子,电极反应式为 2H+ 2e-=Hf;铁电极反应式为 Fe 2e-=F+,用吸管吸出铁片附近溶液少许置 于试管中,向其中滴加少量新制饱和氯水,发生反应的离子方程式为2Fe2+ Cl2=2F(e+ 2CI,然后滴加几滴硫氰化钾溶液,由于存在 Fe3*,所以溶液变红,继续滴加过量新制饱和氯水,颜色褪去,如果原因是+3 价铁被氧化为 FeCf,则该反应的离子方程式为2Fe3+ 3Cl2+8H2O=2FeC+ 6CI+ 16H+O(3)如图其他条件不变,若将盐桥换成弯铜导线与石墨相连成n型,则甲池为原电池,铁电极反应为Fe 2=F,铜电极反应为 Q+ 2HzO+ 4e =4OH;乙池为电解池,石墨(2)电极为阳极,电极反应为2Cl
温馨提示
- 1. 本站所有资源如无特殊说明,都需要本地电脑安装OFFICE2007和PDF阅读器。图纸软件为CAD,CAXA,PROE,UG,SolidWorks等.压缩文件请下载最新的WinRAR软件解压。
- 2. 本站的文档不包含任何第三方提供的附件图纸等,如果需要附件,请联系上传者。文件的所有权益归上传用户所有。
- 3. 本站RAR压缩包中若带图纸,网页内容里面会有图纸预览,若没有图纸预览就没有图纸。
- 4. 未经权益所有人同意不得将文件中的内容挪作商业或盈利用途。
- 5. 人人文库网仅提供信息存储空间,仅对用户上传内容的表现方式做保护处理,对用户上传分享的文档内容本身不做任何修改或编辑,并不能对任何下载内容负责。
- 6. 下载文件中如有侵权或不适当内容,请与我们联系,我们立即纠正。
- 7. 本站不保证下载资源的准确性、安全性和完整性, 同时也不承担用户因使用这些下载资源对自己和他人造成任何形式的伤害或损失。
最新文档
- 2025会议场地租赁合同(合同范本)
- 《2025光伏电站用工试用期合同》
- 品牌危机公关处理指南
- 小学生防拐防骗课件
- 在线医疗平台医生资源整合及服务模式创新方案
- 低血糖的识别与护理
- 服务型企业营销与品牌建设指南
- 花木市场委托协议
- 航空行业智能航空物流与运营管理方案
- 电信行业网络优化与客户服务升级策略方案
- 《医养结合事业发展探究的国内外文献综述》4400字
- 水电施工机械新能源化的可行性分析与应用研究
- 关于中山市中医四诊智能化与传统中医诊断之间的协同效应调查问卷
- 【MOOC】压力与情绪管理-四川大学 中国大学慕课MOOC答案
- 我的家乡西藏山南
- 零星维修工程 投标方案(技术方案)
- 项目管理培训之进度管理课件
- 110kV@@变电站工程高大模板工程专项施工方案
- 先兆流产课件-课件
- 2022年北京市公务员录用考试《行测》真题及答案解析
- DB11T 1028-2021 民用建筑节能门窗工程技术标准

评论
0/150
提交评论