



版权说明:本文档由用户提供并上传,收益归属内容提供方,若内容存在侵权,请进行举报或认领
文档简介
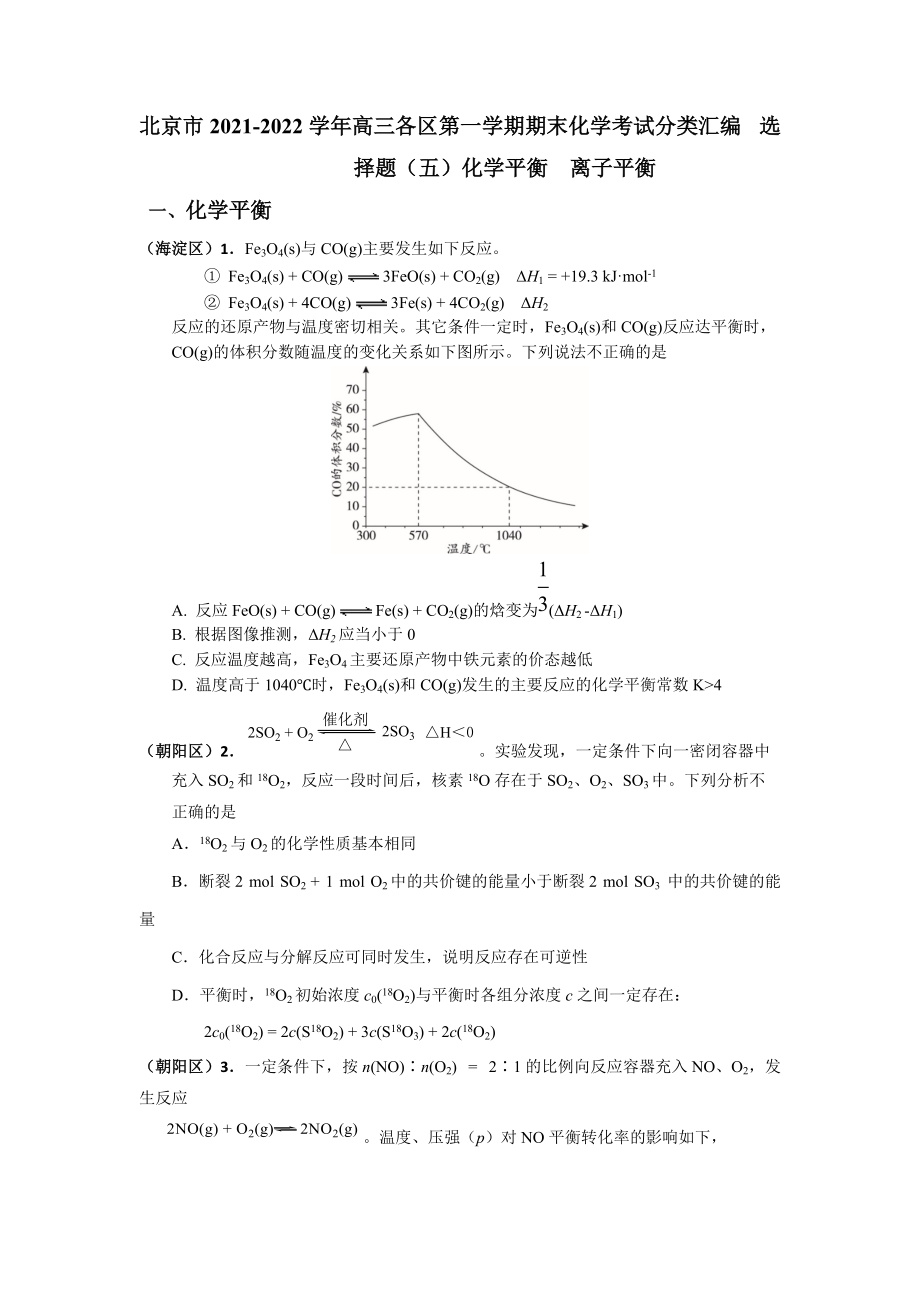
1、北京市2021-2022学年高三各区第一学期期末化学考试分类汇编 选择题(五)化学平衡 离子平衡 一、化学平衡 (海淀区)1Fe3O4(s)与CO(g)主要发生如下反应。 Fe3O4(s) + CO(g) 3FeO(s) + CO2(g) H1 = +19.3 kJ·mol-1 Fe3O4(s) + 4CO(g) 3Fe(s) + 4CO2(g) H2 反应的还原产物与温度密切相关。其它条件一定时,Fe3O4(s)和CO(g)反应达平衡时,CO(g)的体积分数随温度的变化关系如下图所示。下列说法不正确的是A. 反应FeO(s) + CO(g) Fe(s) + CO2(g)的焓变为13
2、(H2 -H1)B. 根据图像推测,H2应当小于0C. 反应温度越高,Fe3O4主要还原产物中铁元素的价态越低D. 温度高于1040时,Fe3O4(s)和CO(g)发生的主要反应的化学平衡常数K>4(朝阳区)2。实验发现,一定条件下向一密闭容器中充入SO2和18O2,反应一段时间后,核素18O存在于SO2、O2、SO3中。下列分析不正确的是A18O2与O2的化学性质基本相同 B断裂2 mol SO2 + 1 mol O2中的共价键的能量小于断裂2 mol SO3 中的共价键的能量 C化合反应与分解反应可同时发生,说明反应存在可逆性 D平衡时,18O2初始浓度c0(18O2)与平衡时各组分
3、浓度c之间一定存在: 2c0(18O2) = 2c(S18O2) + 3c(S18O3) + 2c(18O2) (朝阳区)3一定条件下,按n(NO)n(O2) = 21的比例向反应容器充入NO、O2,发生反应。温度、压强(p)对NO平衡转化率的影响如下,下列分析正确的是A压强大小关系:p1p2 B其他条件相同时,随温度升高该反应的平衡常数增大C400、p1条件下,O2的平衡转化率为40% D500、p1条件下,该反应的化学平衡常数一定为564 (东城区)4ICl与H2能发生反应:H2g+2IClg=I2g+2HClg H<0。已知:该反应由两个基元反应分步完成,第一步为H2g+IClg=
4、HIg+HClg H1两步反应的活化能分别为Ea1、Ea2,且Ea1>Ea2下列判断不正确的是A. 第一步为氧化还原反应B. 第一步的化学反应速率大于第二步的化学反应速率C. 已知键能:H-H>I-I,可推知键能:H-Cl>I-ClD. 第二步的热化学方程式为HIg+IClg=HClg+I2g H2=H-H1(东城区)5气态醋酸中存在平衡CH3COOH2g2CH3COOHg H。实验测得压强分别为p1 和p2时,上述平衡体系中气体的平均摩尔质量(M)随温度(T)的变化如下图所示。已知:M=混合气体的总质量混合气体的总物质的量;MCH3COOH=60gmol-1下列说法不正确的
5、是A. p1>p2B. H<0C. a点时,nCH3COOH2:nCH3COOH=1:2D. 为使M的值接近60,可采取高温、低压的实验条件(西城区)6中国科学家在淀粉人工光合成方面取得重大突破性进展,该实验方法首先将CO2催化还原为CH3OH。已知CO2催化加氢的主要反应有:CO2(g)+3H2(g) CH3OH(g)+H2O(g) H1=-49.4kJ/molCO2(g)+H2(g) CO(g)+H2O(g) H2=+41.2kJ/mol其他条件不变时,在相同时间内温度对CO2催化加氢的影响如图。下列说法不正确的是A. CO(g)+2H2(g) CH3OH(g) H=-90.6
6、kJ/molB. 使用催化剂,能降低反应的活化能,增大活化分子百分数C. 其他条件不变,增大压强,有利于反应向生成CH3OH的方向进行D. 220240°C,升高温度,对反应速率的影响比对反应的小(丰台区)7臭氧分解2O3 3O2的反应历程包括以下反应:反应:O3 O2 + O (快) 反应:O3 + O 2O2 (慢) 大气中的氯氟烃光解产生的氯自由基(Cl)能够催化O3分解,加速臭氧层的破坏。下列说法正确的是A活化能:反应 >反应BO3分解为O2的速率主要由反应决定CCl 主要参与反应,改变O3分解的反应历程DCl 参与反应提高了O3分解为O2的平衡转化率(丰台区)8某温度
7、下,在密闭容器中进行反应:H2(g) + CO2(g) H2O(g) + CO(g) H >0,已知H2(g)和CO2(g)的初始浓度均为0.01 mol·L-1,测得H2的平衡转化率为60%,下列说法不正确的是ACO2的平衡转化率为60% B升高温度平衡常数K增大 C该温度下反应的平衡常数K = 2.25 D若初始H2(g)、CO2(g)、H2O(g)、CO(g)浓度均为0.01 mol·L-1,则反应逆向进行(石景山区)9在容积不变的密闭容器中发生反应:CO(g) + H2O(g) CO2(g) + H2(g) H < 0,830时反应的平衡常数是1.0,下
8、列说法正确的是A容器内的压强不变时,说明反应达到平衡状态B若平衡时移走CO2,则平衡向正反应方向移动,化学反应速率加快C830时,充入0.1 mol CO和0.3 mol H2O保持温度不变,CO平衡转化率为75%D1000时,某时刻CO2、H2、CO和H2O的浓度均为0.05 mol/L,此时平衡向正反应方向移动(昌平区)10在恒压、NO和O2的起始浓度一定的条件下,催化反应相同时间,测得不同温度下NO转化为NO2的转化率如图中实线所示(图中虚线表示相同条件下NO的平衡转化率随温度的变化)。下列说法正确的是A. 当T<200时,反应2NO(g)+O2(g)=2NO2(g)的H>0
9、B. 图中X点所示条件下,延长反应时间能提高NO转化率C. 由图示信息可以推测:该反应在400时反应速率小于500时D. 400时(Y点),若c始(NO)=c起始(O2)=5.0×10-4mol·L-1,NO平衡转化率约为40%,则平衡常数K=5000二、离子平衡(海淀区)1测定0.1 mol·L-1 Na2CO3溶液升温过程中的pH(不考虑水的蒸发),数据如下。温度/20406080pH11.8011.6811.5411.42下列说法正确的是 A温度升高,Na2CO3溶液中c(OH-)降低 B温度升高时溶液pH降低,原因是CO32-水解生成少量H2CO3 CNa
10、2CO3溶液pH的变化是Kw改变与水解平衡移动共同作用的结果 D溶液中c(CO32-)+ c(HCO3-)始终等于0.1 mol·L-1(海淀区)2 小组同学探究盐溶液对反应Fe 3+ SCN- Fe(SCN) 2+(血红色)的影响。将2 mL 0.01 mol·L-1的FeCl3溶液与2 mL 0.02 mol·L-1的KSCN溶液混合,分别加入等量的试剂,测得平衡后体系的透光率如下图所示。已知:i.溶液血红色越深,透光率越小,其它颜色对透光率的影响可忽略 ii.Fe3+4Cl-FeCl4-(黄色)下列说法不正确的是A. 注入试剂后溶液透光率增大,证明Fe 3+
11、 SCN- Fe(SCN) 2+逆向移动B. 透光率比高,可能是阳离子种类或溶液pH导致的C. 透光率比高,可能发生了反应Fe(SCN)2+ + 4Cl- FeCl4 -+ SCN-D. 若要证明试剂中Cl-对平衡体系有影响,还应使用0.04 mol·L-1的KNO3溶液进行实验(朝阳区)3 对浓度均为0.1 mol·L1 CH3COOH溶液、CH3COONa溶液,下列判断不正确的是 A向中滴加石蕊溶液,溶液变红,说明CH3COOH是弱电解质B向中滴加石蕊溶液,溶液变蓝,说明CH3COOH是弱电解质C向中滴加Na2CO3溶液,产生气泡,说明Ka(CH3COOH)Ka1(H2
12、CO3) D、中的c(CH3COOH) 与c(CH3COO) 之和相等(朝阳区)4下列变化中,不能用盐类水解原理解释的是 A用KI溶液将AgCl转化为AgI B用热饱和Na2CO3溶液清洗试管壁上附着的植物油 C向Al2(SO4)3溶液中加入浓NaHCO3溶液,产生沉淀和气体 D向沸水中滴加FeCl3溶液制备Fe(OH)3胶体 (东城区)5电离常数是研究电解质在水溶液中的行为的重要工具。现有HX、H2Y和H2Z三种酸,各酸及其盐之间不发生氧化还原反应,它们的电离常数如下表所示。酸电离常数(25)HXKa=10-9.2H2YKa1=10-6.4 Ka2=10-10.3H2ZKa1=10-1.9
13、Ka2=10-7.2下列说法正确的是A. 在水溶液中结合H+的能力:Y2-<Z2-B. 0.1molL-1NaX溶液中离子浓度的关系:cNa+<cX-C. Na2Y溶液与过量HX反应的离子方程式:HX+Y2-=HY-+X-D. 25时,浓度均为0.1molL-1的H2Y和H2Z溶液的pH:H2Y<H2Z(东城区)625时,用图1装置进行实验:向蒸馏水中加入MgOH2粉末,一段时间后再加入稀硫酸。测得pH随时间变化的曲线如图2所示。下列对曲线的分析不正确的是A. bc段存在平衡MgOH2smg2+aq+2OH-aqB. cd段QMgOH2<KspMgOH2C. a点时加入
14、的nMgOH2大于c点时加入的nH2SO4D. e点时再加入足量MgOH2粉末,可使溶液的pH与b点的相同(西城区)7关于下列实验的说法不正确的是ACH3COO-的水解程度增大B溶液的pH减小是CH3COO-水解平衡移动的结果CNH4Cl可促进CH3COO-的水解D混合液中c(CH3COO-)和c(CH3COOH)之和大于c(Na+)(丰台区)8常温下浓度均为0.1 mol·L-1的两种溶液: CH3COOH溶液 CH3COONa溶液,下列说法不正确的是A水电离产生的c(OH): < BCH3COONa溶液pH > 7说明CH3COOH为弱酸C两种溶液中均存在:c(CH3
15、COO) + c(CH3COOH) = 0.1 mol·L-1D等体积混合所得酸性溶液中:c(Na+) > c(CH3COO) > c(H+) > c(OH) (石景山区)9在常温下,有关下列4种溶液的叙述中不正确的是编号溶液氨水氢氧化钠溶液醋酸盐酸pH111133A在溶液和中分别加入适量的氯化铵晶体后,两种溶液的pH均减小B分别取1 mL稀释至10 mL,4种溶液的pH:>>>C将溶液和等体积混合,所得溶液中:c(CH3COO)>c(Na+)>c(OH)>c(H+)D将a L溶液和b L溶液混合后,若所得溶液的pH = 4,则a
16、 : b = 9 : 11(门头沟区)10下列有关说法正确的是A水溶液中c(OH) > c(H+),溶液一定显碱性BpH均为3的盐酸和醋酸溶液与足量锌反应,后者产生的氢气多CNH4HSO4溶液呈酸性说明NH3·H2O是弱电解质D室温下,将0.2mol/L的醋酸溶液与0.1mol/L的NaOH溶液等体积混合,所得溶液pH<7,则:c(Na+) > c(CH3COO)(顺义区)11. 某化学小组通过测定溶液pH,计算K2Cr2O7溶液中“Cr2O72-(橙色)+H2O2CrO42-(黄色)+2H+”的平衡常数,结果如下:实验序号温度()K2Cr2O7溶液浓度(mol/L
17、)pH平衡常数26.30.1000a2.5×10-1526.30.30003.78b50.00.10003.751.01×10-14 下列说法不合理的是 A. a大于3.78,b等于2.5×10-15 B. 实验对应平衡常数b计算式为 C.由实验结果可说明该反应为吸热反应 D. 向实验的2mL溶液中加入6滴6 mol/L NaOH溶液,溶液橙色加深;恢复原温度,平衡常数不变(顺义区)12. 借助pH传感器测得0.1mol/LNaHCO3溶液在先升温、后降温过程中pH变化如下图所示: 图1. 升温过程中溶液pH变化 图2. 降温过程中溶液pH变化 下列有关实验数据的
18、分析中,不合理的是 A. 图1中25时,溶液中存在关系:c(HCO3-)> c(H2CO3) > c(CO32-) B. 图1中2545过程,溶液pH逐渐减小,说明HCO3及水的电离平衡正移对pH影响大于HCO3水解平衡正移对pH的影响 C. 图1中4560过程,溶液pH逐渐增大,可能是NaHCO3分解,c(CO32-)逐渐增大导致的结果 D. 图2中降温过程,溶液pH逐渐增大,可能是HCO3或CO32-水解平衡正移所致(昌平区)13. 某温度下,将pH和体积均相同的HCl和CH3COOH溶液分别加水稀释,其pH随加水体积的变化如图所示。下列叙述正确的是A. 稀释前溶液的浓度:c(HCl) c(CH3COOH)B. 溶液中水的电离程度:b点c点C. 从b点到d点,溶液中c(H+)c(OH)逐渐增大D. 在d点和e点均存在:c(H+)c(酸根阴离子)(房山区)14时,在
温馨提示
- 1. 本站所有资源如无特殊说明,都需要本地电脑安装OFFICE2007和PDF阅读器。图纸软件为CAD,CAXA,PROE,UG,SolidWorks等.压缩文件请下载最新的WinRAR软件解压。
- 2. 本站的文档不包含任何第三方提供的附件图纸等,如果需要附件,请联系上传者。文件的所有权益归上传用户所有。
- 3. 本站RAR压缩包中若带图纸,网页内容里面会有图纸预览,若没有图纸预览就没有图纸。
- 4. 未经权益所有人同意不得将文件中的内容挪作商业或盈利用途。
- 5. 人人文库网仅提供信息存储空间,仅对用户上传内容的表现方式做保护处理,对用户上传分享的文档内容本身不做任何修改或编辑,并不能对任何下载内容负责。
- 6. 下载文件中如有侵权或不适当内容,请与我们联系,我们立即纠正。
- 7. 本站不保证下载资源的准确性、安全性和完整性, 同时也不承担用户因使用这些下载资源对自己和他人造成任何形式的伤害或损失。
最新文档
- 《艾青诗选》《水浒传》《儒林外史》《简·爱》课件【知识精研】中考语文名著阅读专项复习
- 2024年专升本思政理论的前景试题及答案
- 吉林省前郭尔罗斯蒙古族自治县八年级生物下册 7.2.2基因在亲子代间的传递教学实录 (新版)新人教版
- 八年级英语上册 Unit 5 My Future Lesson 26 What Will I Be教学实录 (新版)冀教版
- 2024年图书管理员考试实务考量试题及答案
- Unit 3 My Hometown-Welcome to the unit教学设计 2024-2025学年译林版(2024)七年级英语下册
- 汽车维修工高级工(三级)理论复习试题含答案
- 如何评估马工学管理效果试题及答案
- 外贸酒水知识培训课件
- 双眼皮手术知识培训课件
- 2025年郑州铁路职业技术学院单招职业技能测试题库必考题
- 家具全屋定制的成本核算示例-成本实操
- 合伙经营煤炭合同范本
- 2025年安庆医药高等专科学校单招职业适应性考试题库及答案1套
- “艾梅乙”感染者消除医疗歧视制度-
- 煤矿单轨吊机车检修工技能理论考试题库150题(含答案)
- 阳光房施工合同范本
- 医院院长聘用合同范本
- 2025年高考物理一轮复习:热学(解析版)
- 2024年洛阳市孟津区引进研究生学历人才考试真题
- 旋挖机施工方案

评论
0/150
提交评论