



版权说明:本文档由用户提供并上传,收益归属内容提供方,若内容存在侵权,请进行举报或认领
文档简介
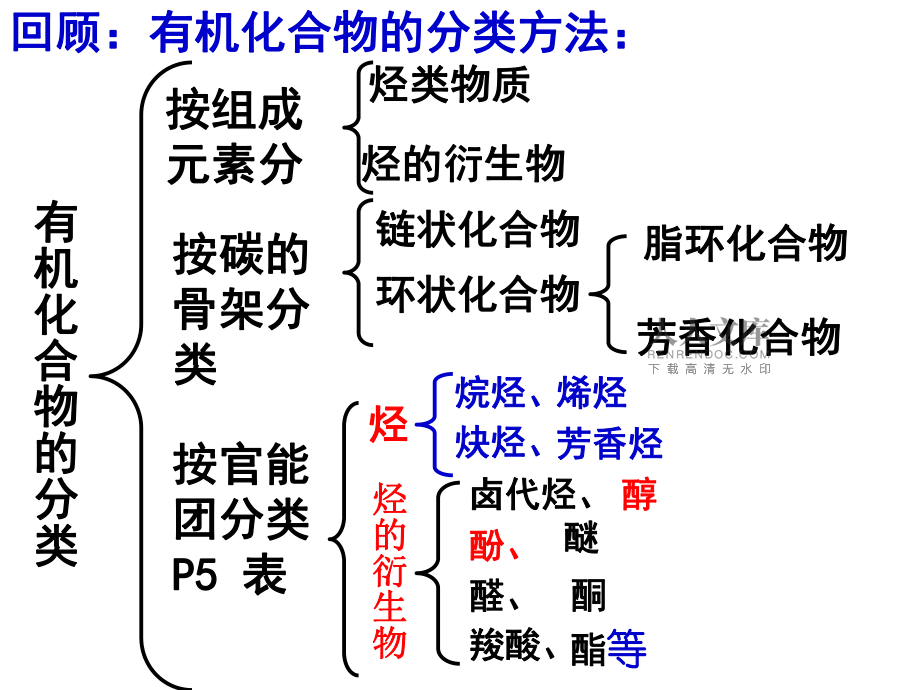
1、第二节 有机化合物的结构特点回顾:有机化合物的分类方法:回顾:有机化合物的分类方法:有机化合物的分类有机化合物的分类按碳的按碳的骨架分骨架分类类链状化合物链状化合物环状化合物环状化合物脂环化合物脂环化合物芳香化合物芳香化合物按官能按官能团分类团分类P5 P5 表表烃烃烷烃、烷烃、烯烃烯烃炔烃、炔烃、芳香烃芳香烃烃的衍生物烃的衍生物卤代烃、卤代烃、 醇醇酚、酚、醚醚醛、醛、酮酮羧酸、羧酸、酯酯等等按组成按组成元素分元素分烃类物质烃类物质烃的衍生物烃的衍生物有机化合物的特点之一就是:有机化合物的特点之一就是:由碳元素所形由碳元素所形成的化合物种类非成的化合物种类非常多!常多!种类繁多种类繁多(30
2、00万多种!万多种!)?一、有机化合物中一、有机化合物中碳原子的成键特点碳原子的成键特点有机物的主要有机物的主要元素是碳元素元素是碳元素1、碳原子的结构特点、碳原子的结构特点碳原子最外层有碳原子最外层有4个电子,不易失去或个电子,不易失去或获得电子而形成阳离子或阴离子。获得电子而形成阳离子或阴离子。碳原子通碳原子通过过共价键(共用电子对)与共价键(共用电子对)与其他原子其他原子(H、O、N、P、S、Cl等等)形形成共价化合物。成共价化合物。例如:甲烷分子(例如:甲烷分子(CH4)请写出甲烷的电子式、结构式、结构简式请写出甲烷的电子式、结构式、结构简式 回答甲烷的空间构型以及键的夹角回答甲烷的空
3、间构型以及键的夹角复习提问:复习提问:电子式电子式结构式结构式CHCH4 4结构简式结构简式 经过科学实验证明甲烷分子的结构是经过科学实验证明甲烷分子的结构是正四面体正四面体结构,碳结构,碳原子位于正四面体的中心,原子位于正四面体的中心,4 4个氢原子分别位于正四面体的个氢原子分别位于正四面体的4 4个顶点上(键角是个顶点上(键角是1091092828)。)。球棍模型球棍模型比例模型比例模型甲烷分子的表示方法甲烷分子的表示方法 空间构型空间构型杂化轨道理论杂化轨道理论科学视野:科学视野:甲烷分子为什么具有正四面体结构呢?甲烷分子为什么具有正四面体结构呢?甲烷分子的形成:甲烷分子的形成: 当碳原
4、子与当碳原子与4个氢原子形成甲烷分子时,碳原子首先激发,个氢原子形成甲烷分子时,碳原子首先激发,然后一个然后一个2s轨道和轨道和3个个2p轨道会发生混杂,混杂时保持轨道总数轨道会发生混杂,混杂时保持轨道总数不变,却得到不变,却得到4个相同的个相同的sp3杂化轨道,为保持斥力最小,夹角只杂化轨道,为保持斥力最小,夹角只能为能为109 28 ,称为,称为sp3杂化轨道,表示这杂化轨道,表示这4个轨道是由个轨道是由1个个s轨轨道和道和3个个p轨道杂化形成的。如下图所示:轨道杂化形成的。如下图所示: 为了四个杂化轨道在空间尽可能远离,使轨道间的排斥最小,为了四个杂化轨道在空间尽可能远离,使轨道间的排斥
5、最小,4个杂化轨道的伸展方向分别以个杂化轨道的伸展方向分别以大头指向正四面体的四个顶点大头指向正四面体的四个顶点。 四个四个H原子分别以原子分别以4个个s轨道与轨道与C原子上的四个原子上的四个sp3杂杂化轨道沿化轨道沿轨道对称轴轨道对称轴重叠,就形成了四个性质、能量重叠,就形成了四个性质、能量和键角都完全相同的和键角都完全相同的S-SP3键,从而构成一个正四面键,从而构成一个正四面体构型的分子。体构型的分子。 10928思考:乙烯和乙炔中的思考:乙烯和乙炔中的C分别为什么杂化类型?有哪些键?分别为什么杂化类型?有哪些键?四个四个sp3杂化轨道再与杂化轨道再与H原子结合:原子结合: 甲烷分子中四
6、个甲烷分子中四个C-HC-H键是等同的,它们键是等同的,它们的键长均为的键长均为109.3pm109.3pm、键角均为键角均为109028、键键能为能为413.4KJ/mol413.4KJ/mol。共价键参数共价键参数键长:键长:键角:键角:键能:键能:成键两个原子的核心间距。成键两个原子的核心间距。键长越短,化学键越稳定。键长越短,化学键越稳定。两共价键在空间的夹角。两共价键在空间的夹角。决定分子的空间构型。决定分子的空间构型。气态基态原子形成气态基态原子形成1mol化学键所释放化学键所释放的最低能量。的最低能量。键能越大,化学键越稳定。键能越大,化学键越稳定。相对应相对应回忆:回忆:2、碳
7、原子间的结合方式、碳原子间的结合方式碳原子不仅能与碳原子不仅能与H H或其他原子形成或其他原子形成4 4个共价键个共价键, ,碳原子之间也能相互以共价键结合。碳原子之间也能相互以共价键结合。(1)碳原子之间可以形成稳定的单键、双键、叁键碳原子之间可以形成稳定的单键、双键、叁键;(2)多个碳原子可以相互结合成长短不一的碳链,多个碳原子可以相互结合成长短不一的碳链, 碳链也可带有支链碳链也可带有支链;(3)多个碳原子还可以相互结合成环,碳环和碳链多个碳原子还可以相互结合成环,碳环和碳链 还可以相互结合。还可以相互结合。(1)碳原子含有碳原子含有4个价电子,可以跟其它原子形个价电子,可以跟其它原子形
8、成成4个共价键个共价键;(成键数目多成键数目多)(5)有机物分子普遍存在有机物分子普遍存在同分异构同分异构现象。现象。(这是有机物种类繁多的主要原因)(这是有机物种类繁多的主要原因)(2)碳原子之间可以形成稳定的单键、双键、叁键碳原子之间可以形成稳定的单键、双键、叁键; (成键种类多)(成键种类多) (3)多个碳原子可以相互结合成长短不一的碳链,多个碳原子可以相互结合成长短不一的碳链, 碳链也可带有支链碳链也可带有支链;(4)多个碳原子还可以相互结合成环,碳环和碳链多个碳原子还可以相互结合成环,碳环和碳链 还可以相互结合;还可以相互结合;(连接方式多)(连接方式多)(同分构体多)(同分构体多)
9、P9P9【思考与交流】【思考与交流】36.0727.99.5分子组成相同分子组成相同;链状结构链状结构结构不同,出现带有支链结构结构不同,出现带有支链结构结论结论:支链越多支链越多,沸点越低沸点越低!理解:理解:三个相同:三个相同:分子式相同分子式相同分子组成相同分子组成相同相对分子质量相同相对分子质量相同两个两个不同不同:结构不同结构不同 性质不同性质不同P10“学与问学与问”的第一问:己烷的第一问:己烷(C6H14)有有5种同分异构体种同分异构体,你能写出它们的结构式吗你能写出它们的结构式吗?并总结并总结同分异构体书写的基本规律同分异构体书写的基本规律!二、有机化合物的同分异构现象二、有机化合物的同分异构现象1. 同分异构现象和同分异构现象和同分异
温馨提示
- 1. 本站所有资源如无特殊说明,都需要本地电脑安装OFFICE2007和PDF阅读器。图纸软件为CAD,CAXA,PROE,UG,SolidWorks等.压缩文件请下载最新的WinRAR软件解压。
- 2. 本站的文档不包含任何第三方提供的附件图纸等,如果需要附件,请联系上传者。文件的所有权益归上传用户所有。
- 3. 本站RAR压缩包中若带图纸,网页内容里面会有图纸预览,若没有图纸预览就没有图纸。
- 4. 未经权益所有人同意不得将文件中的内容挪作商业或盈利用途。
- 5. 人人文库网仅提供信息存储空间,仅对用户上传内容的表现方式做保护处理,对用户上传分享的文档内容本身不做任何修改或编辑,并不能对任何下载内容负责。
- 6. 下载文件中如有侵权或不适当内容,请与我们联系,我们立即纠正。
- 7. 本站不保证下载资源的准确性、安全性和完整性, 同时也不承担用户因使用这些下载资源对自己和他人造成任何形式的伤害或损失。
最新文档
- 口腔美白操作流程
- 生物教学团队建设方案计划
- 资金需求预测报告计划
- 开展主题式教学活动计划
- 教学培训与发展计划
- 探索开放式管理促进创新与灵活性计划
- 加强财务管理的投资方向计划
- 投资咨询工程师思维训练试题及答案总结
- 投资咨询工程师财务报表解析试题及答案
- 2024年育婴师职业资格考试要点试题及答案
- 《将军胡同》阅读试题及答案
- 压力容器使用单位压力容器安全日管控、周排查、月调度制度+记录
- 法律尽职调查所需资料清单
- 118种元素原子结构示意图
- jbt11969游泳池用空气源热泵热水机电子版
- 法理学马工程教材
- 生物跟医药方面专业术语
- 轮状病毒性肠炎护理查房
- 最全的遗传概率计算方法(高中生物)题库
- 租用电表合同范本
- 广州新华学院

评论
0/150
提交评论