



版权说明:本文档由用户提供并上传,收益归属内容提供方,若内容存在侵权,请进行举报或认领
文档简介
第七章多环芳烃与非苯芳烃主要内容
多环芳烃的类型萘的结构,萘环上的亲电取代反应,取代基对反应取向的影响,萘环上的氧化还原蒽和菲的性质(芳香性和烯烃性质)几个非苯芳烃及性质简介多苯代脂烃
联苯二苯甲烷三苯甲烷二联苯三联苯多环芳烃的类型
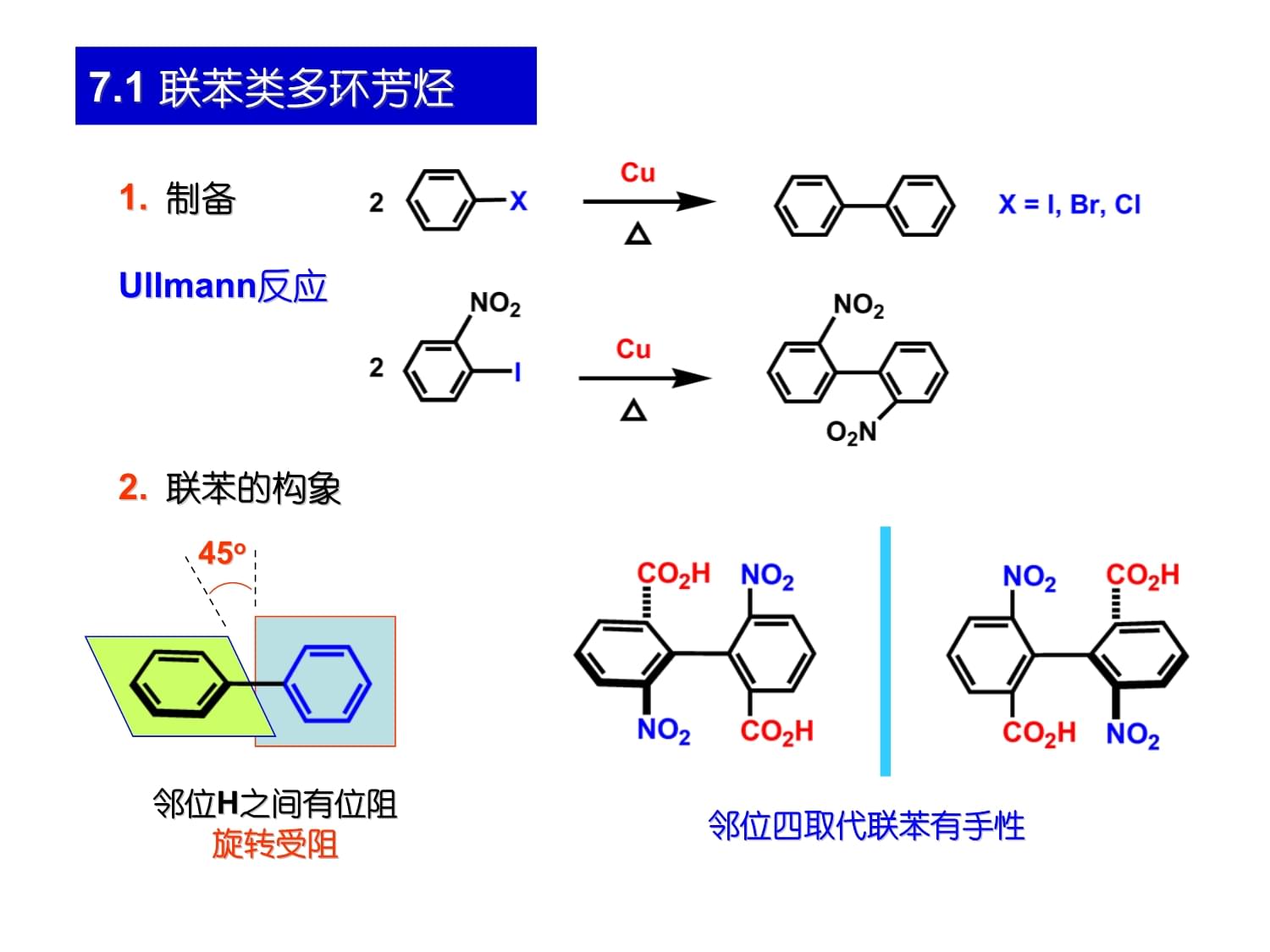
稠环芳烃萘蒽菲Ullmann反应制备联苯的构象45o邻位H之间有位阻旋转受阻邻位四取代联苯有手性7.1联苯类多环芳烃亲电取代反应思考题:写出下列两个化合物的一溴代产物一般在对位4.重要联苯衍生物--联苯胺(4,4‘-二氨基联苯)(联苯胺重排)氢化偶氮苯合成多种染料的中间体,该化合物有毒,且有致癌可能,近来很少用.萘的结构和芳香性共振能:255kJ/mol
主要反应:亲电取代芳香性:137pm140pm139pm142pm7.2稠环芳烃I——萘α位----1,4,5,8β位----2,3,6,7平面结构,所有的碳原子都是sp2杂化的,是大π键体系。萘分子中各键长有所不同,各碳原子也不完全等同:萘的共振式分析:有四种不等性C-C键,其中C1-C2双键性质最明显(键最短)只有一个环始终保持芳香性(说明另一环较为活泼)一个完整苯环二个完整苯环一个完整苯环最稳定共振式萘的共振能分析共振能255kJ/mol(小于苯共振能的二倍)
150.7kJ/mol-104kJ/mol~150
kJ/mol产物或中间体保留一个苯环在一个环上反应损失的共振能小于单个苯环的反应性质比苯活泼—容易发生加成,氧化,亲电取代通常反应发生在一个环上反应特点萘环上的亲电取代反应萘的a-位活性比b-位大,一般为a-取代(动力学控制产物)
E体积较大时为
b-取代(热力学控制产物)位阻较小E与8位H有排斥力a-取代b-取代规律:如何解释萘的a-位活性比b-位大?----由机理分析反应的取向有二个稳定的共振式(哪二个?)中间体较稳定只有一个稳定的共振式中间体较不稳定取代在a-位取代在b-位萘环上的各类亲电取代反应卤代反应和硝化反应(a-取代)萘比苯容易发生亲电取代磺化反应(取向受反应温度影响)反应温度0~40oC160oC84~85%7~15%15~16%85~93%热力学控制和动力学控制:磺化反应是可逆的,α-萘磺酸比β-萘磺酸易发生去磺酸基反应。-萘磺酸位阻大-萘磺酸位阻小-萘磺酸比-萘磺酸稳定α位活泼,反应快,但位阻大,不稳定,容易脱去;β位不活泼,难生成,但较稳定,生成后难脱去。如何解释萘的磺化反应的热力学控制和动力学控制?SO3HOHNH2碱熔法布赫雷尔反应萘的磺化反应用于制备萘的β衍生物取代基对反应取向的影响萘环上原取代基为第一类定位基---a位有给电子基例:主要产物次要产物主要产物试从反应中间体稳定性解释反应取向活化的环萘环上原取代基为第一类定位基---b位有给电子基例:动力学控制产物热力学控制产物主要主要活化的环萘环上原取代基为第二类定位------a位有吸电子基或β位有吸电子基主要产物次要产物钝化的环主要产物次要产物钝化的环例:主要少量例:45%产率31%无论原取代基在萘环的α位还是β位,新进入基团一般进入异环的α位(5位或8位)
萘环的氧化有烷基取代时邻苯二甲酸酐1,4-萘醌氧化负电荷密度较大的环萘环的还原苯在类似条件下不被还原机理?(碱)蒽的化学反应
亲电取代(芳香性)一般在9位反应例外,为什么?7.3稠环芳烃II——蒽和菲
加成和氧化(共轭双烯性质)蒽醌1,4-加成Diels-Alder反应在9、10位反应(保留二个苯环)还原氧化910共振能150.6kj/mol255kj/mol351.4kj/mol每个环共振能150128117氧化反应:难易还原反应:难易加成反应:难易苯、萘、蒽反映反应活性的比较:菲的化学反应亲电取代(芳香性)加成、氧化(烯烃性质)在9、10位反应(保留二个苯环)还原氧化芴的亚甲基上氢原子相当活泼,可被碱金属取代,化学反应水解7.4非苯系芳烃---Huckcl规则1931年,E.Huckel用分子轨道法计算了单环多烯的π电子的能级,从而提出了一个判断芳香体系的规则,称为休克尔规则。
休克尔提出,单环多烯烃要有芳香性,必须满足三个条件:(1)成环原子共平面或接近于平面,平面扭转不大于0.1nm;(2)环状闭合共轭体系(成环的原子都有与平面垂直的p轨道);(3)环上π电子数为4n+2(n=0、1、2、3……)。
一百多年前,Kekule就预见,除了苯外,可能存在其他具有芳香性的环状共轭多烯烃。如何判断芳香性?解释Huckcl规则:
单环共轭多烯(CnHn)的∏分子轨道能级--------成键轨道、非键轨道、反键轨道环多烯(CnHn)的分子轨道能级及基态电子构型
------可简便地用顶角朝下的各种正多边形来表示。充满简并的成键轨道和非键轨道的电子数正好是4的倍数,而充满能量最低的成键轨道需要两个电子
----------这就是4n+2数目合理性所在.只有成键轨道全部充满电子(有些也填满非键轨道)时,才具有芳香性。Frost圆圈法——画出单环共轭多烯(CnHn)的∏分子轨道能级环丙烯正离子电子数=2环戊二烯负离子
电子数=6环辛四烯负离子
环庚三烯正离子三苯甲基正离子电子数=6电子数=10
[10]轮烯符合4n+2规则,π电子数为10,但它轮内的氢原子具有排斥作用,致使环不能在同一平面上,故没有芳香性。把[10]-轮烯两个内部氢用一个CH2代替,减少了内部斥力,使[10]-轮烯,除-CH2-外,其它碳原子在同一平面内,具有芳香性轮烯[18]轮烯:18个π电子,符合4n+2规则。轮烯内氢原子的排斥力是很微弱,整个分子基本是处于同一平面上,具有一定芳香性。稠环化合物把Huckcl规则用于稠环芳烃,则是计算成环原子外围的Π电子数。芳香性:成环原子共平面,π电子数为4n
温馨提示
- 1. 本站所有资源如无特殊说明,都需要本地电脑安装OFFICE2007和PDF阅读器。图纸软件为CAD,CAXA,PROE,UG,SolidWorks等.压缩文件请下载最新的WinRAR软件解压。
- 2. 本站的文档不包含任何第三方提供的附件图纸等,如果需要附件,请联系上传者。文件的所有权益归上传用户所有。
- 3. 本站RAR压缩包中若带图纸,网页内容里面会有图纸预览,若没有图纸预览就没有图纸。
- 4. 未经权益所有人同意不得将文件中的内容挪作商业或盈利用途。
- 5. 人人文库网仅提供信息存储空间,仅对用户上传内容的表现方式做保护处理,对用户上传分享的文档内容本身不做任何修改或编辑,并不能对任何下载内容负责。
- 6. 下载文件中如有侵权或不适当内容,请与我们联系,我们立即纠正。
- 7. 本站不保证下载资源的准确性、安全性和完整性, 同时也不承担用户因使用这些下载资源对自己和他人造成任何形式的伤害或损失。
最新文档
- 高校干部请假管理制度
- 见习就业基地管理制度
- 供应商管理制度培训
- 算力中心建设与未来发展路径
- 生活垃圾焚烧处理厂初步设计方案解析
- 产教融合实训基地建设路径与可行性分析
- 2025年听力设备行业发展趋势与市场前景解析
- 2025至2030年中国羊毛衫衣片行业发展研究报告
- 2025至2030年中国纺织设备用传动平带市场分析及竞争策略研究报告001
- 2025至2030年中国纸板包装桶数据监测研究报告
- 普华永道财务管理与集团内部控制课件
- 2020年民办中学小升初提前招生考试语文数学整套试卷及答案
- 原子物理学:第6章 第5节 塞曼效应
- 景观人行吊桥(悬索桥)施工组织设计
- 八大特殊作业试题及答案
- 车辆转让确认书
- 二氧化碳爆破方案
- 人工智能第2章知识表示课件
- 珠三角一年断指四万
- 大学详解(敬守版)
- 某某江水利枢纽工程设计说明书与计算书

评论
0/150
提交评论