


版权说明:本文档由用户提供并上传,收益归属内容提供方,若内容存在侵权,请进行举报或认领
文档简介
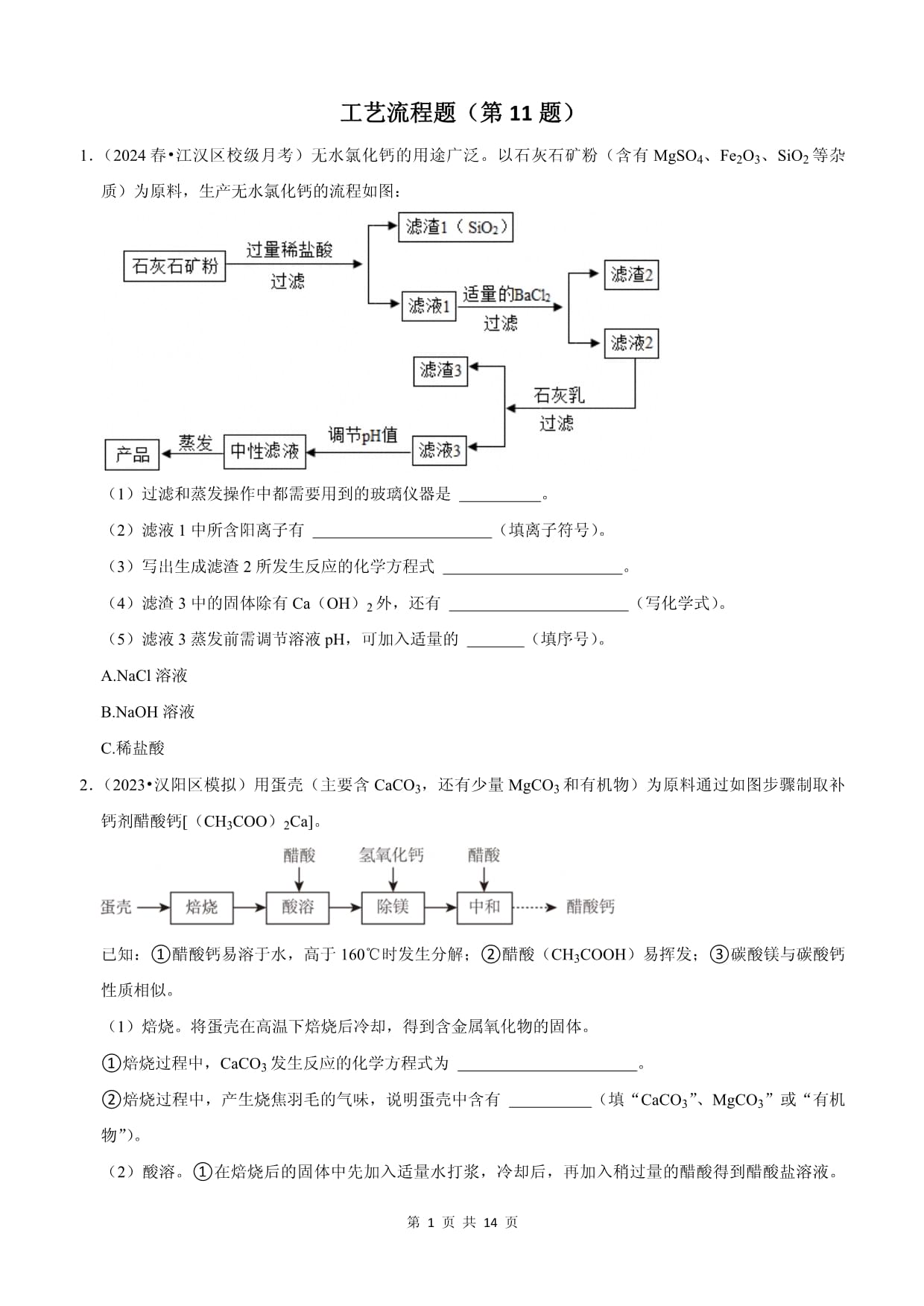
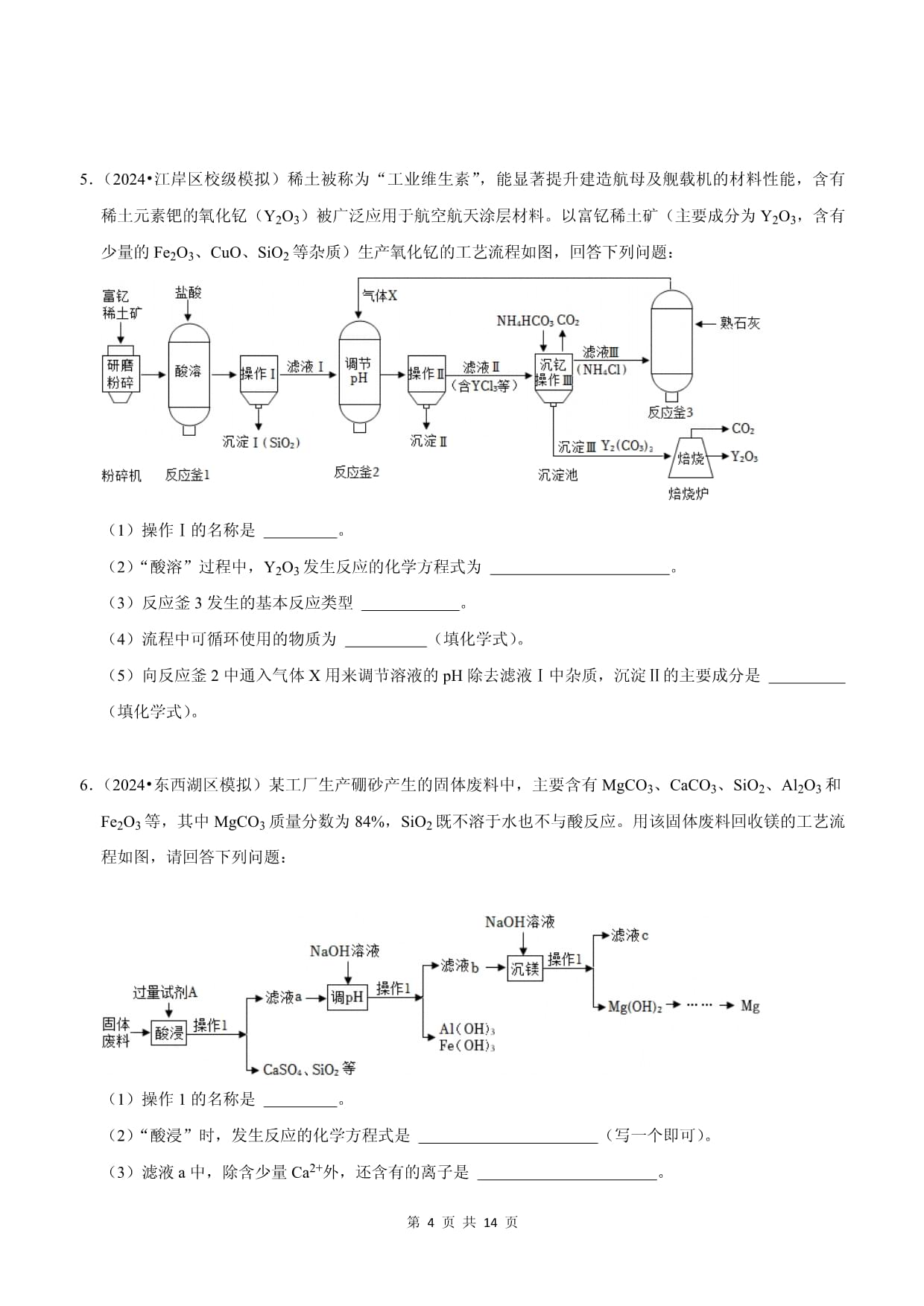
第第页工艺流程题(第11题)1.(2024春•江汉区校级月考)无水氯化钙的用途广泛。以石灰石矿粉(含有MgSO4、Fe2O3、SiO2等杂质)为原料,生产无水氯化钙的流程如图:(1)过滤和蒸发操作中都需要用到的玻璃仪器是。(2)滤液1中所含阳离子有(填离子符号)。(3)写出生成滤渣2所发生反应的化学方程式。(4)滤渣3中的固体除有Ca(OH)2外,还有(写化学式)。(5)滤液3蒸发前需调节溶液pH,可加入适量的(填序号)。A.NaCl溶液B.NaOH溶液C.稀盐酸2.(2023•汉阳区模拟)用蛋壳(主要含CaCO3,还有少量MgCO3和有机物)为原料通过如图步骤制取补钙剂醋酸钙[(CH3COO)2Ca]。已知:①醋酸钙易溶于水,高于160℃时发生分解;②醋酸(CH3COOH)易挥发;③碳酸镁与碳酸钙性质相似。(1)焙烧。将蛋壳在高温下焙烧后冷却,得到含金属氧化物的固体。①焙烧过程中,CaCO3发生反应的化学方程式为。②焙烧过程中,产生烧焦羽毛的气味,说明蛋壳中含有(填“CaCO3”、MgCO3”或“有机物”)。(2)酸溶。①在焙烧后的固体中先加入适量水打浆,冷却后,再加入稍过量的醋酸得到醋酸盐溶液。不能向焙烧后的固体中直接加入醋酸的原因是。②为提高“酸溶”步骤的反应速率,可采取的具体措施有(写1条,不考虑“搅拌”和“使用催化剂”)。(3)除镁。在酸溶后的溶液中加入Ca(OH)2至碱性,将(CH3COO)2Mg转化为Mg(OH)2沉淀除去。该反应属于(填基本反应类型)。(4)中和。在除镁后的溶液中加入醋酸调节溶液pH为7。其目的有:①将溶液中的少量Ca(OH)2转化为(CH3COO)2Ca;②。(5)将中和后的溶液蒸发浓缩至有大量晶体析出,过滤得到醋酸钙晶体。蒸发时不能直接将溶液蒸干的原因是。(6)醋酸钙高温下分解所得氧化钙可作为气体吸收剂。将(CH3COO)2Ca质量分数为94.8%的样品50.0g在高温下完全分解,计算分解得到CaO的质量(写出计算过程)。已知:①醋酸钙分解反应为(CH3COO)2Ca高温¯CaO+C3H6O↑+CO2②(CH3COO)2Ca的相对分子质量为158。3.(2024•江岸区校级模拟)硫酸铜用途广泛,比如在渔业上用作杀虫剂、杀菌剂。由废铜料(含锌)生产硫酸铜的工艺流程如图所示。回答下列问题:(1)分离固体与浸取液的操作为。(2)“酸浸”中发生反应的化学方程式为。(3)“固体乙”为。(4)工业上还可以用固体甲与浓硫酸在加热下,反应生成硫酸铜、水和一种会造成酸雨的气体,该气体中各元素的质量比为。(5)硫酸铜还对过氧化氢分解具有催化作用,为证明硫酸铜在反应前后质量不变,兴趣小组向3mL5%的过氧化氢溶液中滴入mg10%的硫酸铜溶液,充分反应后,按如图所示步骤进行实验。当m=时,证明硫酸铜在反应前后质量不变。4.(2024•江汉区一模)MgSO4•7H2O是一种重要的化工原料,某工厂以一种镁矿石(主要成分为SiO2和MgCO3,还含有少量FeCO3,其它成分忽略)为原料制备MgSO4•7H2O的主要流程如图:查阅资料:①SiO2既不溶于水也不溶于稀硫酸。②部分离子开始沉淀及完全沉淀时的pH如表所示:离子开始沉淀时的pH完全沉淀时的pHFe3+2.73.7Mg2+8.010.1③硫酸镁溶液在不同温度下进行浓缩结晶,可得到结晶水含量不同的晶体:温度/℃﹣3.9~1.81.8~48.148.1~67.567.5~200析出晶体MgSO4•12H2OMgSO4•7H2OMgSO4•6H2OMgSO4•H2O等请回答下列问题:(1)为了提高“酸溶“速率,可采取的措施有:适当升高温度、(写一种)。(2)MgCO3溶于稀硫酸的化学方程式为。(3)“氧化”过程发生反应:H2O2+2FeSO4+H2SO4═Fe2(SO4)3+2H2O,保持温度不变情况下,随着Fe2(SO4)3的生成,一段时间后观察到溶液中急速产生大量气泡,其可能原因是。(4)“调节pH”选用MgO使Fe3+转化为沉淀,调节时应控制溶液的pH范围是(填序号)。A.2.7﹣10.1B.2.7~8.0C.3.7~8.0D.3.7~10.1(5)“操作a”的具体操作是:蒸发浓缩溶液至表面有晶膜出现(此时MgSO4溶液已饱和)、、过滤、95%的乙醇洗涤、低温干燥。5.(2024•江岸区校级模拟)稀土被称为“工业维生素”,能显著提升建造航母及舰载机的材料性能,含有稀土元素钯的氧化钇(Y2O3)被广泛应用于航空航天涂层材料。以富钇稀土矿(主要成分为Y2O3,含有少量的Fe2O3、CuO、SiO2等杂质)生产氧化钇的工艺流程如图,回答下列问题:(1)操作Ⅰ的名称是。(2)“酸溶”过程中,Y2O3发生反应的化学方程式为。(3)反应釜3发生的基本反应类型。(4)流程中可循环使用的物质为(填化学式)。(5)向反应釜2中通入气体X用来调节溶液的pH除去滤液Ⅰ中杂质,沉淀Ⅱ的主要成分是(填化学式)。6.(2024•东西湖区模拟)某工厂生产硼砂产生的固体废料中,主要含有MgCO3、CaCO3、SiO2、Al2O3和Fe2O3等,其中MgCO3质量分数为84%,SiO2既不溶于水也不与酸反应。用该固体废料回收镁的工艺流程如图,请回答下列问题:(1)操作1的名称是。(2)“酸浸”时,发生反应的化学方程式是(写一个即可)。(3)滤液a中,除含少量Ca2+外,还含有的离子是。(4)若流程中镁的总损耗为10%,则100t的固体废料可回收镁的质量是。7.(2024•蔡甸区校级模拟)为缓减全球变暖趋势,中国向世界庄严承诺:“力争在2030年前实现碳达峰,2060年前实现碳中和”。其中碳捕集是实现“碳中和”的措施之一,新兴碳捕集技术的工艺流程如图所示。(1)二氧化碳气体可以被压缩的原因是。(2)从反应①的混合物中分离出CaCO3沉淀的操作是。反应②的化学方程式为。(3)整个流程中可以循环使用的物质有。8.(2024•汉阳区校级模拟)三星堆青铜器见证了中华文明的多元灿烂。生活中铜制品长期露置在潮湿空气中会锈蚀,生成“铜绿”[化学式为Cu2(OH)2CO3]。【查阅资料】铜绿能与稀硫酸反应生成硫酸铜、水和二氧化碳。【工艺流程】为从某锈蚀的铜样品中回收铜并制得硫酸锌,“取该铜样品(除含有铜、锌和铜绿外,不含其它物质),进行如图操作:请回答下列问题:(1)操作Ⅰ的名称是。(2)气体a中含有(填化学式)。(3)溶液A中的溶质有。(4)写出步骤②的一个化学方程式。(5)步骤③中加入适量稀硫酸的作用是。9.(2024•武汉模拟)过氧化钙(CaO2)是一种常用的杀菌剂和防腐剂。CaO2在常温下稳定,350℃时迅速分解生成CaO和O2。某工厂以石灰石为原料生产CaO2的工艺流程如图所示。回答下列问题:(1)“煅烧”时发生的反应属于(填基本反应类型)。(2)“水溶”时发生反应的化学方程式为。(3)“沉淀”时加入过氧化氢溶液,发生化合反应。“调pH”得到的溶液中存在的离子有。(4)CaO2样品纯度的测定。如图为测定样品中CaO2质量分数的装置(夹持装置省略,杂质不参加反应)。①检查该装置气密性的方法是。②若所取样品质量是mg,充分加热后测得生成气体体积为VmL(密度为ρg/L),则样品中CaO2的质量分数为(用代数式表示)。10.(2024•江岸区校级模拟)蛇纹石矿可以看做由MgO、Fe2O3、Al2O3、SiO2组成。由蛇纹石制取碱式碳酸镁的实验步骤如图1所示:查阅资料:A.几种物质沉淀和溶解时的pH如坐标图像所示;B.难溶性碱加热会生成两种氧化物,各元素化合价都不变。(1)操作a名称。(2)在环节Ⅰ中产生的红褐色沉淀的反应方程式是。(3)进行环节Ⅰ时,需控制溶液pH=6~7(有关沉淀与溶液pH的关系见如图2),此时没有产生沉淀的离子是(写离子符号)。Ca(OH)2不能过量,若Ca(OH)2过量,可能导致(填化学式,下同)溶解和产生另一种沉淀。(4)从沉淀混合物A中经过一些操作可提取红色氧化物作颜料,具体操作是:先向沉淀物A中加入氢氧化钠溶液调节pH>13,经过一系列操作后灼烧,得到氧化物(填化学式)做颜料。参考答案及解析1.【解答】解:(1)根据过滤和蒸发操作中可知,需要用到的玻璃仪器是玻璃棒;(2)碳酸钙和盐酸反应生成氯化钙、水和二氧化碳,氧化铁和盐酸反应生成氯化铁和水,所以滤液1中含有的所有金属阳离子的符号是:Mg2+、Fe3+、Ca2+、H+;(3)滤液1中含有氯化铁、硫酸镁和氯化钙,加入氯化钡后,氯化钡和硫酸镁反应生成了硫酸钡和氯化镁,化学方程式为BaCl2+MgSO4=MgCl2+BaSO4↓;(4)铁离子和氢氧根离子反应会生成氢氧化铁沉淀,和镁离子反应会生成氢氧化镁沉淀,所以滤渣3中的固体除有Ca(OH)2外,还有Mg(OH)2、Fe(OH)3;(5)滤液3中含有氯化钙和氢氧化钙,最后得到的是氯化钙,所以加入盐酸调节pH值,故选:C故答案为:(1)玻璃棒;(2)Mg2+、Fe3+、Ca2+、H+;(3)BaCl2+MgSO4=MgCl2+BaSO4↓;(4)Mg(OH)2、Fe(OH)3;(5)C。2.【解答】解:(1)①碳酸钙在高温的条件下生成氧化钙和二氧化碳,化学方程式为:CaCO3高温¯CaO+CO2②焙烧过程中,产生烧焦羽毛的气味,说明蛋壳中含有蛋白质,蛋白质属于有机物;(2)①在焙烧后的固体中先加入适量水打浆,冷却后,再加入稍过量的醋酸得到醋酸盐溶液。不能向焙烧后的固体中直接加入醋酸的原因是:焙烧后的固体为氧化钙,若向氧化钙固体中加入醋酸,氧化钙与水反应放热,会加速醋酸的挥发;②为提高“浸取”步骤的反应速率,可采取的具体措施有:增大硫酸的浓度,升高温度,将烧渣粉碎等;(3)醋酸镁和氢氧化钙反应生成氢氧化镁沉淀和醋酸钙,该反应属于复分解反应;(4)在除镁后的溶液中加入醋酸调节溶液pH为7。其目的有:①将溶液中的少量Ca(OH)2转化为(CH3COO)2Ca;②调节溶液的pH防止溶液吸收空气中的二氧化碳;(5)将中和后的溶液蒸发浓缩至有大量晶体析出,过滤得到醋酸钙晶体。蒸发时不能直接将溶液蒸干的原因是:醋酸钙易溶于水,高于160℃时发生分解;(6)设分解得到CaO的质量为x。(CH3COO)2Ca高温¯CaO+C3H6O↑+CO21585694.8%×50.0gx156x=16.8g答:分解得到CaO的质量是16.8g。故答案为:(1)①CaCO3高温¯CaO+CO2②有机物;(2)①焙烧后的固体为氧化钙,若向氧化钙固体中加入醋酸,氧化钙与水反应放热,会加速醋酸的挥发;②增大硫酸的浓度(或升高温度,将烧渣粉碎等);(3)复分解;(4)防止溶液吸收空气中的二氧化碳;(5)醋酸钙易溶于水,高于160℃时发生分解;(6)16.8g。3.【解答】解:(1)分离固体与浸取液的操作为过滤。(2)“酸浸”中锌和稀硫酸反应生成硫酸锌和氢气,发生反应的化学方程式为Zn+H2SO4═ZnSO4+H2↑。(3)“固体乙”为铜和氧气反应生成的氧化铜。(4)铜和浓硫酸在加热条件下生成硫酸铜、水和一种会造成酸雨的气体(由质量守恒定律:反应前后元素种类不变,该气体是二氧化硫),二氧化硫气体中各元素的质量比为32:(16×2)=1:1;(5)反应的化学方程式及其质量关系:CuSO4+Ba(OH)2═BaSO4↓+Cu(OH)2↓160233980.1mg根据题意有23.3160m=1600n当m1600n331故答案为:(1)过滤;(2)Zn+H2SO4═ZnSO4+H2↑;(3)CuO;(4)1:1;(5)1600n3314.【解答】解:(1)为了提高“酸溶“速率,可采取的措施除适当升高温度外,还可以将镁矿石粉碎,增大反应物的接触面积,故答案为:将镁矿石粉碎;(2)碳酸镁与稀硫酸反应生成硫酸镁、水和二氧化碳,故反应的化学方程式写为:MgCO3+H2SO4=MgSO4+H2O+CO2↑;故答案为:MgCO3+H2SO4=MgSO4+H2O+CO2↑;(3)实验中有过氧化氢参加反应,生成的硫酸铁作催化剂,加快过氧化氢分解的速率,产生氧气,故答案为:生成的硫酸铁作催化剂,加快过氧化氢分解的速率,产生氧气;(4)由图可知,铁离子开始沉淀的pH为2.7,完全沉淀时的pH为3.7,镁离子开始沉淀的pH为8.0,完全沉淀时的pH为10.1,选用氧化镁调节pH使铁离子转化为沉淀,应控制溶液的pH范围为3.7~8.0,避免镁离子沉淀,故答案为:C;(5)由图可知,在溶液的温度为1.8℃~48.1℃时形成的晶体是MgSO4•7H2O,所以操作a的具体操作是蒸发浓缩溶液至表面有晶膜出现(此时MgSO4溶液已饱和)、降温至1.8℃~48.1℃结晶、过滤、95%的乙醇洗涤、低温干燥,故答案为:降温至1.8℃~48.1℃结晶。5.【解答】解:(1)经过操作Ⅰ,难溶性固体和液体分离,所以操作Ⅰ是过滤;(2)盐酸能与金属氧化物反应生成盐和水,酸溶中Y2O3发生反应的化学方程式为:Y2O3+6HCl=2YCl3+3H2O;(3)由图可知,反应釜3中氯化铵与氢氧化钙反应生成氯化钙、水和氨气,属于复分解反应;(4)反应釜3中氯化铵与氢氧化钙反应生成氯化钙、水和氨气,反应釜2中又需要通入氨气,所以该流程中可循环使用的物质为NH3;(5)由图可知,反应釜1中氧化钇和盐酸反应生成氯化钇和水,氧化铁和盐酸反应生成氯化铁和水,氧化铜和盐酸反应生成氯化铜和水,向反应釜2中通入气体X使溶液呈碱性,且气体X由氯化铵和熟石灰反应生成,则气体X为氨气;气体X为氨气,溶于水后形成氨水,氨水与滤液Ⅰ中的氯化铁反应生成氯化铵和氢氧化铁沉淀,氨水与氯化铜反应生成氯化铵和氢氧化铜沉淀,则沉淀Ⅱ的主要成分是Fe(OH)3和Cu(OH)2。故答案为:(1)过滤;(2)Y2O3+6HCl=2YCl3+3H2O;(3)复分解反应;(4)NH3;(5)Fe(OH)3和Cu(OH)2。6.【解答】解:(1)操作Ⅰ将固体和液体分离,固液分离的操作是过滤;(2)由流程图“酸浸”时生成硫酸钙,故试剂A是硫酸,硫酸与碳酸钙反应生成硫酸钙、水和二氧化碳,碳酸镁和稀硫酸反应生成硫酸镁、二氧化碳和水,Al2O3和Fe2O3也会和硫酸反应生成硫酸盐和水,反应的化学方程式分别为:CaCO3+H2SO4=CaSO4+H2O+CO2↑、MgCO3+H2SO4=MgSO4+H2O+CO2↑;Al2O3+3H2SO4=Al2(SO4)3+3H2O;Fe2O3+3H2SO4=Fe2(SO4)3+3H2O;(3)硫酸钙微溶于水,碳酸镁与硫酸反应生成硫酸镁、水和二氧化碳,氧化铝与硫酸反应生成硫酸铝和水,氧化铁与硫酸反应生成硫酸铁和水,硫酸过量,故滤液a中的阳离子是Ca2+、Mg2+、Al3+、Fe3+、H+;(4)根据质量守恒定律,反应前后元素的质量不变,故回收镁的质量是即为固体废料中镁元素质量=100t×84%×24故答案为:(1)过滤;(2)CaCO3+H2SO4=CaSO4+H2O+CO2↑[或MgCO3+H2SO4=MgSO4+H2O+CO2↑;Al2O3+3H2SO4=Al2(SO4)3+3H2O;Fe2O3+3H2SO4=Fe2(SO4)3+3H2O];(3)Mg2+、Al3+、Fe3+、H+;(4)21.6t。7.【解答】解:(1)二氧化碳能被压缩是因为分子之间有间隔,加压情况下,间隔减小。(2)碳酸钠和石灰水中的氢氧化钙反应生成碳酸钙沉淀和氢氧化钠,过滤能将固体和液体分离,则操作为过滤;碳酸钙高温分解生成氧化钙和二氧化碳,反应的化学方程式为:CaCO3高温¯CaO+CO2(3)由图可知,过程中既有氢氧化钠、氢氧化钙的生成,同时流程还需要氢氧化钠和氢氧化钙,则可循环使用的物质有氢氧化钠、氢氧化钙。故答案为:(1)分子间有间隔;(2)过滤;CaCO3高温¯CaO+CO2(3)NaOH、Ca(OH)2。8.【解答】解:(1)操作Ⅰ的名称是过滤。故答案为:过滤。(2)气体a中含有锌和稀硫酸反应生成的氢气、稀硫酸和碱式碳酸铜反应生成的二氧化碳。故答案为:H2、CO2。(3)溶液A中的溶质有碱式碳酸铜和稀硫酸反应生成的硫酸铜、锌和稀硫酸反应生成的硫酸锌、过量的硫酸。故答案为:硫酸铜、硫酸锌、硫酸。(4)步骤②中,锌和稀硫酸反应生成硫酸锌和氢气,和硫酸铜反应生成硫酸锌和铜,反应的化学方程式是Zn+H2SO4═ZnSO4+H2↑、Zn+CuSO4═ZnSO4+Cu。故答案为:Zn+H2SO4═ZnSO4+H2↑或Zn+CuSO4═ZnSO4+Cu。(5)步骤③中加入适量稀硫酸的作用是把锌恰好完全转化成硫酸锌。故答案为:把锌恰好完全转化成硫酸锌。9.【解答】解:(1)“煅烧”时碳酸钙高温分解生成氧化钙和二氧化碳,该反应符合“一变多”的特点,属于分解反应;(2)“水溶”时氧化钙和水反应生成氢氧化钙,化学方程式为:CaO+H2O=Ca(OH)2;(3)“沉淀”时加入过氧化氢溶液,发生化合反应(符合“多变一”的特点),得到CaO2•8H2O,根据反应前后元素种类不变,说明是氢氧化钙和过氧化氢发生反应,根据反应前后原子种类和数目不变,则有水参与反应,化学方程式即为Ca(OH)2+H2O2+6H2O=CaO2•8H2O;说明“调pH”得到的溶液中含有氢氧化钙,显碱性,盐酸和氢氧化钙反应生成氯化钙和水,则存在的离子有钙离子、氢氧根离子、氯离子;(4)①检查该装置气密性的方法是:向右拉动注射器活塞,松手后,活塞恢复至原位,说明该
温馨提示
- 1. 本站所有资源如无特殊说明,都需要本地电脑安装OFFICE2007和PDF阅读器。图纸软件为CAD,CAXA,PROE,UG,SolidWorks等.压缩文件请下载最新的WinRAR软件解压。
- 2. 本站的文档不包含任何第三方提供的附件图纸等,如果需要附件,请联系上传者。文件的所有权益归上传用户所有。
- 3. 本站RAR压缩包中若带图纸,网页内容里面会有图纸预览,若没有图纸预览就没有图纸。
- 4. 未经权益所有人同意不得将文件中的内容挪作商业或盈利用途。
- 5. 人人文库网仅提供信息存储空间,仅对用户上传内容的表现方式做保护处理,对用户上传分享的文档内容本身不做任何修改或编辑,并不能对任何下载内容负责。
- 6. 下载文件中如有侵权或不适当内容,请与我们联系,我们立即纠正。
- 7. 本站不保证下载资源的准确性、安全性和完整性, 同时也不承担用户因使用这些下载资源对自己和他人造成任何形式的伤害或损失。
最新文档
- 注册公司的租地合同范本
- 电梯装潢承包合同协议书
- 精装销售合同协议书模板
- 水质在线监测服务协议书
- 私人饭店里劳务合同范本
- 美业门店合伙协议书范本
- 防火触电交底协议书模板
- 独家冠名广告协议书范本
- 油罐车机械租赁合同范本
- 自闭症机构与家长协议书
- 书籍保密协议书范文
- 2025年秋季学期特殊教育教学工作计划
- 基层护理进修后回院汇报
- 护理查对制度安全警示教育
- 2024年四川成都农业科技中心招聘笔试真题
- 2025年滨州生物会考试题及答案
- 公路改扩建工程地质灾害危险性评估报告
- 四川省2024年普通高等学校高职教育单独招生文化考试数学试题
- 更换气管套管流程
- 二零二五年度生物制药委托生产合作协议4篇
- 【课件】2025年中考化学一轮复习教材提升课件第一单元走进化学世界

评论
0/150
提交评论