



版权说明:本文档由用户提供并上传,收益归属内容提供方,若内容存在侵权,请进行举报或认领
文档简介
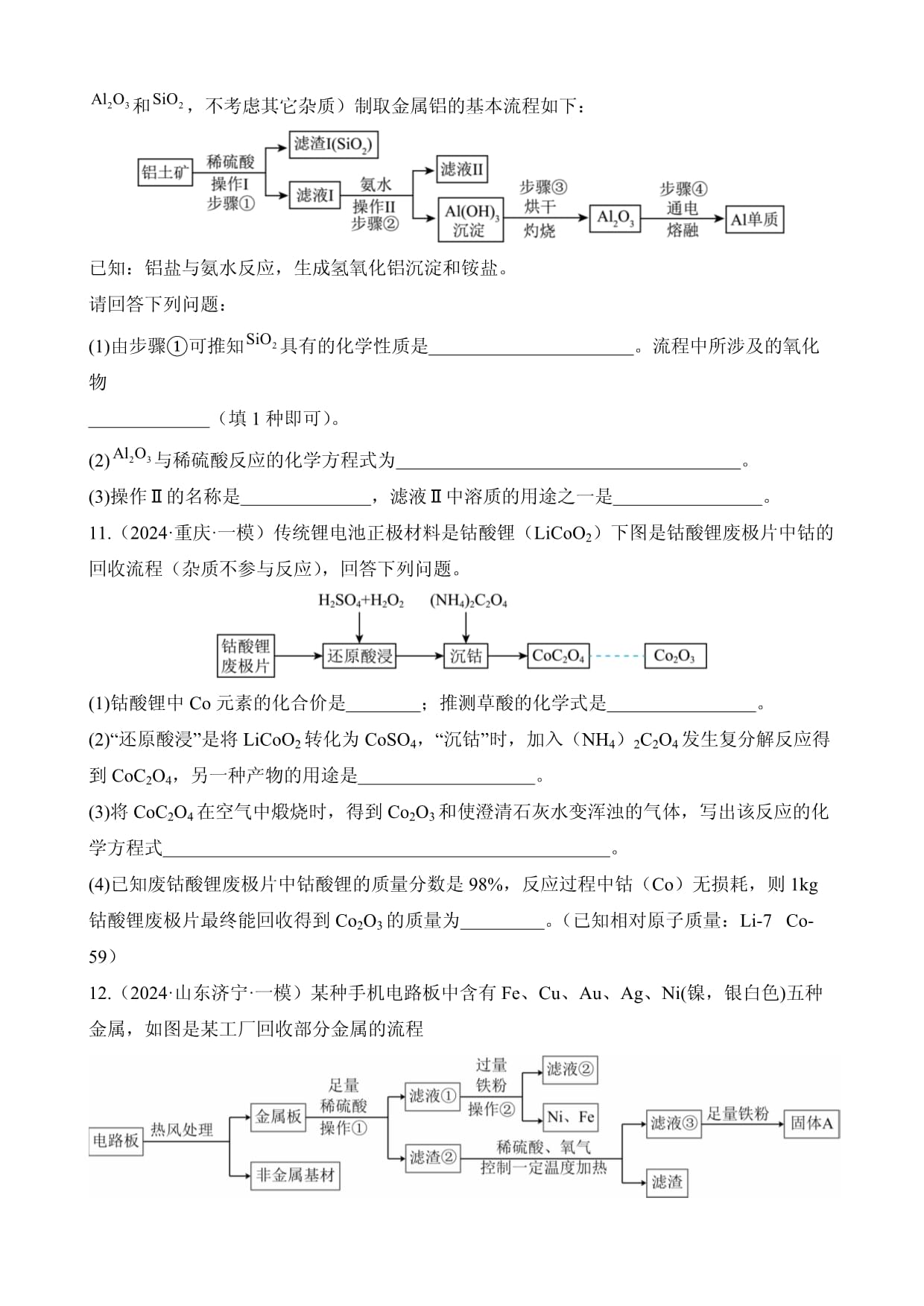
题型三工艺流程题(试题分值:100分测试时间:60分钟)一、选择题(本题包括2小题,每小题3分,共6分。每小题只有一个正确答案)1.(2023·黑龙江大庆·中考真题)某工厂的工业废水中含有大量的FeSO4和CuSO4,为减少污染并变废为宝,工厂计划从该废水中回收和金属铜,流程如图所示。下列说法不正确的是A.试剂⑤是铁粉,试剂⑦是稀盐酸B.①的成分为C.操作⑥与操作⑧均为过滤D.滤液②、④合并后经蒸发浓缩、冷却结晶、过滤、洗涤、干燥即获得FeSO4·7H2O2.(2024·河南·一模)2024年2月,几场大雪给人们的生活带来一些不便,为防止道路结冰,可向路面撒融雪剂,一种以“氯盐”又称“化冰盐”为主要成分的无机融雪剂,常用工业碳酸钙(含少量NaCl、FeCl3等杂质)为原料生产融雪剂,主要生产流程如下图:有关此流程的说法正确的是A.操作I和操作II相同B.固体甲和固体C都是纯净物C.加过量熟石灰可将Fe3+全部转化为沉淀物D.溶液B无需加盐酸,直接进行操作II也能得到C的固体二、非选择题(本题包括20小题,每空1分,共94分)3.(2023·湖北十堰·中考真题)工业上从铝土矿(主要成分为,还含有SiO2、Fe2O3等)中提取的主要流程如下:已知:①SiO2难溶于水,不与盐酸反应。②当时,完全转化为沉淀。(1)操作1的名称是。(2)在“盐酸浸取”前需将铝土矿粉碎,其目的是。(3)“煅烧”过程中反应的化学方程式是2Al(OH)3Al2O3+3X,X的化学式是。(4)向溶液2中加入过量稀氨水,生成沉淀的化学方程式为。4.(2023·内蒙古通辽·中考真题)下图是用粗硅原料(含氧化镁杂质,不考虑其他杂质与酸反应)制备高纯硅和金属镁的流程。已知:硅不与稀盐酸反应。请回答下列问题。(1)操作1的名称是。(2)上述流程中,可循环利用的物质是。(3)滤液中含有的阳离子为。(4)MgCl2制备Mg的化学方程式为。5.(2023·湖北咸宁·中考真题)兴趣小组的同学利用某废镍材料(含有金属Ni及少量Fe、Cu)回收镍,设计流程如下图所示(部分产物略去)。请根据上述流程回答下列问题:(1)过滤时,玻璃棒的作用是;(2)写出“酸浸”时发生反应的化学方程式(任写一个)。(3)过氧化氢具有氧化性,“氧化”时发生反应的化学方程式为,则X的化学式是。(4)Ni、Fe、Cu的金属活动性由强到弱的顺序为。(5)已知Fe3+和Ni2+开始沉淀和完全沉淀时的pH如表。“除铁”过程中加入NaOH溶液的目的是通过调节溶液的pH使Fe3+完全沉淀而Ni2+不沉淀,则pH的范围是(填字母序号)。开始沉淀时的pH完全沉淀时的pHFe3+2.73.2Ni2+7.28.7A.2.7≤pH<3.2 B.3.2≤pH<7.2 C.7.2≤pH<8.76.(2023·湖南衡阳·中考真题)黄铜(锌和铜的合金)在古代应用非常广泛,古人用炉甘石(),赤铜()和木炭制备黄铜,其中—种流程如下:(1)黄铜和纯铜相比较,硬度更大的是。(2)反应Ⅱ中赤铜与木炭反应生成铜和二氧化碳,请写出此反应的化学方程式。(3)黄铜与黄金外观上非常相似,请用一种方法对两者进行区分。7.(2023·湖南怀化·中考真题)海水是一种重要资源,利用海水可制取金属镁等物质。某化学兴趣小组的同学设计了如下实验流程:根据流程回答下列问题:(1)操作Ⅰ的名称是,该操作用到的玻璃仪器有烧杯,漏斗和;该仪器在操作Ⅰ中的作用是。操作Ⅰ中加入的NaOH溶液应过量,其目的是。(2)试剂X是(填名称),写出溶液A中加入试剂X发生反应的化学方程式。8.(2024·安徽宿州·一模)在进行“垃圾的分类与回收利用”的跨学科实践活动时,兴趣小组对金属垃圾(主要成分是铁、铜、氧化铁和二氧化硅)的处理及综合利用的部分工艺如图所示。请回答下列问题:(1)操作Ⅰ、Ⅱ的名称为。由此流程可推知SiO2的性质有(填字母)。A.难溶于水 B.化学性质很活泼 C.不能与稀硫酸反应(2)步骤③发生反应的基本反应类型是。(3)请写出步骤②所发生反应的化学方程式:。(4)倡导金属垃圾回收利用的意义是。9.(2024·福建漳州·一模)近年来新能源汽车使用量的剧增,加速了废旧电池的处理需求。下面是某废旧锂电池回收工艺的部分流程图。(1)前期处理中的“拆解、破碎”属于(填“物理”或“化学”)变化。(2)图中操作a的名称,甲溶液是。(3)流程图中MnO,Mn的化合价是。(4)在硫酸镍溶液中加入铁即可回收镍(Ni),得出镍的金属活动性比铁(填“强”或“弱”),该反应的化学方程式为,属于反应(填基本反应类型)。10.(2024·安徽马鞍山·一模)铝和铝合金是一类重要的金属材料、工业上用铝土矿(含有和,不考虑其它杂质)制取金属铝的基本流程如下:已知:铝盐与氨水反应,生成氢氧化铝沉淀和铵盐。请回答下列问题:(1)由步骤①可推知具有的化学性质是。流程中所涉及的氧化物(填1种即可)。(2)与稀硫酸反应的化学方程式为。(3)操作Ⅱ的名称是,滤液Ⅱ中溶质的用途之一是。11.(2024·重庆·一模)传统锂电池正极材料是钴酸锂(LiCoO2)下图是钴酸锂废极片中钴的回收流程(杂质不参与反应),回答下列问题。(1)钴酸锂中Co元素的化合价是;推测草酸的化学式是。(2)“还原酸浸”是将LiCoO2转化为CoSO4,“沉钴”时,加入(NH4)2C2O4发生复分解反应得到CoC2O4,另一种产物的用途是。(3)将CoC2O4在空气中煅烧时,得到Co2O3和使澄清石灰水变浑浊的气体,写出该反应的化学方程式。(4)已知废钴酸锂废极片中钴酸锂的质量分数是98%,反应过程中钴(Co)无损耗,则1kg钴酸锂废极片最终能回收得到Co2O3的质量为。(已知相对原子质量:Li-7
Co-59)12.(2024·山东济宁·一模)某种手机电路板中含有Fe、Cu、Au、Ag、Ni(镍,银白色)五种金属,如图是某工厂回收部分金属的流程(1)操作①的名称是。(2)写出滤液②中阳离子的符号。(3)根据以上工艺流程图,可以得到Cu、Ni、Fe的金属活动性由强到弱的顺序依次是。(4)已知滤渣②中的铜与稀硫酸、氧气在加热的条件下会生成硫酸铜和一种氧化物,写出该反应的化学方程式。13.(2024·湖南怀化·模拟预测)化学实验室要从X、银、铜、锌四种金属混合物中分离某贵重金属。流程如图所示:(未做特别说明的“固体”,可能为纯净物或混合物,X在化合物中为+2价)(1)写出①反应中产生的气体是。(2)四种金属的活动性由强到弱的顺序是。(3)滤液A中共含有种溶质,固体丙中一定含有的金属是。14.(2023·四川·中考真题)2022年春节联欢晚会中《只此青绿》呈现了宋代《千里江山图》,让我们仿佛置身于宋代的青山绿水之中、《千里江山图》里的绿色来自孔雀石,其主要成分为CuCO3•Cu(OH)2,含有FeCO3、SiO2杂质。工业上以孔雀石为原料制备重要化工原料胆矾(CuSO4•5H2O)的流程如图。回答相关问题:(1)《千里江山图》色彩依旧,说明常温下绿色颜料孔雀石的性质。(2)“酸浸”发生的反应属于四大基本反应类型中的,溶液1中含的金属阳离子有。(3)“氧化”过程中发生反应的化学方程式为:2FeSO4+H2O2+H2SO4═+2H2O(请补充完该方程式)。(4)“沉淀铁”不能将CuCO3•Cu(OH)2替换为NaOH,其原因是(任答1点)。(5)系列操作有蒸发、结晶、、洗涤、干燥。(6)加热500g胆矾至全部变成白色无水CuSO4,固体质量减轻了g(不需要写出计算过程)。15.(2024·黑龙江佳木斯·一模)海水晒盐得到的粗盐常含有、等杂质,工业提纯粗盐的流程如图所示。(1)步骤④:操作a的名称是。(2)步骤⑥:操作b中用到玻璃棒,玻璃棒的作用是。(3)如果将步骤②和步骤③的顺序颠倒,则所制得的精盐水中还含有。(4)写出步骤③中反应的化学方程式。16.(2024·黑龙江哈尔滨·一模)某工厂生产高锰酸钾的流程如下图所示,请回答下列问题。(1)氧化室内发生反应的化学方程式为。(2)电解室中化学反应前后化合价发生变化的元素有(填元素符号)。(3)生产流程中可循环利用的物质是(填化学式)。17.(2024·安徽·一模)烧碱-纯碱法净化卤水过程产生的盐泥中主要含有及少量的和。下图是实验室模拟工业上以该盐泥为原料制备的操作流程:(1)步骤①中操作a的名称是。(2)步骤③中的试剂X应选下列物质中的______(填序号)。A.KOH溶液 B.Ca(OH)2溶液C.Na2SO4溶液 D.Ca(NO3)2溶液(3)步骤②中发生中和反应的化学方程式为。(4)步骤④中“一系列操作”主要是,说明CaCl2的溶解度随温度的降低而。18.(2023·内蒙古呼和浩特·中考真题)为了实现碳减排目标,许多国家都在研究二氧化碳的减排措施,其中“碳捕捉和封存”技术是实现这一目标的重要途径之一。工业流程如图所示:请回答以下有关问题:(1)“捕捉室”中氢氧化钠溶液常喷成雾状,主要目的是。(2)“反应分离器”中涉及的化合反应的方程式为。(3)“封存室”内二氧化碳由气态变为液态,从微观角度解释变化的原因是。(4)整个过程中,可以循环利用的物质除水之外,还有(填化学式)。19.(2023·湖北荆州·中考真题)燃煤电厂利用NaOH溶液处理烟气,实现“碳捕集”,其主要转化流程如下。请回答下列问题:(1)溶液X中的溶质是。(2)写出烟气通入氢氧化钠溶液中所发生反应的化学方程式。(3)写出干冰的一种用途。(4)上述流程中可循环使用的物质有溶液X和。20.(2023·重庆·中考真题)氢气是重要的化工原料。下图是通过热化学循环用硫化氢气体(H2S)制备氢气的模拟工艺流程。(1)吸收室中生成的S可进一步燃烧为反应室提供SO2,写出该反应的化学方程式。(2)HI进入产品室中发生的反应属于(填基本反应类型)。(3)写出一种上述流程中可以循环利用的物质。(4)硫化氢气体制备氢气时生成两种单质,写出化学方程式。21.(2024·河南周口·一模)粗盐中常含有氯化钙、氯化镁、硫酸钠等杂质,某同学设计如图实验流程提纯粗盐,所加试剂分别为过量的NaOH溶液、BaCl2溶液、Na2CO3溶液和稀盐酸。请回答下列问题:(1)写出除去杂质氯化镁的化学方程式。(2)实验过程中多次用到了玻璃棒,它在过滤操作中的作用是什么?(3)若将加入的稀盐酸换为稀硫酸,则会引起的后果是什么?22.(2024·云南·一模)“氨法”捕集二氧化碳是实现“碳中和”的重要途径之一,目前受到广泛关注和研究,其主要流程如下图,请回答相关问题:(1)为了降低“碳排放”,下列建议可行的是______。A.随手关灯 B.全面禁止燃烧煤和汽油C.大力发展火力发电 D.推广使用新能源汽车(2)常温下,氨水的pH7(填“>”、“=”或“<”)。(3)工业上用氨水喷淋吸收废气中的CO2,采用“喷淋”的原因是。(4)反应①的化学方程式是,该反应的温度不宜高,原因是。(5)上述流程中,可循环利用的物质是。(6)CO2的后续处理包括利用、封存等,写出CO2的一种用途。
题型三工艺流程题(试题分值:100分测试时间:60分钟)一、选择题(本题包括2小题,每小题3分,共6分。每小题只有一个正确答案)1.(2023·黑龙江大庆·中考真题)某工厂的工业废水中含有大量的FeSO4和CuSO4,为减少污染并变废为宝,工厂计划从该废水中回收和金属铜,流程如图所示。下列说法不正确的是A.试剂⑤是铁粉,试剂⑦是稀盐酸B.①的成分为C.操作⑥与操作⑧均为过滤D.滤液②、④合并后经蒸发浓缩、冷却结晶、过滤、洗涤、干燥即获得FeSO4·7H2O【答案】A【解析】A、某工厂的工业废水中含有大量的FeSO4和CuSO4,实验目的是从该废水中回收FeSO4和金属铜,则加入的金属是铁,铁和硫酸铜反应生成硫酸亚铁和铜,试剂⑤是铁粉,过滤后,能得到硫酸亚铁溶液、铁和铜的混合物,铁能与稀硫酸反应生成硫酸亚铁和氢气,则试剂⑦是稀硫酸,不能使用稀盐酸,否则会生成氯化亚铁,故选项A说法错误;B、铁和硫酸铜反应生成硫酸亚铁和铜,试剂⑤是铁粉,过滤后,能得到硫酸亚铁溶液、铁和铜的混合物,所以①的成分为Fe、Cu,故选项B说法正确;C、操作⑥与操作⑧均为过滤,均是将金属和溶液分离,故选项C说法正确;D、滤液②、④均为硫酸亚铁溶液,合并后经蒸发浓缩、冷却结晶、过滤、洗涤、干燥即获得FeSO4·7H2O,故选项D说法正确;故选:A。2.(2024·河南·一模)2024年2月,几场大雪给人们的生活带来一些不便,为防止道路结冰,可向路面撒融雪剂,一种以“氯盐”又称“化冰盐”为主要成分的无机融雪剂,常用工业碳酸钙(含少量NaCl、FeCl3等杂质)为原料生产融雪剂,主要生产流程如下图:有关此流程的说法正确的是A.操作I和操作II相同B.固体甲和固体C都是纯净物C.加过量熟石灰可将Fe3+全部转化为沉淀物D.溶液B无需加盐酸,直接进行操作II也能得到C的固体【答案】C【解析】A、操作I将难溶性固体甲与溶液B进行了分离,属于过滤,操作II将固体C从其溶液中分离出来,属于结晶,选项错误;B、碳酸钙与稀盐酸反应生成氯化钙、水和二氧化碳,则溶液A中含有氯化铁、氯化钙和氯化钠,加入氢氧化钙后,氯化铁与氢氧化钙反应生成氯化钙和氢氧化铁沉淀,熟石灰微溶于水,过量的熟石灰和氢氧化铁沉淀会被过滤出来,因此固体甲中有氢氧化铁和熟石灰,属于混合物,而滤液中的剩余氢氧化钙与所加入的盐酸反应生成氯化钙,蒸发结晶后得到的C是氯化钠和氯化钙固体,因此甲和C都是混合物,选项错误;C、氯化铁与氢氧化钙反应生成氯化钙和氢氧化铁沉淀,则加过量熟石灰可将Fe3+全部转化为沉淀物,选项正确;D、由B可知,溶液A中含有氯化铁、氯化钙和氯化钠,加入氢氧化钙后,加入过量熟石灰后,熟石灰只与氢氧化铁反应生成氯化钙和氢氧化铁沉淀,则溶液B中含有氯化钠、氯化钙和过量的氢氧化钙,直接进行操作II得到固体中含有氯化钠、氯化钙和过量的氢氧化钙与蒸发结晶后得到的C是氯化钠和氯化钙固体不同,选项错误;故选C。二、非选择题(本题包括20小题,每空1分,共94分)3.(2023·湖北十堰·中考真题)工业上从铝土矿(主要成分为,还含有SiO2、Fe2O3等)中提取的主要流程如下:已知:①SiO2难溶于水,不与盐酸反应。②当时,完全转化为沉淀。(1)操作1的名称是。(2)在“盐酸浸取”前需将铝土矿粉碎,其目的是。(3)“煅烧”过程中反应的化学方程式是2Al(OH)3Al2O3+3X,X的化学式是。(4)向溶液2中加入过量稀氨水,生成沉淀的化学方程式为。【答案】(1)过滤(2)增大与酸的接触面积,反应进行的更充分(3)H2O(4)AlCl3+3NH3·H2O=3NH4Cl+Al(OH)3↓【解析】(1)经过操作1后物质被分成溶液和不溶物两部分,说明操作1起到固液分离的作用,故填过滤;(2)在“盐酸浸取”前需将铝土矿粉碎,其目的是:增大与酸的接触面积,反应进行的更充分;(3)根据质量守恒定律反应前后原子的种类和数目不变进行判断,反应物中有Al:2、O:6、H:6,生成物有Al:2、O:3,所以3X含有O原子3个,H原子6个,X中含有2个H原子和1个O原子,则X的化学式为:H2O;(4)根据实验流程可以判断出溶液2为氯化铝(氧化铝和盐酸反应生成氯化铝和水)溶液,氯化铝与氨水反应生成氯化铵和氢氧化铝,故化学方程式为:AlCl3+3NH3·H2O=3NH4Cl+Al(OH)3↓。4.(2023·内蒙古通辽·中考真题)下图是用粗硅原料(含氧化镁杂质,不考虑其他杂质与酸反应)制备高纯硅和金属镁的流程。已知:硅不与稀盐酸反应。请回答下列问题。(1)操作1的名称是。(2)上述流程中,可循环利用的物质是。(3)滤液中含有的阳离子为。(4)MgCl2制备Mg的化学方程式为。【答案】(1)过滤(2)HCl、Cl2(3)Mg2+、H+(4)MgCl2Mg+Cl2↑【解析】(1)操作1实现了固液分离,名称是过滤;(2)由图可知,HCl、Cl2既是反应物,又是生成物,可以循环利用;(3)氧化镁和稀盐酸反应生成氯化镁和水,硅和其它杂质与稀盐酸不反应,稀盐酸过量,故滤液中含有的阳离子为:Mg2+、H+;(4)氯化镁在通电的条件下反应生成镁和氯气,该反应的化学方程式为:MgCl2Mg+Cl2↑。5.(2023·湖北咸宁·中考真题)兴趣小组的同学利用某废镍材料(含有金属Ni及少量Fe、Cu)回收镍,设计流程如下图所示(部分产物略去)。请根据上述流程回答下列问题:(1)过滤时,玻璃棒的作用是;(2)写出“酸浸”时发生反应的化学方程式(任写一个)。(3)过氧化氢具有氧化性,“氧化”时发生反应的化学方程式为,则X的化学式是。(4)Ni、Fe、Cu的金属活动性由强到弱的顺序为。(5)已知Fe3+和Ni2+开始沉淀和完全沉淀时的pH如表。“除铁”过程中加入NaOH溶液的目的是通过调节溶液的pH使Fe3+完全沉淀而Ni2+不沉淀,则pH的范围是(填字母序号)。开始沉淀时的pH完全沉淀时的pHFe3+2.73.2Ni2+7.28.7A.2.7≤pH<3.2 B.3.2≤pH<7.2 C.7.2≤pH<8.7【答案】(1)引流(2)Fe+H2SO4===FeSO4+H2↑/Ni+H2SO4===NiSO4+H2↑(3)H2O(4)Fe、Ni、Cu(合理表述即可)(5)B【解析】(1)过滤时,玻璃棒的作用为引流。(2)在金属活动性顺序中,铁>氢>铜,则铁能与盐酸反应生成硫酸亚铁和氢气,又由于滤液Ⅰ中含有镍离子,则说明镍能与盐酸反应生成硫酸镍和氢气,反应的化学方程式为Fe+H2SO4===FeSO4+H2↑或Ni+H2SO4===NiSO4+H2↑。(3)反应前后,原子的种类和个数不变,等号左边有2Fe、3S、4H和14O,等号右边除2X外,有2Fe、3S和12O,则2X中含有4H和2O,则X的化学式为H2O。(4)结合流程可知,加入向滤液Ⅱ加入铁粉能置换出镍,则说明铁比镍活泼,则金属活动性顺序铁>镍>铜。(5)由于Fe3+完全沉淀时pH为3.2,而Ni2+开始沉淀时的pH为7.2,则若想使Fe3+完全沉淀而Ni2+不沉淀,pH的范围为3.2~7.2,故选B。6.(2023·湖南衡阳·中考真题)黄铜(锌和铜的合金)在古代应用非常广泛,古人用炉甘石(),赤铜()和木炭制备黄铜,其中—种流程如下:(1)黄铜和纯铜相比较,硬度更大的是。(2)反应Ⅱ中赤铜与木炭反应生成铜和二氧化碳,请写出此反应的化学方程式。(3)黄铜与黄金外观上非常相似,请用一种方法对两者进行区分。【答案】(1)黄铜(2)(3)取少量两者置于试管中,向试管中加入适量稀盐酸,有气泡生成的是黄铜,无明显现象的是黄金【解析】(1)合金的强度和硬度一般比组成它们的纯金属更高,抗腐蚀性也更好,黄铜是锌和铜的合金,故硬度更大的是黄铜;(2)反应Ⅱ中赤铜与木炭在1100℃~1300℃时反应生成铜和二氧化碳气体,化学方程式为;(3)黄铜是锌和铜的合金,锌可以与稀盐酸反应生成氢气和氯化锌,而黄金化学性质稳定,不与稀盐酸反应,故区分方法是:取少量两者置于试管中,向试管中加入适量稀盐酸,有气泡生成的是黄铜,无明显现象的是黄金。7.(2023·湖南怀化·中考真题)海水是一种重要资源,利用海水可制取金属镁等物质。某化学兴趣小组的同学设计了如下实验流程:根据流程回答下列问题:(1)操作Ⅰ的名称是,该操作用到的玻璃仪器有烧杯,漏斗和;该仪器在操作Ⅰ中的作用是。操作Ⅰ中加入的NaOH溶液应过量,其目的是。(2)试剂X是(填名称),写出溶液A中加入试剂X发生反应的化学方程式。【答案】(1)过滤玻璃棒引流将MgCl2完全转化为Mg(OH)2沉淀(2)稀盐酸NaOH+HCl=NaCl+H2O【解析】(1)根据流程图可知操作Ⅰ为固液分离,则为过滤操作;过滤操作中需要用到的仪器为铁架台(带铁圈)、烧杯、漏斗、玻璃棒,其中烧杯、漏斗、玻璃棒为玻璃仪器;过滤操作中玻璃棒的作用为引流,防止液体溅出;NaOH能与MgCl2反应生成Mg(OH)2沉淀与NaCl,实验中需要加过量的NaOH,可以将MgCl2完全转化为Mg(OH)2沉淀;(2)MgCl2溶液中含有少量的NaCl,加入过量的NaOH溶液,反应后过滤得到的滤液A中溶质为NaOH、NaCl,固体B为Mg(OH)2;NaOH能与HCl反应生成NaCl与H2O,Mg(OH)2能与HCl反应生成MgCl2与H2O,则X试剂为稀盐酸;溶液A中NaOH与稀盐酸反应的化学反应方程式为:NaOH+HCl=NaCl+H2O。8.(2024·安徽宿州·一模)在进行“垃圾的分类与回收利用”的跨学科实践活动时,兴趣小组对金属垃圾(主要成分是铁、铜、氧化铁和二氧化硅)的处理及综合利用的部分工艺如图所示。请回答下列问题:(1)操作Ⅰ、Ⅱ的名称为。由此流程可推知SiO2的性质有(填字母)。A.难溶于水 B.化学性质很活泼 C.不能与稀硫酸反应(2)步骤③发生反应的基本反应类型是。(3)请写出步骤②所发生反应的化学方程式:。(4)倡导金属垃圾回收利用的意义是。【答案】(1)过滤AC/CA(2)复分解反应(3)3H2SO4+Fe2O3===Fe2(SO4)3+3H2O(4)节约金属资源,减少环境污染【解析】(1)根据题目给出的流程图和信息:I、II均将固液分离,为过滤操作;由流程中加入稀硫酸后,二氧化硅为固体形式未变,可知二氧化硅难溶于水、不能与稀硫酸反应,不能得出化学性质很活泼的结论。故选AC;(2)步骤③中,硫酸铁和氢氧化钠反应生成氢氧化铁和硫酸钠,该反应是由两种化合物相互交换成分生成两种化合物的反应,属于复分解反应;(3)步骤②中,氧化铁和硫酸反应生成硫酸铁和水,化学方程式为:Fe2O3+3H2SO4=Fe2(SO4)3+3H2O;(4)倡导金属垃圾回收利用既可以减少环境的污染,又可以节约资源和能源。9.(2024·福建漳州·一模)近年来新能源汽车使用量的剧增,加速了废旧电池的处理需求。下面是某废旧锂电池回收工艺的部分流程图。(1)前期处理中的“拆解、破碎”属于(填“物理”或“化学”)变化。(2)图中操作a的名称,甲溶液是。(3)流程图中MnO,Mn的化合价是。(4)在硫酸镍溶液中加入铁即可回收镍(Ni),得出镍的金属活动性比铁(填“强”或“弱”),该反应的化学方程式为,属于反应(填基本反应类型)。【答案】(1)物理(2)过滤稀硫酸(3)+2价(4)弱Fe+NiSO4===FeSO4+Ni置换【解析】(1)前期处理中的“拆解、破碎”,该过程中没有新物质生成,故属于物理变化;(2)分离固液的操作是过滤,故图中操作a的名称为过滤;由流程图可知,往Ni、Co、MnO的混合物中加入甲溶液得到NiSO4、CoSO4、MnSO4,说明该过程中发生的反应为酸与金属、金属氧化物反应生成盐,根据质量守恒定律化学反应前后元素种类不变可知,甲溶液为稀硫酸;(3)MnO中氧元素的化合价为-2价,根据在化合物中各元素化合价代数和为零可得Mn的化合价为+2价;(4)在硫酸镍溶液中加入铁即可回收镍(Ni),说明镍的金属活动性比铁弱;硫酸镍与铁反应生成镍与硫酸亚铁,该反应的化学方程式为Fe+NiSO4===FeSO4+Ni;该反应为一种单质与一种化合物反应生成另一种单质和另一种化合物,属于置换反应。10.(2024·安徽马鞍山·一模)铝和铝合金是一类重要的金属材料、工业上用铝土矿(含有和,不考虑其它杂质)制取金属铝的基本流程如下:已知:铝盐与氨水反应,生成氢氧化铝沉淀和铵盐。请回答下列问题:(1)由步骤①可推知具有的化学性质是。流程中所涉及的氧化物(填1种即可)。(2)与稀硫酸反应的化学方程式为。(3)操作Ⅱ的名称是,滤液Ⅱ中溶质的用途之一是。【答案】(1)不与酸反应二氧化硅或氧化铝(2)Al2O3+3H2SO4=Al2(SO4)3+3H2O(3)过滤作氮肥【解析】(1)由步骤①加入稀硫酸过滤可得到滤渣二氧化硅,则说明二氧化硅具有不与酸反应的化学性质;氧化物是由两种元素组成,其中一种是氧元素的化合物,流程中所涉及的氧化物二氧化硅、氧化铝;(2)Al2O3与稀硫酸反应生成硫酸铝和水,化学方程式为:Al2O3+3H2SO4=Al2(SO4)3+3H2O;(3)操作Ⅱ分离固体与液体的操作,是过滤操作;硫酸铝与氨水反应生成氢氧化铝沉淀和硫酸铵,滤液Ⅱ中溶质为硫酸铵,硫酸铵只含有氮、磷、钾三种元素中的氮元素,可以做氮肥。11.(2024·重庆·一模)传统锂电池正极材料是钴酸锂(LiCoO2)下图是钴酸锂废极片中钴的回收流程(杂质不参与反应),回答下列问题。(1)钴酸锂中Co元素的化合价是;推测草酸的化学式是。(2)“还原酸浸”是将LiCoO2转化为CoSO4,“沉钴”时,加入(NH4)2C2O4发生复分解反应得到CoC2O4,另一种产物的用途是。(3)将CoC2O4在空气中煅烧时,得到Co2O3和使澄清石灰水变浑浊的气体,写出该反应的化学方程式。(4)已知废钴酸锂废极片中钴酸锂的质量分数是98%,反应过程中钴(Co)无损耗,则1kg钴酸锂废极片最终能回收得到Co2O3的质量为。(已知相对原子质量:Li-7
Co-59)【答案】(1)+3H2C2O4(2)作氮肥(3)4CoC2O4+3O24Co2O3+8CO2(4)0.83kg/0.83千克【解析】(1)根据化合物中各元素政府化合价代数和为0,在LiCoO2中,锂元素是+1价,氧元素-2价,故Co元素化合价为+3价;铵根化合价为+1价,根据草酸铵化学式可知,草酸根的化合价为-2价,氢元素化合价为+1价,故草酸的化学式是H2C2O4;(2)草酸铵与硫酸钴反应生成草酸钴和硫酸铵,硫酸铵含有氮元素,可用作氮肥;(3)草酸钴和氧气在高温条件下生成三氧化二钴和二氧化碳气体,方程式是4CoC2O4+3O24Co2O3+8CO2;(4)化学反应前后元素种类和质量不变,最终回收Co2O3的质量为x,x=0.83kg。12.(2024·山东济宁·一模)某种手机电路板中含有Fe、Cu、Au、Ag、Ni(镍,银白色)五种金属,如图是某工厂回收部分金属的流程(1)操作①的名称是。(2)写出滤液②中阳离子的符号。(3)根据以上工艺流程图,可以得到Cu、Ni、Fe的金属活动性由强到弱的顺序依次是。(4)已知滤渣②中的铜与稀硫酸、氧气在加热的条件下会生成硫酸铜和一种氧化物,写出该反应的化学方程式。【答案】(1)过滤(2)Fe2+(3)Fe>Ni>Cu(4)2Cu+O2+2H2SO42CuSO4+2H2O【解析】(1)由图可知,通过操作①可将固体和液体分离,则其名称为过滤。(2)由于通过操作②后得到了镍和铁,则说明滤液①中含有镍离子,则向金属板中加入硫酸时,铁和硫酸反应生成硫酸亚铁和氢气,镍和硫酸反应生成硫酸镍和氢气,加入铁粉时,铁和硫酸镍反应生成镍和硫酸亚铁,则滤液②中的溶质为硫酸亚铁,其中的阳离子为Fe2+。(3)结合前面分析可知,铁、镍能和硫酸反应,但铜不能和硫酸反应,则说明铜最不活泼,且铁能将镍从硫酸镍中置换出来,则说明铁比镍活泼,则说明金属活动性顺序:铁>镍>铜。(4)铜和氧气、硫酸在加热条件下生成硫酸铜和一种氧化物,根据反应前后元素的种类不变,则生成的氧化物为水,反应的化学方程式为:2Cu+O2+2H2SO42CuSO4+2H2O。13.(2024·湖南怀化·模拟预测)化学实验室要从X、银、铜、锌四种金属混合物中分离某贵重金属。流程如图所示:(未做特别说明的“固体”,可能为纯净物或混合物,X在化合物中为+2价)(1)写出①反应中产生的气体是。(2)四种金属的活动性由强到弱的顺序是。(3)滤液A中共含有种溶质,固体丙中一定含有的金属是。【答案】(1)氢气/H2(2)Zn>X>Cu>Ag(3)3/三银/Ag【解析】(1)锌能与稀硫酸反应生成氢气和硫酸锌,因此反应①中产生的气体是氢气;(2)向金属混合物中加入一定量的稀硫酸,锌能与稀硫酸反应生成氢气和硫酸锌,铜、银不能与稀硫酸反应,X无法得出结论;向滤液A中加入过量锌,过滤后得到固体混合物乙,说明乙中有锌和X,则在反应①中X能与稀硫酸反应生成X的硫酸盐,在反应②中锌能置换出X的硫酸盐中的X,说明锌比X活泼,则在金属活动性顺序里,锌和X排在氢前面,铜和银排在氢后面,故四种金属的活动性由强到弱的顺序是锌>X>铜>银;(3)由第(2)小问分析可知,向金属混合物中加入一定量的稀硫酸,锌能与稀硫酸反应生成氢气和硫酸锌,X能与稀硫酸反应生成氢气和X的硫酸盐,向滤液A中加入过量锌,得到气体,说明滤液A中含有过量的稀硫酸,故滤液A中含有硫酸锌、硫酸、X的硫酸盐三种溶质;由金属活动性氢>铜>银可知,固体甲为铜、银,向固体甲中加入一定质量的硝酸银溶液,铜与硝酸银反应生成银和硝酸铜,因此固体丙中一定有银,由于不知道铜与硝酸银溶液是否恰好完全反应,因此无法确定固体丙中是否含有铜。14.(2023·四川·中考真题)2022年春节联欢晚会中《只此青绿》呈现了宋代《千里江山图》,让我们仿佛置身于宋代的青山绿水之中、《千里江山图》里的绿色来自孔雀石,其主要成分为CuCO3•Cu(OH)2,含有FeCO3、SiO2杂质。工业上以孔雀石为原料制备重要化工原料胆矾(CuSO4•5H2O)的流程如图。回答相关问题:(1)《千里江山图》色彩依旧,说明常温下绿色颜料孔雀石的性质。(2)“酸浸”发生的反应属于四大基本反应类型中的,溶液1中含的金属阳离子有。(3)“氧化”过程中发生反应的化学方程式为:2FeSO4+H2O2+H2SO4═+2H2O(请补充完该方程式)。(4)“沉淀铁”不能将CuCO3•Cu(OH)2替换为NaOH,其原因是(任答1点)。(5)系列操作有蒸发、结晶、、洗涤、干燥。(6)加热500g胆矾至全部变成白色无水CuSO4,固体质量减轻了g(不需要写出计算过程)。【答案】(1)稳定(2)复分解反应铜离子、亚铁离子(3)Fe2(SO4)3(4)防止带入钠离子(5)过滤(6)180【解析】(1)《千里江山图》色彩依旧,说明其上的物质较为稳定,较长时间也没有和其他物质反应。所以常温下绿色颜料孔雀石的性质稳定。(2)“酸浸”时,稀硫酸和碳酸铜反应生成硫酸铜、水和二氧化碳,和氢氧化铜反应生成硫酸铜和水,和碳酸亚铁反应生成硫酸亚铁、水和二氧化碳,都是两种化合物交换成分,生成新的化合物的反应,都属于四大基本反应类型中的复分解反应。溶液1中含的金属阳离子有铜离子、亚铁离子。(3)化学反应前后原子的种类和数目不变,反应前铁原子是2个,反应后应该是2个,包含在未知物质中,反应前硫原子是3个,反应后应该是3个,包含在未知物质中,反应前氧原子是14个,反应后应该是14个,其中12个包含在未知物质中,反应前后氢原子都是4个。所以未知物质包含2个铁原子、3个硫原子、12个氧原子,为Fe2(SO4)3,前面的化学计量数为1,不写。(4)除杂过程应避免引入杂质。“沉淀铁”不能将CuCO3•Cu(OH)2替换为NaOH,原因是防止带入钠离子。(5)沉铁后的溶液2是硫酸铜溶液,胆矾是五水硫酸铜,所以系列操作是硫酸铜结晶的过程,为蒸发、结晶、过滤(将结晶出的胆矾和液体分开)、洗涤、干燥。(6)胆矾加热减少的是结晶水的质量。500g胆矾中结晶水的质量为,所以固体质量减轻了180g。15.(2024·黑龙江佳木斯·一模)海水晒盐得到的粗盐常含有、等杂质,工业提纯粗盐的流程如图所示。(1)步骤④:操作a的名称是。(2)步骤⑥:操作b中用到玻璃棒,玻璃棒的作用是。(3)如果将步骤②和步骤③的顺序颠倒,则所制得的精盐水中还含有。(4)写出步骤③中反应的化学方程式。【答案】(1)过滤(2)搅拌,防止局部温度过高,造成液体飞溅(3)氯化钙/CaCl2(4)CaCl2+Na2CO3=CaCO3↓+2NaCl、Ca(OH)2+Na2CO3=CaCO3↓+2NaOH【解析】(1)步骤④操作a是将沉淀与滤液分离,该操作的名称为过滤;(2)步骤⑥操作b是从精盐水中获得精盐,氯化钠的溶解度受温度影响变化不大,采用的方法是蒸发;蒸发操作中玻璃棒的作用是搅拌,防止局部温度过高,造成液体飞溅;(3)步骤②和步骤③分别是加入过量的氢氧化钙溶液、碳酸钠溶液,分别是用于除去粗盐中的氯化镁、氯化钙的,但是加入碳酸钠溶液要放在加入的氢氧化钙溶液之后,这样碳酸钠会除去反应剩余的氢氧化钙;如果将步骤②和步骤③的顺序颠倒,过量的氢氧化钙与步骤⑤中加入的稀盐酸反应生成氯化钙,则所制得的精盐水中还含有:氯化钙;(4)步骤②中加入过量的氢氧化钙,氢氧化钙和氯化镁反应生成氢氧化镁沉淀和氯化钙;步骤③中加入过量的碳酸钠溶液,碳酸钠和氯化钙反应生成碳酸钙沉淀和氯化钠,碳酸钠和步骤②中过量的氢氧化钙反应生成碳酸钙沉淀和氢氧化钠,化学方程式为:CaCl2+Na2CO3=CaCO3↓+2NaCl、Ca(OH)2+Na2CO3=CaCO3↓+2NaOH。16.(2024·黑龙江哈尔滨·一模)某工厂生产高锰酸钾的流程如下图所示,请回答下列问题。(1)氧化室内发生反应的化学方程式为。(2)电解室中化学反应前后化合价发生变化的元素有(填元素符号)。(3)生产流程中可循环利用的物质是(填化学式)。【答案】(1)2MnO2+O2+4KOH=2K2MnO4+2H2O(2)Mn、H(3)KOH【解析】(1)氧化室内发生反应为二氧化锰、氧气、氢氧化钾反应生成锰酸钾和水,反应的化学方程式:2MnO2+O2+4KOH=2K2MnO4+2H2O,故填:2MnO2+O2+4KOH=2K2MnO4+2H2O;(2)“电解室”反应中,锰酸钾和水通电反应生成高锰酸钾、氢气和氢氧化钾,锰酸钾中钾元素显+1价,氧元素显-2价,锰元素显+6价,水中氢元素显+1价,氧元素显-2价,高锰酸钾中钾元素显+1价,氧元素显-2价,锰元素显+7价,氢气中氢元素化合价为0,氢氧化钾中钾元素显+1价,氢元素显+1价,氧元素显-2价,反应前后化合价发生变化的元素有锰元素(+6价变为+7价)、氢元素(+1价变为0价),故填:Mn、H。(3)由生产流程知,氢氧化钾既是反应物,又是生成物,则可循环利用的物质是KOH,故填:KOH。17.(2024·安徽·一模)烧碱-纯碱法净化卤水过程产生的盐泥中主要含有及少量的和。下图是实验室模拟工业上以该盐泥为原料制备的操作流程:(1)步骤①中操作a的名称是。(2)步骤③中的试剂X应选下列物质中的______(填序号)。A.KOH溶液 B.Ca(OH)2溶液C.Na2SO4溶液 D.Ca(NO3)2溶液(3)步骤②中发生中和反应的化学方程式为。(4)步骤④中“一系列操作”主要是,说明CaCl2的溶解度随温度的降低而。【答案】(1)过滤(2)B(3)2HCl+Mg(OH)2=MgCl2+2H2O(4)降温结晶(合理表述即可)减小(合理表述即可)【解析】(1)步骤①中操作a实现了固液分离,名称是过滤;(2)A、氢氧化钾能与氯化镁反应生成氢氧化镁和氯化钾,虽然除去了氯化镁,但是引入了新的杂质氯化钾,不符合题意;B、氢氧化钙能与氯化镁反应生成氢氧化镁和氯化钙,除去了氯化镁,也没有引入新的杂质,符合题意;C、硫酸钠和氯化镁不反应,无法除去氯化镁,不符合题意;D、硝酸钙和氯化镁不反应,无法除去硝酸钙,不符合题意。故选B;(3)步骤②中发生中和反应的反应为氢氧化镁和盐酸反应生成氯化镁和水,该反应的化学方程式为:2HCl+Mg(OH)2=MgCl2+2H2O;(4)步骤④将氯化钙溶液经过一系列操作得到氯化钙,“一系列操作”主要是降温结晶,因为氯化钙的溶解度随温度的降低而减小,降低温度,氯化钙的溶解度减小,氯化钙结晶析出。18.(2023·内蒙古呼和浩特·中考真题)为了实现碳减排目标,许多国家都在研究二氧化碳的减排措施,其中“碳捕捉和封存”技术是实现这一目标的重要途径之一。工业流程如图所示:请回答以下有关问题:(1)“捕捉室”中氢氧化钠溶液常喷成雾状,主要目的是。(2)“反应分离器”中涉及的化合反应的方程式为。(3)“封存室”内二氧化碳由气态变为液态,从微观角度解释变化的原因是。(4)整个过程中,可以循环利用的物质除水之外,还有(填化学式)。【答案】(1)增大反应物接触面接,使反应更充分(2)CaO+H2O===Ca(OH)2(3)分子间的间隔减小(4)CaO、NaOH【解析】(1)将氢氧化钠溶液喷成雾状,能增大反应物的接触面积,使反应更充分。(2)煅烧炉中碳酸钙高温分解为氧化钙和二氧化碳,则物质A为氧化钙,氧化钙能与水反应生成氢氧化钙,而氢氧化钙能与碳酸钠反应生成碳酸钙沉淀和水,则“反应分离器”中涉及的化合反应的方程式为:CaO+H2O===Ca(OH)2。(3)二氧化碳由气态变为液态,分子间的间隔改变。(4)由流程可知,反应过程中除水之外,既有氧化钙和氢氧化钠生成,又需要氧化钙和氢氧化钠参与,则可循环利用的物质还有氧化钙和氢氧化钠。19.(2023·湖北荆州·中考真题)燃煤电厂利用NaOH溶液处理烟气,实现“碳捕集”,其主要转化流程如下。请回答下列问题:(1)溶液X中的溶质是。(2)写出烟气通入氢氧化钠溶液中所发生反应的化学方程式。(3)写出干冰的一种用途。(4)上述流程中可循环使用的物质有溶液X和。【答案】(1)NaOH/氢氧化钠 (2)2NaOH+CO2===Na2CO3+H2O(3
温馨提示
- 1. 本站所有资源如无特殊说明,都需要本地电脑安装OFFICE2007和PDF阅读器。图纸软件为CAD,CAXA,PROE,UG,SolidWorks等.压缩文件请下载最新的WinRAR软件解压。
- 2. 本站的文档不包含任何第三方提供的附件图纸等,如果需要附件,请联系上传者。文件的所有权益归上传用户所有。
- 3. 本站RAR压缩包中若带图纸,网页内容里面会有图纸预览,若没有图纸预览就没有图纸。
- 4. 未经权益所有人同意不得将文件中的内容挪作商业或盈利用途。
- 5. 人人文库网仅提供信息存储空间,仅对用户上传内容的表现方式做保护处理,对用户上传分享的文档内容本身不做任何修改或编辑,并不能对任何下载内容负责。
- 6. 下载文件中如有侵权或不适当内容,请与我们联系,我们立即纠正。
- 7. 本站不保证下载资源的准确性、安全性和完整性, 同时也不承担用户因使用这些下载资源对自己和他人造成任何形式的伤害或损失。
最新文档
- 辽宁科技大学《中外戏剧鉴赏》2023-2024学年第一学期期末试卷
- 昆明理工大学《五官科护理学》2023-2024学年第一学期期末试卷
- 江苏农林职业技术学院《金融建模与计算》2023-2024学年第一学期期末试卷
- 吉林工程职业学院《植物食品加工工艺学》2023-2024学年第一学期期末试卷
- 湖南女子学院《材料分析测试原理》2023-2024学年第一学期期末试卷
- 【物理】第十章 浮力 单元练习+-2024-2025学年人教版物理八年级下册
- 黑龙江能源职业学院《政治学导论》2023-2024学年第一学期期末试卷
- 高考物理总复习《电磁感应规律及应用》专项测试卷含答案
- 重庆五一职业技术学院《导航与制导系统》2023-2024学年第一学期期末试卷
- 重庆工贸职业技术学院《测绘学概论》2023-2024学年第一学期期末试卷
- 石油天然气建设工程交工技术文件编制规范(SYT68822023年)交工技术文件表格仪表自动化安装工程
- 患者跌倒坠床的应急预案试题及答案
- GB/T 24128-2018塑料塑料防霉剂的防霉效果评估
- 福建省地方标准《先张法预应力混凝土管桩基础技术规程》DBJ13-2023
- 危险作业监护人员培训
- 职业病防治企业台账样本
- 充电桩验收表
- 城市水环境新型污染物的去除新技术课件
- 中长期贷款按实际投向统计统计制度
- 锅炉专业2020年防非停措施
- 中国铁塔股份有限公司通信铁塔、机房施工及验收规范(试行)

评论
0/150
提交评论