



版权说明:本文档由用户提供并上传,收益归属内容提供方,若内容存在侵权,请进行举报或认领
文档简介
姓名:_________________学号:_________________班级:_________________学校:_________________ 密封线 姓名:_________________学号:_________________班级:_________________学校:_________________ 密封线 密封线 高考模拟化学期末试卷题号一二三四五六阅卷人总分得分注意事项:1.全卷采用机器阅卷,请考生注意书写规范;考试时间为120分钟。2.在作答前,考生请将自己的学校、姓名、班级、准考证号涂写在试卷和答题卡规定位置。
3.部分必须使用2B铅笔填涂;非选择题部分必须使用黑色签字笔书写,字体工整,笔迹清楚。
4.请按照题号在答题卡上与题目对应的答题区域内规范作答,超出答题区域书写的答案无效:在草稿纸、试卷上答题无效。A卷(第I卷)(满分:100分时间:120分钟)一、单选题(下列各题的四个选项中,只有一个是符合题意的答案。)
1、2021年,我国航空航天事业取得了辉煌成就。下列成就所涉及的材料为半导体材料的是A.“天问一号”探测器使用的复合材料—SiC增强铝基复合材料B.“天舟三号”货运飞船使用的质量轻强度高的材料——铝合金C.“长征五号”运载火箭使用的高效清洁的液体燃料——液氢D.“神舟十三号”载人飞船使用的太阳能电池材料——砷化镓
3、设为阿伏加德罗常数值。下列有关叙述正确的是A.18g的H2O中含有的中子数为10B.58.5g食盐中,含有NaCl分子数为C.标准状况下,11.2LCHCl3的原子数为2.5D.1molC2H6O中可能含有C-H键个数为6
4、Q、W、X、Y、Z为原子序数依次增大的短周期元素,Q的基态原子中只有1种运动状态的电子,W、Z的基态原子分别是同周期中未成对电子数最多的,X的基态原子2p能级上未成对电子数与成对电子数相同,Y与Q处于同一主族。下列说法正确的是A.简单离子半径:B.第一电离能:C.沸点:D.化合物中只含有离子键
5、下列说法中错误的是A.乳酸[]分子中存在2个手性碳原子B.酸性强弱:三氟乙酸>三氯乙酸>乙酸C.基态碳原子核外有三种能量不同的电子D.区分晶体和非晶体最可靠的科学方法是对固体进行X射线衍射实验
6、完成下列实验,所选装置正确的是(
)ABCD实验
目的实验室
制备乙烯分离苯和溴苯的混合物(沸点:苯为80.1℃,溴苯为156.2℃)分离KCl和NH4Cl固体混合物实验室用纯碱和稀硫酸制备二氧化碳实验
装置
A.AB.BC.CD.D
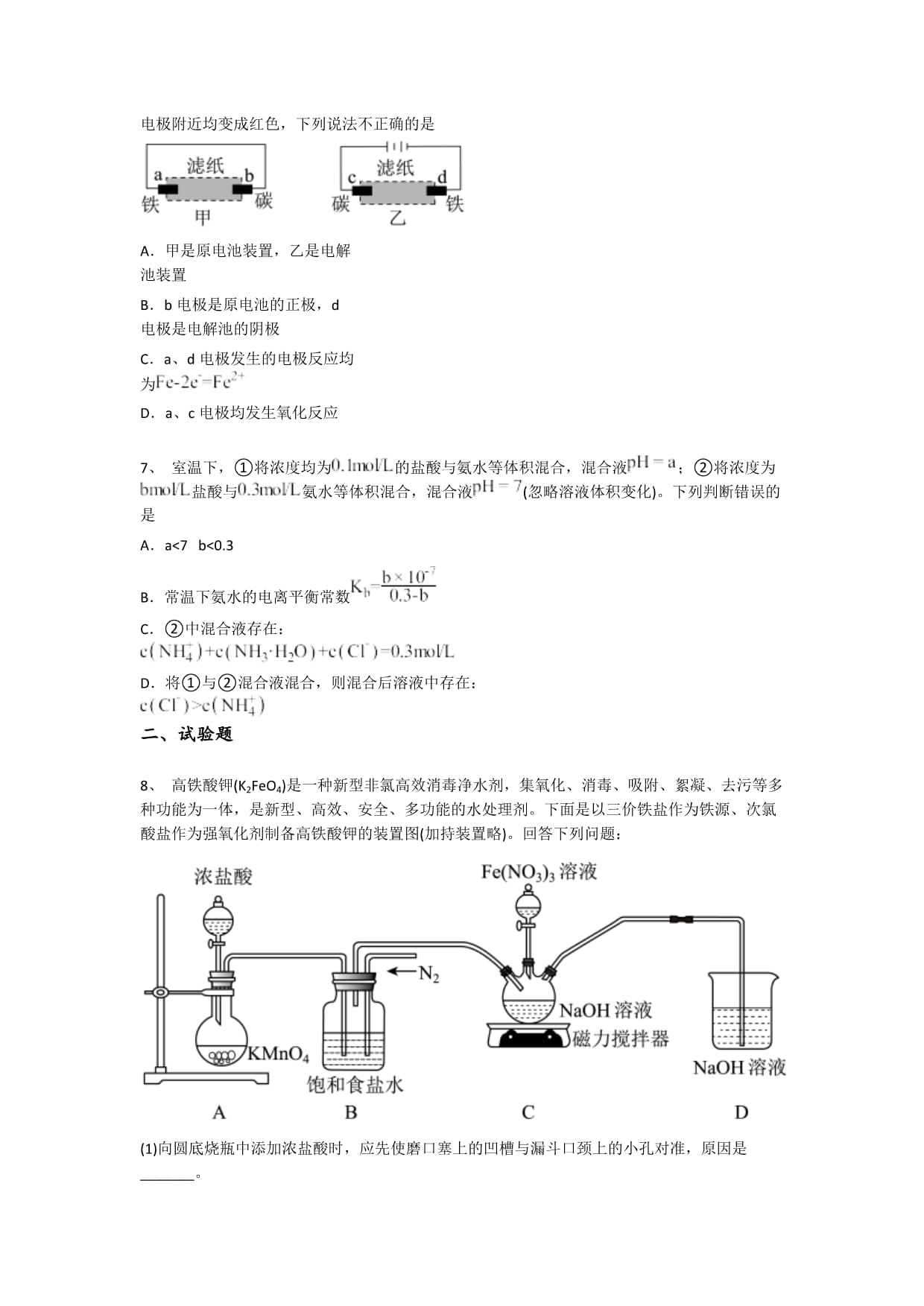
7、用滴有酚酞和氯化钠溶液的湿润滤纸分别做如图所示的甲、乙两个实验,结果发现b、d电极附近均变成红色,下列说法不正确的是
A.甲是原电池装置,乙是电解池装置B.b电极是原电池的正极,d电极是电解池的阴极C.a、d电极发生的电极反应均为D.a、c电极均发生氧化反应
7、室温下,①将浓度均为的盐酸与氨水等体积混合,混合液;②将浓度为盐酸与氨水等体积混合,混合液(忽略溶液体积变化)。下列判断错误的是A.a<7
b<0.3B.常温下氨水的电离平衡常数C.②中混合液存在:D.将①与②混合液混合,则混合后溶液中存在:二、试验题
8、高铁酸钾(K2FeO4)是一种新型非氯高效消毒净水剂,集氧化、消毒、吸附、絮凝、去污等多种功能为一体,是新型、高效、安全、多功能的水处理剂。下面是以三价铁盐作为铁源、次氯酸盐作为强氧化剂制备高铁酸钾的装置图(加持装置略)。回答下列问题:
(1)向圆底烧瓶中添加浓盐酸时,应先使磨口塞上的凹槽与漏斗口颈上的小孔对准,原因是_______。
(2)装置B既可以除去A中挥发出的HCl气体,又可以_______。
(3)实验结束时通入氮气的目的是_______。
(4)装置C中制备高铁酸钠发生反应的离子方程式为_______。
(5)低温下,在充分反应后的装置C反应液中加入KOH至饱和,可析出高铁酸钾粗产品,该反应的离子方程式为_______。粗产品中的可溶性杂质可通过_______方法进一步提纯。
(6)目前,利用氧化还原滴定原理测定高铁酸钾纯度,最为常见的方法是亚铬酸盐法:
准确称取ag高铁酸钾粗品配成V1mL溶液,取V2mL该待测液于锥形瓶中,加入浓碱性溶液和过量的三价铬盐。再加稀硫酸和指示剂二苯胺磺酸钠,用cmo1·L-1硫酸亚铁铵标准液滴定至溶液颜色由紫色变成浅绿色,即为终点,共消耗标准液V3mL(假设杂质不参与反应)。
①滴定时发生反应的离子方程式为_______。
②该粗品中高铁酸钾的质量分数为_______(用含字母的代数式表示)。
③若硫酸亚铁铵标准液放在空气中时间过长,则测得粗品中高铁酸钾质量分数_______(填“偏大”“偏小”“不变”)。三、工艺流程题
9、从铜电解液中分离得到的粗硫酸镍晶体中含有大量的杂质元素(Cu、Fe、As、Ca、Zn等),我国科学家对粗硫酸镍进行精制提纯,其工艺流程如下。
已知:i.含镍溶液中的主要离子有:Ni2+、SO、Cu2+、Fe2+、AsO、Ca2+和Zn2+
ii.饱和H2S溶液中,c(H2S)≈0.1mol/L
ⅲ.部分物质的电离常数和溶度积常数如下表物质电离常数物质溶度积常数物质溶度积常数H2SKa1=1.1×10−7
Ka2=1.3×10−13CuS6.3×10−36FeS6.3×10−18NiS3.2×10−19Ni(OH)25.5×10−16CaF24×10−11Fe(OH)32.8×10−39
(1)H2S是弱电解质,Ka1×Ka2=_______[用c(H2S)、c(H+)和c(S2−)表示]=1.43×10−20。
(2)滤渣1中含有As2S3和S,写出生成As2S3和S的离子方程式_______。
(3)解释“氧化除杂”中析出Fe(OH)3的原因_______。
(4)“氟化除杂”中试剂a为_______。
(5)“P204萃取”水溶液的pH约为3.3,结合下图解释原因_______。
(6)理论上“硫化除杂”之后,溶液中c(Cu2+)=_______mol/L[计算时c(H2S)取0.1mol/L,结果保留两位有效数字]。四、原理综合题
10、氯乙烯是制备塑料的重要中间体,可通过乙炔选择性催化加氢制备。已知:
I.
II.
III.
VI.部分化学键的键能如表所示。化学键C-CC=CC-HC-ClH-Cl键能(kJ/mol)347.7x413.4340.2431.8回答下列问题
(1)表中__________。
(2)在体积可变的密闭容器中以物质的量之比为1∶1充入和,分别在不同压强下发生反应,实验测得乙炔的平衡转化率与温度的关系如图所示。、、由大到小的顺序为__________。随温度升高,三条曲线逐渐趋于重合的原因为__________。
(3)—定温度下,向盛放催化剂的恒容密闭容器中以物质的量之比为1∶1充入和,假设只发生反应I和II。实验测得反应前容器内压强为,10min达到平衡时、的分压分别为、。
①0~10min内,HCl的总消耗速率__________Pa/min(用分压表示)。
②反应I的平衡常数__________(用含、、的代数式表示)。
(4)科学家发现反应I在催化剂Au/C作用下的反应历程如图所示。“2→3”的化学方程式可表示为:
①“4→5”的化学方程式为__________。
②反应物在催化剂表面经历过程“扩散→吸附(活性位点)→表面反应→脱附”。若保持体系中分压不变,HCl分压过高时反应催化效率降低的可能原因是__________。
11、氨基吡啶与铜等金属离子所形成的配合物具备良好的磁学性质,某氨基吡啶衍生物铜配合物X的结构简式如图所示。
(1)基态氯原子的价层电子排布图为______;下列不同状态的氮原子中,能量最高的是______(填字母)。
A.
B.
C.
D.
(2)C、N、O元素原子的电负性由大到小的顺序为______。
(3)X中的配位数是______;铜元素有不同价态氧化物,高温下稳定性______CuO(填“大于”或“小于”),从离子的电子层结构角度分析,主要原因是______。
(4)X中N原子的杂化方式为______。
(5)下列关于X的说法中不正确的是______(填字母)。A.存在大π键B.存在氢键、配位键等化学键C.碳、氧原子间形成的σ键和π键个数比为2∶1D.铜属于d区元素
12、以有机物A为原料合成药物F的路线如下:
回答下列问题:
(1)A分子中碳原子的杂化方式为___________,用*标记A分子中含有的手性碳原子:___________。
(2)试剂X的分子式为,写出试剂X的结构简式:___________,的反应类型为___________。
(3)反应中,每1molD参与反应,产生1molHBr,写出的反应的化学方程式:___________。
(4)在C的同分异构体中,同时满足下列条件的有___________种(不含立体异构),其中核磁共振氢谱显示有6组氢(氢原子数目比为)的结构简式为______
温馨提示
- 1. 本站所有资源如无特殊说明,都需要本地电脑安装OFFICE2007和PDF阅读器。图纸软件为CAD,CAXA,PROE,UG,SolidWorks等.压缩文件请下载最新的WinRAR软件解压。
- 2. 本站的文档不包含任何第三方提供的附件图纸等,如果需要附件,请联系上传者。文件的所有权益归上传用户所有。
- 3. 本站RAR压缩包中若带图纸,网页内容里面会有图纸预览,若没有图纸预览就没有图纸。
- 4. 未经权益所有人同意不得将文件中的内容挪作商业或盈利用途。
- 5. 人人文库网仅提供信息存储空间,仅对用户上传内容的表现方式做保护处理,对用户上传分享的文档内容本身不做任何修改或编辑,并不能对任何下载内容负责。
- 6. 下载文件中如有侵权或不适当内容,请与我们联系,我们立即纠正。
- 7. 本站不保证下载资源的准确性、安全性和完整性, 同时也不承担用户因使用这些下载资源对自己和他人造成任何形式的伤害或损失。
最新文档
- 2025至2030年防水粉碎机项目投资价值分析报告
- 泌尿外科肿瘤患者心理护理
- 2025至2030年铝玻璃丝包线项目投资价值分析报告
- 廉洁履职培训
- 银行培训总结演讲
- 2025至2030年药品原料项目投资价值分析报告
- 2025至2030年色校盆项目投资价值分析报告
- 骨科术后病人的护理措施
- 危险化学品生产单位特殊作业安全规范
- 背负式牧草收割机使用有什么优势呢
- 大小便观察与护理
- 2025年-重庆市安全员-A证考试题库附答案
- 湖北省孝感市高新区2023-2024学年七年级下学期数学期中考试试卷(含答案)
- 8.2 诚信经营 依法纳税课件-高中政治统编版选择性必修二法律与生活
- 领导带班及24小时值班制度
- 具身智能机器人扩散策略Diffusion Policy环境安装与运行
- 湖北省武汉市2024-2025学年高三2月调研考试英语试题含答案
- 小学英语国测试卷
- 安徽省涡阳县高炉小学-春暖花已开一起向未来-二年级下册开学家长会【课件】
- 核电站设备采购合同
- 《OCR技术及其应用》课件

评论
0/150
提交评论