



版权说明:本文档由用户提供并上传,收益归属内容提供方,若内容存在侵权,请进行举报或认领
文档简介
第三章
物質的形成及變化壹、原子的結構一、1808年,道耳吞提出原子說:物質均由原子所組成,原子是不可分割。
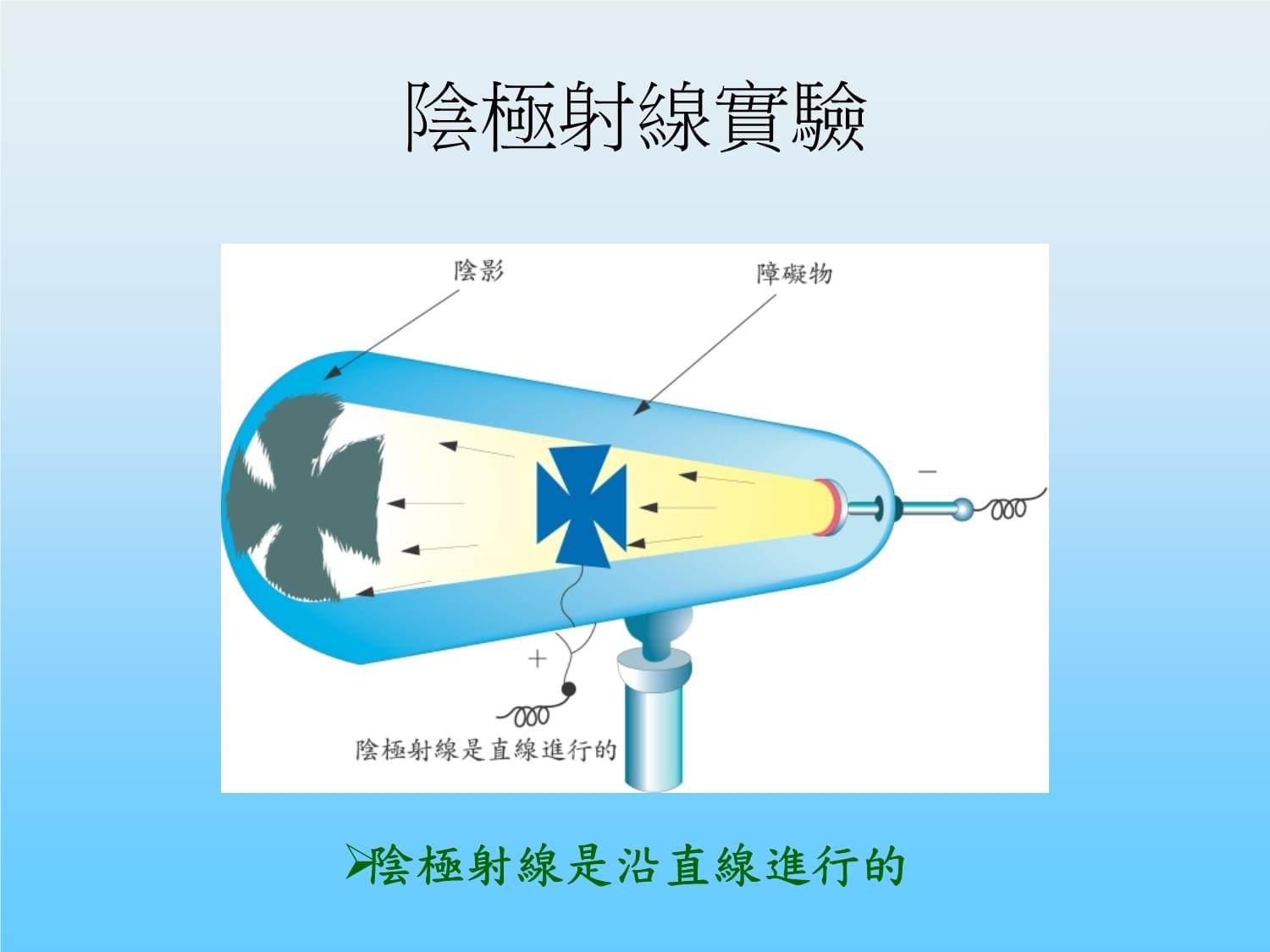
二、電子的發現1895年,湯木生對由陰極射線實驗中發現:(1)底片上有陰影。(2)使轉輪轉動(具粒子性)。(3)加電場,偏向正極(具負電性)。(4)加磁場,會偏轉;推導出荷質比
(e/m)。(5)將此陰極射線之粒子稱為
。電子陰極射線實驗陰極射線是沿直線進行的陰極射線實驗陰極射線是具有質量的粒子陰極射線實驗陰極射線為帶負電之粒子可利用此裝置測出陰極射線的電荷與質量之比2.1909年,米力坎經四年努力,以油滴實驗得到電子電荷是
湯木生對由陰極射線實驗+米力坎油滴實驗推導得電子的質量為
。解:
三、原子的模型1.1898年,湯木生首先提出原子模型(西瓜模型、梅子布丁、葡萄乾土司)2.拉塞福α粒子(氦原子核)散射實驗:
(1)α粒子大部分穿透金箔
原子大部分是空的,電子活動空間(電子占大部分體積)
(2)少部分大角度反彈
原子核帶正電,原子質量集中於原子核
10-15m1Å=10-10m原子核=半徑1cm小球原子=半徑1km小球例:質子數=
11
;中子數=
12
;電子數=
11
。質子數=
17
;中子數=
18
;電子數=
18
。
Z=原子序=質子數=電子數(對電中性原子)A=質量數=質子數+中子數四、質子的發現:拉塞福α粒子撞擊氮原子核五、中子的發現:查兌克α粒子撞擊鈹原子核核反應:1.原子序守恆
2.質量數守恆
3.質能守恆E=mC2E:能量(Joule)
m:質量(kg)
C:光速
例:核反應前後損失1克質量,會釋放出多少能量?
六、電子的排列規則:第一層最多2個,第二層最多8個,第三層最多8個。貳、物質的形成—化學鍵結
一、離子鍵
(例)1.金屬元素+非金屬元素(銨根離子)(、OH-、、…)2.離子晶體,例:MgCl2、NH4Cl3.高熔點、高沸點4.以簡式表達5.無方向性6.一敲就碎(無延展性)NaClNaCl-離子鍵氯化鈉晶體結構二、共價鍵(共用價電子形成鍵結)例:H+ClH-Cl1.非金屬元素+非金屬元素2.以分子式表達3.分子化合物(共價化合物)4.熔、沸點低HClHCl共價鍵孤對電子(lonepairelectron)
L.P.三、金屬鍵(以陽離為骨架,浸在電子海中)1.有自由移動電子,導電性良好2.金屬在固態、液態下皆可導電鈉金屬的自由電子金屬的延展性參、
物質的質量一、1961年國際純粹及應用化學聯合會以12C=12.0000為標準。
1mol12C=12克;一個12C=12amu
(atomicmassunit)二、平均原子量例:自然界含有35Cl(75%)及37Cl(25%),已知35Cl及37Cl之原子量分別為35及37,則氯的原子量為多少?答:例:自然界中硼有兩種同位素(即B,B),已知10B及11B之原子量分別為10及11,又知硼之平均原子量為10.8,則此兩種同位素的含量比值(:)是多少?答:設的含量為x;的含量為1-x10x+11(1-x)=10.8x=0.2----10B
則1-x=0.8----11B
:=1:4三、分子量:原子量的總和例:CO2=
;
H2O=
。四、莫耳(mol)計算莫耳數
=例:等重的下列各氣體,何者所含的原子數最多?
(A)C2H4
(B)CH4
(C)CO2
(D)N2
4418例:46克C2H5OH含有
2
molC原子,
個氧原子,
6
克氫原子。
五、補充
1atm、0℃(STP,StandardTemperatureandPressure)
1mol氣體體積為22.4升1atm、25℃(NTP,NormalTemperatureandPressure)
1mol氣體體積為24.5升
例:16克CH4完全燃燒,在STP情況下,產生CO2幾升?暗示:
CH4消耗1莫耳,產生CO21莫耳,在STP下,相當於是22.4升肆、物質在溶液中的性質
一、阿瑞尼士之解離說:物質溶於水會解離成陰、陽離子,陽離子游向負極,陰離子游向正極,形成電的通路二、電解質:物質溶於水,因解離而導電的物質。例:酸、鹼、鹽三、導電
固態
金屬、石墨液態
金屬、離子化合物液態
電解質例:(1)下列何者可導電?(2)何者是電解質?(A)Cu(s)(B)NaCl(l)(C)HCl(aq)
(D)H2SO4(l)(E)C2H5OH(aq)(F)KNO3(s)
(A)(B)(C)(B)(C)(D)(F)伍、物質的變化一、沈澱反應1.產生沉澱原因:溶解度低2.Cl-與Ag+、Pb2+、Cu+、Hg22+、Tl+沉澱
SO42-與Sr2+、Ba2+、Pb2+沉澱
NH4+、IA+不沉澱;NO3-、CH3COO-不沈澱
3.常見沈澱反應(1)淨離子反應方程式(2)淨離子反應方程式(黃色)
白色二、酸鹼中和酸:〔H+〕>〔OH-〕鹼:〔H+〕<〔OH-〕酸鹼中和:
淨離子反應方程式(只有強酸+強鹼)
三、氧化還原反應氧化
還原
1.與氧化合
1.失去氧
2.失去電子NaNa++e-2.獲得電子Cl+e-
Cl-例:鋅-銅電池
氧化半反應還原半反應例:電解反應,陽極進行氧化反應,陰極進行還原反應
被電解物質CuBr2(aq)H2O陰極(還原)陽極(氧化)
温馨提示
- 1. 本站所有资源如无特殊说明,都需要本地电脑安装OFFICE2007和PDF阅读器。图纸软件为CAD,CAXA,PROE,UG,SolidWorks等.压缩文件请下载最新的WinRAR软件解压。
- 2. 本站的文档不包含任何第三方提供的附件图纸等,如果需要附件,请联系上传者。文件的所有权益归上传用户所有。
- 3. 本站RAR压缩包中若带图纸,网页内容里面会有图纸预览,若没有图纸预览就没有图纸。
- 4. 未经权益所有人同意不得将文件中的内容挪作商业或盈利用途。
- 5. 人人文库网仅提供信息存储空间,仅对用户上传内容的表现方式做保护处理,对用户上传分享的文档内容本身不做任何修改或编辑,并不能对任何下载内容负责。
- 6. 下载文件中如有侵权或不适当内容,请与我们联系,我们立即纠正。
- 7. 本站不保证下载资源的准确性、安全性和完整性, 同时也不承担用户因使用这些下载资源对自己和他人造成任何形式的伤害或损失。
最新文档
- 2025届陕西省西安市一中学高三第二次联考(二模)英语试题含解析
- 安庆市枞阳县2025届三下数学期末统考试题含解析
- 2024-2025学年陕西省西安电子科技大附中高三年级下学期4月月考历史试题试卷含解析
- 明溪县2025年四下数学期末质量跟踪监视试题含解析
- 2025年江西省上饶市余干二中学初三4月仿真模拟(六)物理试题试卷含解析
- 中国诗词大会模拟试题200道
- 浙江大学2024文学理论及作业答案
- 招聘与面试案例大
- 食品质检员在企业中的作用分析试题及答案
- 防恐培训课件
- 快餐店创业计划书
- 2025年辅警招聘考试试题库及答案(全优)
- 【初中地理】西亚课件-2024-2025学年人教版(2024)七年级地理下册
- 2024年4月27日福建省事业单位《综合基础知识》真题及答案
- (一模)2025年广东省高三高考模拟测试 (一) 英语试卷(含官方答案及详解)
- 退役军人无人机培训宣传
- 退役军人保密教育
- 《园林微景观设计与制作》课件-项目二 作品展示
- 本科毕业论文完整范文(满足查重要求)城市社区网格化治理问题研究
- 2025年旅游专业面试试题及答案
- 液压升降平台施工方案

评论
0/150
提交评论