



版权说明:本文档由用户提供并上传,收益归属内容提供方,若内容存在侵权,请进行举报或认领
文档简介
1、教学目标:掌握卤代烷的消除反应机理、立体化学、反应取向及影响因素。教学重点:消除反应机理,反应取向Saytzeff规则。 教学安排: H , H , H H ;40min3 4 5 6卤代烷不仅能发生 S 反应,还可以发生消除反应。卤代烷分子中消去卤化氢生成烯烃常N称为消除反应(Elimination)用E表示。由于卤代烷中C-X键有极性,卤素的诱导作用 可通过a碳传递到卩碳上,致使卩-H原子有一定的“酸性”;在碱的作用下卤代烷易于消 去卩-H和卤原子,称为卩-消除;这种消除反应是烯烃的一种制备方法。如:CF43(CH2)9CH=CHCF43(CH2)9CH=CH2CH3(CH2)9CH2CH
2、2Br 也口曲鮎卜与卤代烷的 S 反应相似,卤代烷在发生消除反应时,也有双分子和单分子消除机理,分N别记为 E2 和 E1。一双分子消除反应(E2)1E2 反应机理在卤代烷的双分子消除反应机理中,反应是一步完成的,其反应速率与反应物和亲核试剂 的浓度成正比,故称为双分子消除反应机理。记为E2。反应的动力学方程为:险去=kf 在反应过程中,碱对卤代烷的卩-H进攻,同时C-X键开始发生异裂,在达到过渡态时,C-H 键和 C-H 键都达到了高度的异裂活化状态,此时 C-C 之间已有了部分双键的性 pap a质,这两个而原子已有部分SP2杂化的特性。这时反应体系处于最高能量水平,随着反应的 时行, p
3、-H 完全成碱结合,卤负离子彻底离去,最终生成了烯烃。0H* ch0H* ch3-ch=ch2 + h2o + X-2立体化学实验表明,在按E2机理进行的消除反应中,一般发生反式消除即卤原子与P-H在O键 的两侧(异侧)被消除。p-H 与 X p-H 与 X 处于反式共平面能量低:例:例:二单分子消除反应(E1)E1 反应与 S 1 反应有相似的机理,反应也是分两步进行。首先卤代烷在碱性水溶液中解 N离为碳正离子,随后OH若进攻碳正离子的中心碳原子,则生成取代产物;若进攻卩-氢 原子则发生消除反应生成烯烃。两者也是相伴而生E1消除反应的机理可表示如下(以叔 丁基卤为例):(tw 3C-X -(
4、CHQ+ :X-或一-(CHs) 或一-(CHs) 2C=CH + H2O第一步是慢步骤,第二步是快的,即反应速度取决于卤代烷的浓度,反应的动力学方程为 u=kRX ,故这种反应机理称为单分子消除反应机理。与 S 1 反应相似, E1 反应也常常发生重排反应,例如:N(驰:sCCHsEr卫空(CH:)乳缶汁W+亠CHC-dhCHs-Cj-CHsCft *伽)UCH-CHa + H三.消除反应的取向当卤代烷含有两个或两个以上不同的卩-氢原子可供消除时,究竟哪一个氢原子被消除 呢?这就是取向问题。实验证明,卤代烷脱卤化氢时,氢原子主要从含氢较小的相邻碳原子(卩-碳原子)上脱去。换言之,主要生成双键
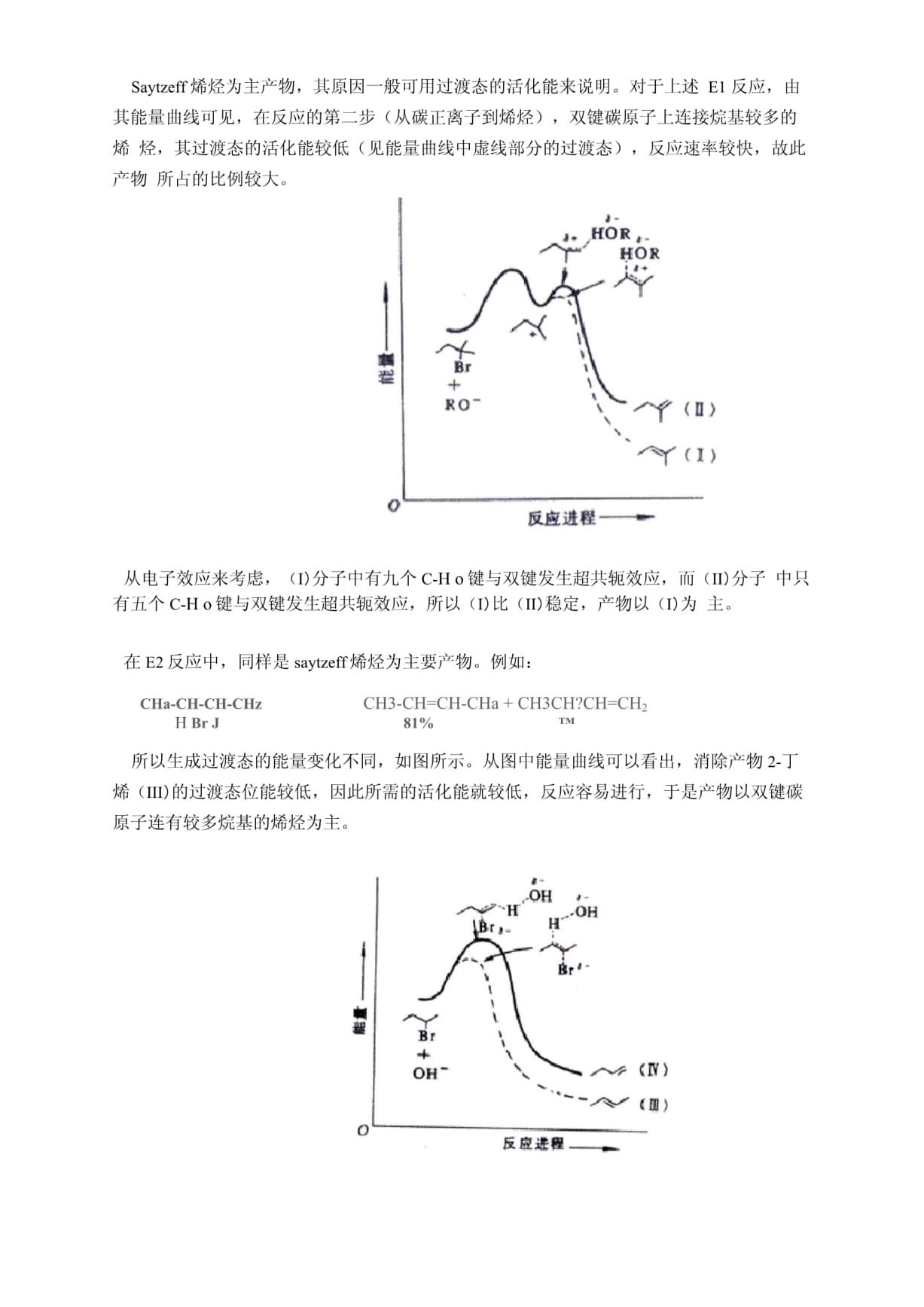
5、碳原子上连有较多取代基的烯烃。这是一条 经验规律,称为 Saytzeff 规则,这种消除取向称为 Saytzeff 取向。反之,生成双键碳原子 上连有较少取代基的烯烃,则为 Hofmann 取向。例如:Saytzeff 烯烃为主产物,其原因一般可用过渡态的活化能来说明。对于上述 E1 反应,由 其能量曲线可见,在反应的第二步(从碳正离子到烯烃),双键碳原子上连接烷基较多的烯 烃,其过渡态的活化能较低(见能量曲线中虚线部分的过渡态),反应速率较快,故此产物 所占的比例较大。从电子效应来考虑,(I)分子中有九个C-H o键与双键发生超共轭效应,而(II)分子 中只有五个C-H o键与双键发生超共轭
6、效应,所以(I)比(II)稳定,产物以(I)为 主。在E2反应中,同样是saytzeff烯烃为主要产物。例如:CHa-CH-CH-CHzCH3-CH=CH-CHa + CH3CH?CH=CH2H Br J81%所以生成过渡态的能量变化不同,如图所示。从图中能量曲线可以看出,消除产物2-丁 烯(III)的过渡态位能较低,因此所需的活化能就较低,反应容易进行,于是产物以双键碳 原子连有较多烷基的烯烃为主。另外,也可以用超共轭效应来解释。在(III)分子中,有六个C-H o键与双键发生超共 轭效应,而在(W)分子中,仅有两个C-H o键与双键发生超共轭效应,因此(III)比(W) 稳定,产物以(II
7、I)为主。如果脱去卩-H所处位置有明显的空间位阻或碱的体积很大,不利于处在中间位置的卩-H脱去,则以处于一端的卩-H的脱去较为有利,这就生成了了 Hofmann取向为主的端烯烃:CH3CH2CHCH3-JBr心 “ CH3CH CHCHs + CTHsCHMHMHd 叫 ACH3CH2CHCH3-JBr粘熾=CH3CH=CHCH3 + C 阳CHzCH 二 CHr(47%)(53%)佻CHC1。出BrCCH3h洛需 * CH丈H2CH2CH2CHHH2 + CH3CH2CH2CH=CHCH3(33%)(67%)(JHsCHiCHiCHsCH-CHs + CHgCHaCHCHCHj(91%)(9
8、%)CH3 (CH5)3CCH = C(CH3)2 + (CH3)3CCH26 = CH2(14%)(86ft)霭c肘 sCCH = C (CH3 i + (CHs) 3CCH?C =CHsCHa(2ft)(98%)_KOCjHs_EOCzH, i四.影响消除反应的活性1 烷基的结构不同结构的卤代烷发生消除反应( E1 和 E2 )的活性一般为: 3RX2RX1RX 因为对于 E1 反应机理,第一步 R+ 的形成为决定反应速度的步骤, R+ 越稳定,越易形 成,其R+稳定性为3R+2R+1R+。对于E2反应机理,因为强碱是与卩-H相结合的, 它不攻击a-C。为存在SN2机理中的那种空间位阻,所
9、以当a-C上有连有较多的支链烷基 时,对 E2 反应反而是有利的。这是因为多个支链烷基的存在对部分双键的形成有推动作 用,不仅可以降低过渡态的热力学能,还会使生成的烯烃获得最大程度的稳定。2碱的浓度碱的浓度大,碱性强,有利于碱对卤代烷的卩-H进攻,容易发生消除反应。 3离去基团离去基团越容易离去,越容易进行消除反应。4 溶剂的极性溶剂的极性增加,不利于消除反应。极性溶剂对强碱的溶剂化作用会降低碱的强度使之与 卩-H的反应能力下降。另外,极性强不利于过渡态时负电荷的分散。E2反应中过渡态化学 键的变化涉及了五个原子,负电荷更加分散,因此对E2反应更不利。E1、E2 消除反应比较E1E2反应机理11慢丨丨H C C L .H-C-C* + L-H f f土 -HB+C=C + L-一步动力学Hci -C-L1一级反应(单分子)
温馨提示
- 1. 本站所有资源如无特殊说明,都需要本地电脑安装OFFICE2007和PDF阅读器。图纸软件为CAD,CAXA,PROE,UG,SolidWorks等.压缩文件请下载最新的WinRAR软件解压。
- 2. 本站的文档不包含任何第三方提供的附件图纸等,如果需要附件,请联系上传者。文件的所有权益归上传用户所有。
- 3. 本站RAR压缩包中若带图纸,网页内容里面会有图纸预览,若没有图纸预览就没有图纸。
- 4. 未经权益所有人同意不得将文件中的内容挪作商业或盈利用途。
- 5. 人人文库网仅提供信息存储空间,仅对用户上传内容的表现方式做保护处理,对用户上传分享的文档内容本身不做任何修改或编辑,并不能对任何下载内容负责。
- 6. 下载文件中如有侵权或不适当内容,请与我们联系,我们立即纠正。
- 7. 本站不保证下载资源的准确性、安全性和完整性, 同时也不承担用户因使用这些下载资源对自己和他人造成任何形式的伤害或损失。
最新文档
- 改革开放史培训
- 小细胞低色素性贫血的健康宣教
- 安全标志使用培训
- 自然材料生成课件
- 肠内营养的观察及护理
- 视网膜静脉阻塞的健康宣教
- 心源性胸痛的健康宣教
- 广西壮族自治区南宁市马山县重点中学2024届中考适应性考试数学试题含解析
- 2025合作协议书模板:广告制作合作合同
- 皮肤白血病的健康宣教
- 消防更换设备方案范本
- 2024年环境影响评估试题及答案
- 【初中历史】2024-2025学年部编版七年级下学期历史中考复习提纲
- 象棋-小学社团活动记录表
- 边坡坡度测量记录表
- 中职 AutoCAD 2018计算机辅助设计项目化教程课程标准
- 功能医学与健康管理
- HZS75型搅拌站安装施工方法
- DB13(J)∕T 8377-2020 建筑施工安全管理标准
- 吊装施工施工组织设计
- 2019人教版高中英语选择性必修三单词表

评论
0/150
提交评论