



版权说明:本文档由用户提供并上传,收益归属内容提供方,若内容存在侵权,请进行举报或认领
文档简介
1、 2015-2016 学年度苏锡常镇四市高三教学情况调研(二) 化 学 本试卷分第I卷(选择题)和第n卷(非选择题)两部分。满分 120 分,考试时间 100 分钟。 可能用到的相对原子质量: H 1 C12 N14 O16 Na 23 Mg- 24 Al 27 S 32 K 39 Ca- 40 M - 55 Fe 56 C - 64 第I卷(选择题共 40 分) 单项选择题:本题包括 10 小题,每小题 2 分,共 20 分。每小题只有一个选项符合题意。 1. 化学与生活、生产密切相关。下列叙述错误的是 ( ) A. 过氧化钠可用作呼吸面具中的供氧剂 B. 向海水中加净水剂明矶可使海水淡化
2、C. 使用含有氯化钙的融雪剂会加速桥梁的腐蚀 D. 服用抗氧剂维生素 C 有利于人体对铁元素的吸收 2. 下列有关卤族元素及其化合物的表示正确的是 ( ) A. 氟离子的结构示意图: B.次氯酸的结构式:H Cl O H: C.溴化铵的电子式: D.质子数为 53,中子数为 78 的碘原子:1531I 3. 下列物质的性质与应用对应关系错误的是 ( ) A. 二氧化氯具有强氧化性,可用于杀菌消毒 B. 氢氧化铝具有弱碱性,可用于治疗胃酸过多 C. 二氧化硅的熔沸点很高,可用于制作石英坩埚 D钠钾合金的密度小,可用于快中子反应堆的热交换剂 4. 下列实验现象可用同一原理解释的是 ( ) A. 向
3、品红溶液中分别通入 SQ 和 Cl2,品红均褪色 B. 向裂化汽油和苯乙烯中分别加入溴水,溴水均褪色 C. 分别加热盛有氯化铵和单质碘的试管,内壁或管口均有固体凝结 D. 分别向鸡蛋白溶液中加入饱和硫酸铵溶液和甲醛溶液,均有固体析出 5. X、Y Z、W 都是周期表中前 20 号元素。Y、W 同周期,Z、W 同主族;X2+与具有相同的电 子层结构,Z 中核外电子数是 W 中核内质子数的 2 倍;Y的同素异形体之一是地球上天然存在的硬度 最大的物质。下列叙述正确的是 ( ) A. 原子半径大小顺序: XZWY B.氢化物的沸点高低顺序: ZW C.元素非金属性强弱顺序:WZY D.化合物 XW
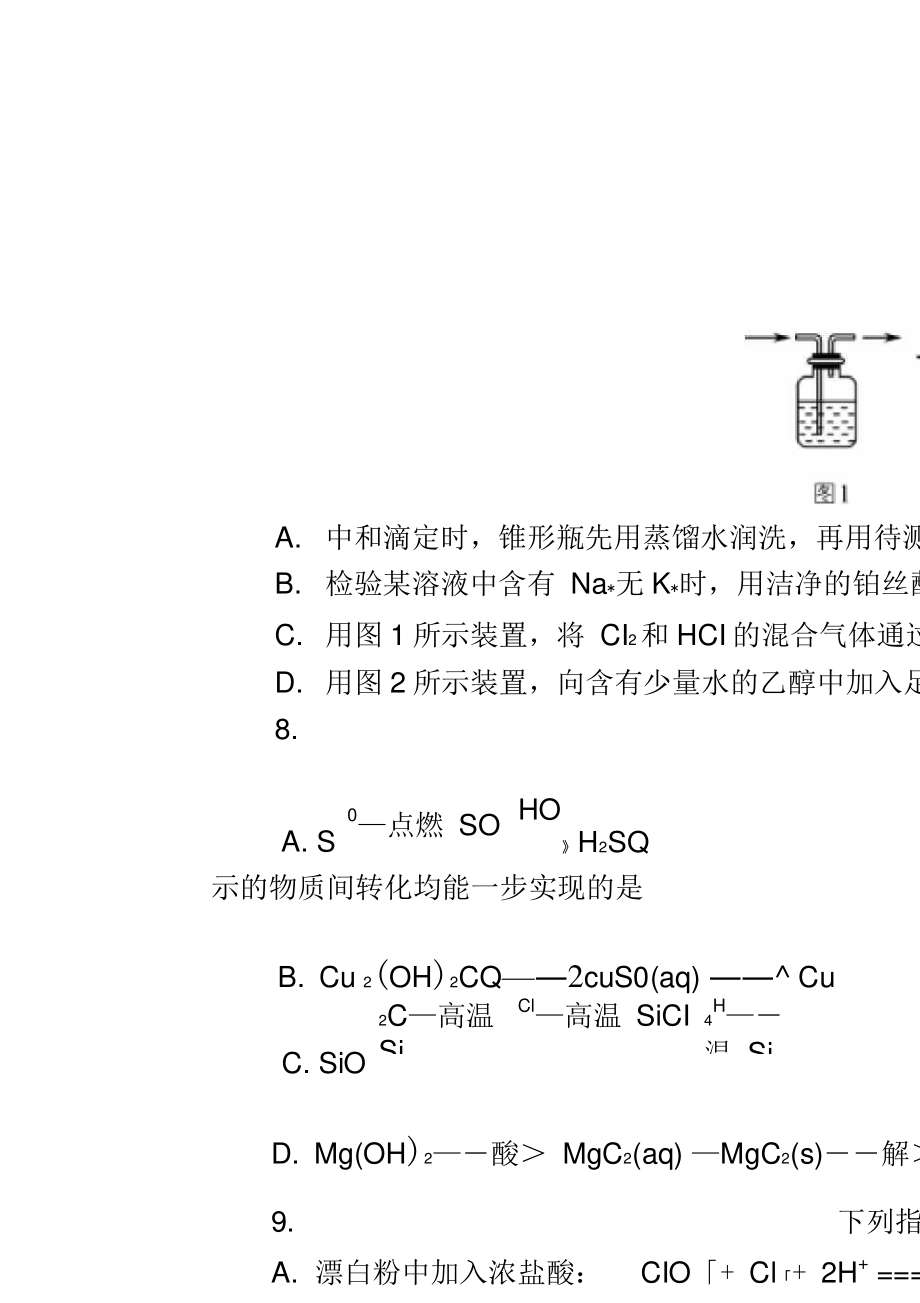
4、与 XW 中化学键类型完全相同 6. 常温下,下列各组离子一定能在指定溶液中大量共存的是 ( ) A. c(l )= 0.1 mol L1 的溶液中:Na*、M + CIO、sO B. 使甲基橙变红色的溶液中: K、NH HCO、C BrBr * -J H 2 C. 与 Al 反应能放出大量 H2的溶液中:Fe2*、Na+ NQ、C D. 由水电离产生的 c(OH ) = 1X10 mol L 的溶液中:Ba、K、NQ、Br 7. 下列实验操作正确的是( )3 A. 中和滴定时,锥形瓶先用蒸馏水润洗,再用待测液润洗 B. 检验某溶液中含有 Na*无 K*时,用洁净的铂丝蘸取该溶液,灼烧,观察火
5、焰颜色 C. 用图 1 所示装置,将 CI2和 HCI的混合气体通过饱和 NHCG 溶液,除去 Cl 2中 HCI D. 用图 2 所示装置,向含有少量水的乙醇中加入足量生石灰,蒸馏,得到无水乙醇 8. 在给定条件下,下列选项中所示的物质间转化均能一步实现的是 ( ) B. Cu 2(OH)2CQ2cuS0(aq) Cu D. Mg(OH)2酸 MgC2(aq) MgC2(s)解Mg 9. 下列指定反应的离子方程式正确的是 ( ) A. 漂白粉中加入浓盐酸: CIO+ Cl+ 2H+ =Cbf + H2O B. 氯化铁溶液洗涤银镜: Fe3 + + Ag=Fd+ + Ag+ C. 0.1 mo
6、l LTNHHSQ 溶液和 0.1 mol L 一 1NaOH 等体积混合: NH* + H+ + 2OH =NH H2O+ HaO D. 0.1 moI Lt 的 NaAIQ 溶液和 0.15 moI L -1的 HSO 溶液等体积混合: AIO2 + 4H+= AI + 2fO 10. 硼氢化钠(NaBH4)和 HC2作原料的燃料电池,负极材料采用 Pt/C,正极材料采用 MnO,其工 作原理如图。下列说法正确的是 ( ) A. 电极 a 为正极,b 为负极 B. 放电时,Na*从 b 极区移向 a 极区 C. 电极 b 上发生的电极反应为 H2O* 2e=2OH D. 每生成 1 moI
7、 BO 转移 6 moI电子 不定项选择题:本题包括 5 小题,每小题 4 分,共 20 分。每小题只有一个或两个选项符合题意。 若正确答案只包括一个选项,多选时,该题得 0 分;若正确答案包括两个选项,只选一个且正确的 得 2 分,选两个且都正确的得满分,但只要选错一个,该小题就得 0 分。 11. 下列说法正确的是( ) A. S 0点燃 SO HO H2SQ C. SiO 2C高温 Si Cl高温 SiCI 4H温 Si 水 4 A. 钢铁的电化学腐蚀和化学腐蚀往往同时发生 B. 反应 C(s) + H2O(g)=CO(g) + H2(g)的 S0 H0 C. 常温下,pH 为 5 的氯
8、化铵溶液和 pH 为 9 的醋酸钠溶液中水的电离程度相同5 D.向 BaSO 沉淀中加入饱和 NaCO 溶液后生成 BaCO,贝U Ksp(BaCQ)c(HA _)c(H + )c(A 2_)c(OH _) D. V(NaOH) = 30 mL 时,溶液中存在如下关系: 2c(H +) 2c(OH_) = c(A2_) 3c(HA) c(HA_) 15. 在体积为 V L 的恒容密闭容器中加入 6 mol CO 和 H 的混合气体,在不同条件下发生反应: CO(g) + 2f(g) CHOH(g)。图 1 表示有、无催化剂时反应的能量变化,图 2 表示平衡时 CHOH 的体积分数随起始 n(C
9、O) : n(H2)的变化关系。下列叙述正确的是 ( )13. A. 下列设计的实验方案能达到实验目的的是 制备 Fe(OH)2:用图 1 所示装置,向试管中加入 测定 H2的生成速率:用图 2 所示装置,制取一定体积的 除去苯中少量苯酚:向苯和苯酚的混合液中 检验淀粉是否水解:取 ) NaOH 溶液,振荡 H2,记录时间 加入浓溴水,过滤 0.5 g 淀粉于洁净的试管中,先加入 5 mL 稀硫酸,水浴加热,一段 6 B. 正反应速率 v正:v正(状态n ) v正(状态川) C. 平衡时 co 的转化率:a (CO,状态I ) a (CO,状态n) D. n (CO): n(H2) = 0.5
10、 时,平衡时 CHOH 的物质的量浓度: c(CHsOH 1 00 C )c(CH 3OH 200 C ) 第n卷(非选择题共 80 分) 16. (12 分)锰酸锂(LiMn 2O)是新一代锂离子电池的正极材料。实验室回收利用废旧锂离子电池 正极材料(锰酸锂、碳粉等涂覆在铝箔上 )的一种流程如下: XaOH溶液 匚十 聶器器豊耆料一碱溶一过滤 1 反应过滤沉淀 X _ 1 Liggq Na;CO3 稀H紊二履落IT过滤IT反应H过滤I 2 4 Hr nn MnO-tLiCO (1) _ X 的化学式为 。 (2) _ 写出“酸溶”过程中反应的离子方程式: 。 (3) _ 反应中与 N&
11、;CO 反应的物质有 和 (填化学式);工业上洗涤 LizCO 用的 是热水而不是冷水,其原因是 _ 。 (4) 固相法制备 LiM nzQ的实验过程如下:将 MnO 和 LizCO 按 4:1的物质的量之比配料,球磨 35 小时,然后升温,高温加热,保温 24 小时,冷却至室温。 写出该反应的化学方程式: _ 。 LiMn 2O4中锰元素的平均价态为+ 3.5。在不同温度下,合成的 LiMnzQ中 MrT、M+和 MrT 的 含量与温度的关系见下表。 T/ C w(M n*)(%) w(M n*)(%) w(M n*)(%) 700 5.56 44.58 49.86 750 2.56 44.
12、87 52.57 800 5.50 44.17 50.33 850 6.22 44.40 49.38 能量炉 mol1) F1 510 +2molH! lmulCH,OH(g) 反应过甩 图 1 1 H= 91 kJ mol ,曲线 b A.正反应的 7 由此可以确定:在上述温度范围内,锰元素的平均价态的变化趋势是 17. (15 分)化合物 G 是一种抗精神病药物,可以通过下列方法合成:8 (2) E TF的反应类型是 _ 。 Y 的分子式为 CoHNzCI,则 Y 的结构简式为 _ 。 (4)写出同时满足下列条件的 C 的一种同分异构体的结构简式: _ 。 苯环上有两个取代基; 核磁共振氢
13、谱图中有 7 个峰; 能发生水解反 应,产物之一是氨基乙酸,另一种产物能与 FeCl3溶液发生显色反应。 化合物 Z( . )是合成一种新型口服强心药的中间体,请写出以 CICH2CHCOC、CICH2COC 为原料制备 Z 的合成路线流程图(无机试剂可任选)。 合成路线流程图示例如下: Q CHCHOH CHCHOi 化剂, CHCOO 浓硫酸CHC CCH 18. (12 分)三草酸合铁酸钾晶体是一种光敏材料,可以通过下列流程来制备: (1) _ ;设计步骤 AB的目的是 已知: * 丿 A1C1? RTC1 A1C1 0 匚易氧化,酰胺键(一XH)难以被H: 还原匸 F R 9 “过滤”
14、前加入 H2C2O4的目的是将 Fe*转化为 FeC2O4 2fO 沉淀;“氧化”时加入 H2GO 的目的是: 参与“氧化”时的反应, _ 。 (2) “氧化”过程中反应的化学方程式为 _ 。 (3) 称取 9.82 g K3Fe(C2O)3 3H2O 固体加热分解,在 110 C时完全失去结晶水;继续加热到 一定温度,反应一段时间后得到混合气体 CO CQ(标准状况下的体积为 2.016 L)和固体 M。研究分 析可知:M 中含有 K2CQ 和另外两种物质(铁元素不以三价形式存在 );M 的质量为 5.42 g 。 CQ 的物质的量为 _ 。 计算 M 中各成分的物质的量(写出计算过程)。
15、19. (15 分)焦亚硫酸钠(Na2S2Q)是一种食品添加剂。 实验室用下图所示装置制备 NazQQ,实验 步骤如下: 利用 N2SQb和 FeSQ PHQ 先后分两个阶段处理含0-8765432 可一 5.5 5.0 丄5 4,0 二送 3.0 2.5 2.0 20 40 W* SO 100 120 反应时间Anin (4)含铬废水中常含有六价铬Cr( W)。 10 的废水,实验结果见右图。 实验过程中溶液的 pH 不断升高的原因是 _ 。 已知:KSpCr(OH) 3 = 6.4 X 10 一31, lg2 0.3 , c(Cr3+)”“ 5.6(2 分) 20. (14 分) (1)
16、bcd(2 分,全对给 2 分,选 2 个且正确给 1 分,选 1 个或有错选不给分) =(2 分) (2) 1 079.7(2 分) 2NH3+ CIO_=CI_+ INH+ HO(2 分) (3) NO+ 5e_ + 6=NH+ 0(2 分) 1 : 4(2 分) (4) 氯胺与水反应存在平衡: NHCI + H2O NH+ HCIO,酸性条件下平衡右移使次氯酸浓度 变大(2 分) 21A. (12 分) 23 (1) 7 mol 或 7X 6.02 x 10 (2 分) SO(或 BR)(2 分) (2) 1 : 1(2 分)Cu失去一个电子时,核外电子排布从Ar3d 104s1变为Ar
17、3d 10能量较低的稳定 结构较容易;Zn失去一个电子时,核外电子排布从 Ar3d 104s2变为Ar3d 104s1较难(2 分) (3) sp 2、sp3(2 分)bcd(2 分,全对给 2 分,选 2 个且正确给 1 分,选 1 个或有错选不给分) 21B. (12 分) (1) 冷凝回流(1 分) (2) 反应物受热均匀,便于控制温度 (1 分) (3) 减少对氨基苯磺酸的损失(2 分) (4) 拆下连接泵和吸滤瓶的橡皮管 (2 分)关闭水龙头(2 分) (5) 提高对氨基苯磺酸的纯度(2 分)提高对氨基苯磺酸的产率(2 分)I .在NQCO溶液中通入 SQ 至 pH 为 4.1,生成 NaHSO 溶液; n .加碳酸钠粉末调至 pH 为 78; 川.再通 SQ 至 pH 为 4.1 ; IV .从过饱和溶液中析出 NstSQ 晶体。 16 (1) 制备焦亚硫酸钠总反应的化学方程式为 _ 。 (2) N
温馨提示
- 1. 本站所有资源如无特殊说明,都需要本地电脑安装OFFICE2007和PDF阅读器。图纸软件为CAD,CAXA,PROE,UG,SolidWorks等.压缩文件请下载最新的WinRAR软件解压。
- 2. 本站的文档不包含任何第三方提供的附件图纸等,如果需要附件,请联系上传者。文件的所有权益归上传用户所有。
- 3. 本站RAR压缩包中若带图纸,网页内容里面会有图纸预览,若没有图纸预览就没有图纸。
- 4. 未经权益所有人同意不得将文件中的内容挪作商业或盈利用途。
- 5. 人人文库网仅提供信息存储空间,仅对用户上传内容的表现方式做保护处理,对用户上传分享的文档内容本身不做任何修改或编辑,并不能对任何下载内容负责。
- 6. 下载文件中如有侵权或不适当内容,请与我们联系,我们立即纠正。
- 7. 本站不保证下载资源的准确性、安全性和完整性, 同时也不承担用户因使用这些下载资源对自己和他人造成任何形式的伤害或损失。
最新文档
- 2024四川泸州兴绿园林绿化有限责任公司及子公司社会公开招聘7人笔试参考题库附带答案详解
- 职高室内设计课程
- 2025年起重机械机械安装维修考试试题题库
- 七年级技术试卷及答案
- 物流行业卡通
- 压裂低压班培训课件
- 美容行业年度计划
- 栏杆漆施工方案
- 基坑勘测方案模板范本
- 2024年秋新冀教版一年级上册数学 0.1 认识新朋友 教学课件
- 湖北省武汉市江岸区2023-2024学年八年级下学期期中物理试题(解析版)
- 内蒙古呼和浩特市第十六中学2024-2025学年高二语文上学期期中试题无答案
- 第一单元 歌唱祖国-《 中华人民共和国国歌》课件 2023-2024学年人音版初中音乐七年级上册
- 智能导盲杖毕业设计创新创业计划书2024年
- 市政道路及设施零星养护服务技术方案(技术标)
- CQI-8分层过程审核指南(附全套表格)
- 搞好班组安全管理工作
- 生物医学体系的确立与发展
- 江苏省南京市秦淮区2023-2024学年七年级下学期期中数学试卷(含答案)
- ISO27001:2022信息安全管理手册+全套程序文件+表单
- 劳动节英文介绍节日由来文化风俗劳动名言课件

评论
0/150
提交评论