



版权说明:本文档由用户提供并上传,收益归属内容提供方,若内容存在侵权,请进行举报或认领
文档简介
1、空气电池空气电池锂电池锂电池二、化学电源二、化学电源一次电池、二次电池、燃料电池一次电池、二次电池、燃料电池选修选修4 4p74 p74 一次电池:一次电池:只能使用一次,不能充电复原继只能使用一次,不能充电复原继续使用的化学电池。续使用的化学电池。碱性锌碱性锌-锰电池、锰电池、 银银-锌纽扣电池等锌纽扣电池等二次电池:二次电池:放电后能充电复原继续使用的化学电放电后能充电复原继续使用的化学电池。如铅蓄电池、氢镍电池、锂电池等。池。如铅蓄电池、氢镍电池、锂电池等。燃料电池:燃料电池:连续地连续地将燃料和氧化剂的化学能将燃料和氧化剂的化学能直接直接转换成电能的化学电池转换成电能的化学电池如:氢氧
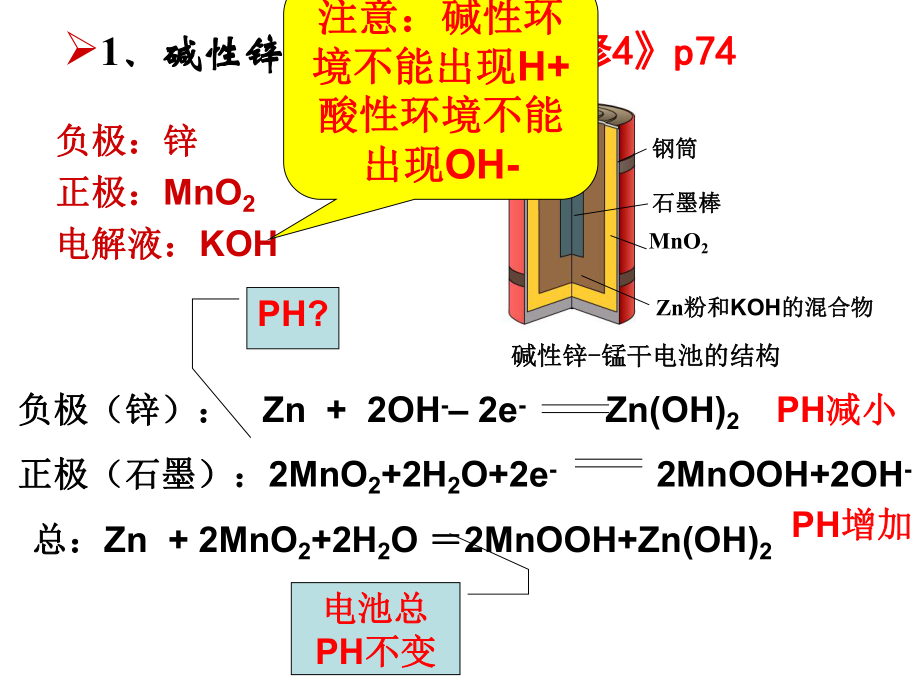
2、燃料电池、如:氢氧燃料电池、CH4、乙醇燃料电池等、乙醇燃料电池等电池优劣的电池优劣的判断:判断:P74比能量(比能量(Wh)/kg, (Wh)/L)比功率比功率(W/kg, W/L)可储存可储存1、碱性锌锰干电池、碱性锌锰干电池选修选修4 4p74 p74 钢筒钢筒石墨棒石墨棒Zn粉粉和和KOH的混合物的混合物碱性锌碱性锌- -锰干电池的结构锰干电池的结构MnO2负极:锌负极:锌正极:正极:MnO2电解液:电解液:KOH负极(锌):负极(锌): Zn + 2OH- 2e- Zn(OH)2正极(石墨):正极(石墨):2MnO2+2H2O+2e- 2MnOOH+2OH-总:总:Zn + 2MnO
3、2+2H2O 2MnOOH+Zn(OH)2PH?PH减小减小PH增加增加电池总电池总PH不变不变注意:碱性环注意:碱性环境不能出现境不能出现H+酸性环境不能酸性环境不能出现出现OH-负极(锌筒):负极(锌筒):Zn-2e-=Zn2+,正极(石墨)正极(石墨):2NH4+2MnO2 + 2e-=2NH3+Mn2O3+H2O2、干电池、干电池(NH4Cl糊状物为电解质、糊状物为电解质、酸性酸性)总反应:总反应:Zn+2NH4+2MnO2= Zn2+2NH3+Mn2O3+H2O钮扣电池:不锈钢制成一个由正钮扣电池:不锈钢制成一个由正极壳和负极盖组成的小圆盒,盒极壳和负极盖组成的小圆盒,盒内靠正极一端
4、填充由内靠正极一端填充由AgAg2 2O O和少量和少量石墨组成的正极活性材料,负极石墨组成的正极活性材料,负极盖一端填充锌汞合金作负极活性盖一端填充锌汞合金作负极活性材料,电解质溶液为浓材料,电解质溶液为浓KOHKOH溶液,溶液,已知电池内已知电池内ZnZn的氧化产物为的氧化产物为ZnOZnO。3 3、银、银- -锌电池锌电池(负极(负极- -锌、正极锌、正极- - Ag2O、电解质为电解质为KOHKOH)负极:负极: Zn + 2OH- 2e- = Zn(OH)2正极:正极: Ag2O + H2O + 2e- = 2Ag + 2OH-总反应:总反应: Zn + Ag2O + H2O = Z
5、n(OH)2 + 2Ag 4、 Ni-Cd电池电池电池电池 Ni-Cd电池:电池:Cd + 2NiO(OH) + 2H2O = 2Ni(OH)2 + Cd(OH)2 Ni-Fe电池:电池:Fe + 2NiO(OH) + 2H2O = 2Ni(OH)2 + Fe(OH)2 负极:负极:Cd-2e- +2OH-=Cd(OH)2正极正极:2NiO(OH) +2e- +2H2O=2Ni(OH)2 +2OH-5. 海水电池(电解质溶液为海水)海水电池(电解质溶液为海水)负极:负极:4Al - 12e- = 4Al3+,正极:正极:3O2+ 6H2O + 12e- = 12OH-总反应:总反应:4Al +
6、 3O2 + 6H2O = 4Al(OH)3(6 6)铅蓄电池)铅蓄电池: :总电池反应总电池反应: : PbO PbO2 2PbPb2H2H2 2SOSO4 4 2PbSO2PbSO4 42H2H2 2O O电极:电极:PbPb为负极为负极, PbO, PbO2 2为正极为正极. .电解液电解液: : H H2 2SOSO4 4溶液溶液电极反应式电极反应式: :放电时:放电时: 负极负极( (PbPb) ) :PbPb( (s s) )SOSO4 42-2-( (aqaq) )2e2e- -PbSOPbSO4 4( (s s) ) 正极正极(PbO(PbO2 2) ) PbOPbO2 2s
7、s4H4H aqaq SOSO4 42 2 aqaq 2e2e PbSOPbSO4 4s s2H2H2 2O OL L充电充电放电放电二次电池二次电池(可充电电池):(可充电电池):当电池中有当电池中有2mol2mol电子电子通过时,消耗硫酸?通过时,消耗硫酸?7. 锂电池锂电池(非水有机溶剂电解液)(非水有机溶剂电解液)负极:负极:2Li - 2e- = 2Li+,正极:正极:I2 + 2e- = 2I-,总反应:总反应:2Li + I2 = 2LiI跟其它金属作负极相比,使用寿命延长,跟其它金属作负极相比,使用寿命延长,高能、质轻、电压高、工作效率高、储存高能、质轻、电压高、工作效率高、储
8、存寿命长。为什么?寿命长。为什么?与作负极材料的金属相比较,相同质量时锂与作负极材料的金属相比较,相同质量时锂提供电子数最多。提供电子数最多。 燃料电池三、燃料电池:三、燃料电池:P77 P77 连续地连续地将燃料和氧化剂的化学能将燃料和氧化剂的化学能直接直接转换成转换成电能的化学电池(电能的化学电池(与一般电池不同?与一般电池不同?P77)一般的可燃物均可与一般的可燃物均可与O2组成燃料电池,如组成燃料电池,如H2、CO、CH4、N2H4、乙醇等。乙醇等。负极负极-可燃物;正极可燃物;正极-氧气氧气优点:能量转化率高优点:能量转化率高污染小(环境友好、绿色电站)污染小(环境友好、绿色电站)装
9、置可持续使用燃料装置可持续使用燃料缺点:输出电压低体积较大附属设备多等缺点:输出电压低体积较大附属设备多等电极本身不是活性物质,电极本身不是活性物质,只是一个催化原件只是一个催化原件1 1、氢氧燃料电池、氢氧燃料电池电极电极: Pt制作的惰性电极制作的惰性电极负极负极a: a: 通入氢气通入氢气正极正极b: b: 通入氧气通入氧气电解质电解质: : 酸性、中性或碱性介质酸性、中性或碱性介质2H2 + = 2H2OKOH溶液溶液H2O2H2Oa b1 1、氢氧燃料电池、氢氧燃料电池介质介质电池反应:电池反应: 2H2 + = 2H2O 酸性酸性负极负极正极正极中性中性负极负极 正极正极碱性碱性负
10、极负极正极正极2H2 - 4e- = 4H+O2 + 2H2O + 4e-= 4OH-2H2 - 4e- = 4H+ O2 + 4H+ + 4e-= 2H2O2H2 +4OH- 4e- = 4H2O O2 + 2H2O + 4e-= 4OH-规律规律: :酸性条件下不能出现酸性条件下不能出现OHOH, 碱性条件下不能出现碱性条件下不能出现H H。2、甲烷燃料电池、甲烷燃料电池(电解质为(电解质为KOH)负极:负极:CH4 + 10OH- - 8e- = CO32- + 7H2O正极:正极:2O2 + 4H2O +8e- = 8OH-总反应:总反应:CH4 + 2O2 + 2OH- = CO32
11、- + 3H2O思考:思考:甲醇燃料电池甲醇燃料电池 (电解质为电解质为KOHKOH)负极:负极:CH4 - 8e- + 2H2O = CO2 + 8H+正极:正极:2O2 +8e-+ 8H+ = 4H2O总反应:总反应:CH4 + 2O2 = CO2+ 2H2O甲烷燃料电池甲烷燃料电池(电解质为(电解质为H2SO4)3 3、甲醇燃料电池、甲醇燃料电池 (电解质为电解质为KOHKOH)负极:负极:2CH3OH - 12e- +16OH-=2CO32-+12H2O正极:正极:3O2 +12e- + 6H2O = 12OH-总反应:总反应:2CH3OH+3O2+4OH- =2CO32-+ 6H2O
12、 甲醇燃料电池甲醇燃料电池 (电解质为电解质为H H2 2SOSO4 4)负极:负极:2CH3OH - 12e- +2H2O=2CO2+12H+正极:正极:3O2 +12e- + 12H+ = 6H2O总反应:总反应:2CH3OH+3O2=2CO2+ 4H2O一种新型燃料电池,它以多孔镍板为电极插入一种新型燃料电池,它以多孔镍板为电极插入KOH溶液中,然后分别向两极通入乙烷和氧气,溶液中,然后分别向两极通入乙烷和氧气,其总反应为:其总反应为:2C2H6 + 7O2 + 8KOH4K2CO3 + 10H2O,有关此,有关此电池的推断正确的是电池的推断正确的是 ( )A负极反应为:负极反应为:14
13、 H2O +7O2 + 28e = 28OHB放电一段时间后,负极周围放电一段时间后,负极周围pH升高升高C每消耗每消耗1mol C2H6,则电路上转移电子为,则电路上转移电子为14 molD放电过程中放电过程中KOH的物质的量浓度不变的物质的量浓度不变C 练一练练一练4、熔融盐为电解质、熔融盐为电解质-燃料电池燃料电池 是一种具有极高发电效率的大功率化学电池,在是一种具有极高发电效率的大功率化学电池,在加拿大等少数发达国家己接近民用工业化水平。加拿大等少数发达国家己接近民用工业化水平。按其所用燃料或熔融盐的不同,有多个不同的品按其所用燃料或熔融盐的不同,有多个不同的品种,如天然气、种,如天然
14、气、CO、-熔融碳酸盐型、熔融磷酸熔融碳酸盐型、熔融磷酸盐型等等,一般要在一定的高温下(确保盐处于盐型等等,一般要在一定的高温下(确保盐处于熔化状态)才能工作。熔化状态)才能工作。例:例:以以Li2CO3和和Na2CO3熔融物为电解质,一极熔融物为电解质,一极通入通入CO,另一极通入,另一极通入CO2和和O2,组成燃料电池。,组成燃料电池。负极:负极: 2CO4e- 2CO32- = 4CO2正极:正极:O24e 2CO2= 2CO32-总反应:总反应:2CO+ 2O2 = 2CO2例:例:一种新型燃料电池,一极通入空气,另一极通入一种新型燃料电池,一极通入空气,另一极通入甲烷气体;电解质是掺
15、杂氧化钇甲烷气体;电解质是掺杂氧化钇 Y2O3 的氧化锆的氧化锆 ZrO2 晶体,在熔融状态下能传导晶体,在熔融状态下能传导O2 。5、熔融氧化物为电解质、熔融氧化物为电解质-燃料电池燃料电池 负极:负极:CH4 - 8e- + 4O2 = CO2 + 2H2O正极:正极:2O2 + 8e- = 4O2 总反应:总反应:CH4 + 2O2 = CO2+ 2H2O(08宁夏卷)一种燃料电池中发生的化学反应为:在宁夏卷)一种燃料电池中发生的化学反应为:在酸性溶液中甲醇与氧作用生成水和二氧化碳。该电池负酸性溶液中甲醇与氧作用生成水和二氧化碳。该电池负极发生的反应是(极发生的反应是( )A.CH3OH
16、(g)+O2(g)=H2O(1)+CO2(g)+2H+(aq)+2e BO2(g)+4H+(aq)+4e=2H2O(L)CCH3OH(g)+H2O(1)=CO2(g)+6H+(aq)+6e DO2(g)+2H2O(1)+4e=4OH C例题例题1 12. 有人设计出利用有人设计出利用CH4和和O2的反应,用铂电极在的反应,用铂电极在KOH溶液中构成原电池。电池的总反应类似于溶液中构成原电池。电池的总反应类似于CH4在在O2中中燃烧,则下列说法正确的是燃烧,则下列说法正确的是 ( ) 每消耗每消耗1molCH4可以向外电路提供可以向外电路提供8mole- 负极上负极上CH4失去电子,电极反应式:
17、失去电子,电极反应式: CH4 + 10 OH- 8e- = CO32- + 7 H2O 正极上是正极上是O2获得电子,电极反应式为:获得电子,电极反应式为: O2 + 2 H2O + 4 e- = 4 OH- 电池放电后,溶液电池放电后,溶液pH升高升高 A. B. C. D. A 3. 氢镍电池是近年开发出来的可充电电池,氢镍电池是近年开发出来的可充电电池,它可以取代会产生镉污染的镉镍电池。氢镍它可以取代会产生镉污染的镉镍电池。氢镍电池的总反应式是:电池的总反应式是: 1/2H2+NiO(OH) Ni(OH)2据此反应判断,下列叙述中正确的是(据此反应判断,下列叙述中正确的是( )A. 电
18、池放电时,负极周围溶液的电池放电时,负极周围溶液的pH不不 断增大断增大B. 电池放电时,镍元素被氧化电池放电时,镍元素被氧化C. 电池充电时,氢元素被还原电池充电时,氢元素被还原D. 电池放电时,电池放电时,H2是负极是负极CD【小结小结】书写燃料电池电极反应式一般分为三步:书写燃料电池电极反应式一般分为三步:第一步,先写出燃料电池的总反应方程式;第一步,先写出燃料电池的总反应方程式;第二步,再写出燃料电池的正极反应式;第二步,再写出燃料电池的正极反应式;第三步,在电子守恒的基础上用燃料电池的第三步,在电子守恒的基础上用燃料电池的总反应式减去正极反应式即得到负极反应式。总反应式减去正极反应式
19、即得到负极反应式。 注意:注意:溶液的酸碱性溶液的酸碱性4 4、燃料电池、燃料电池(1 1)写出正确的燃烧反应化学方程式并)写出正确的燃烧反应化学方程式并找出两极找出两极放电的物质放电的物质,负氧正还负氧正还;(2 2)根据电解液()根据电解液(如溶液的酸碱性如溶液的酸碱性)改)改写燃料电池总反应;写燃料电池总反应;(3 3)写出正极的电极反应式;)写出正极的电极反应式;(4 4)由燃料电池总反应式减去正极的电)由燃料电池总反应式减去正极的电极反应式得到负极的电极反应式。极反应式得到负极的电极反应式。第一步,燃料电池总反应方程式的书写第一步,燃料电池总反应方程式的书写 根据根据燃料燃烧反应燃料
20、燃烧反应写出燃料电池的总反应方程式写出燃料电池的总反应方程式 #若是氢氧燃料电池,其电池总反应方程式不随电解质若是氢氧燃料电池,其电池总反应方程式不随电解质的状态和电解质溶液的酸碱性变化而变化,的状态和电解质溶液的酸碱性变化而变化,即即2H2+O2=2H2O #若燃料是含碳元素的可燃物,其电池总反应方程式若燃料是含碳元素的可燃物,其电池总反应方程式就与电解质的状态和电解质溶液的酸碱性有关,要就与电解质的状态和电解质溶液的酸碱性有关,要考虑燃烧反应后产物是否与电解质发生反应考虑燃烧反应后产物是否与电解质发生反应 第二步,燃料电池正极反应式的书写第二步,燃料电池正极反应式的书写 正极反应的本质都是
21、正极反应的本质都是O O2 2得电子生成得电子生成O O2-2-离子,离子,故正极反应式的基础都是故正极反应式的基础都是O O2 24e4e- -=2O=2O2-2- 电解质为酸性电解质溶液(如稀硫酸)电解质为酸性电解质溶液(如稀硫酸)O O2-2-离子结合离子结合H H+ +离子生成离子生成H H2 2O O正极反应式为正极反应式为O O2 24H4H+ +4e+4e- -=2H=2H2 2O O 电解质为中性或碱性电解质溶液电解质为中性或碱性电解质溶液(如如NaCl溶液或溶液或NaOH溶液溶液)O O2-2-离子结合离子结合H H2 2O O生成生成OHOH- -离子离子正极反应式为正极反
22、应式为O O2 22H2H2 2O +4eO +4e- -=4OH=4OH- - 第三步,燃料电池负极反应式的书写第三步,燃料电池负极反应式的书写 一般燃料电池的负极反应式都是采用间接方法书写一般燃料电池的负极反应式都是采用间接方法书写 即在电子守恒的基础上用总反应式减去正极反应式即在电子守恒的基础上用总反应式减去正极反应式 【小结小结】直接书写燃料电池负极反应式直接书写燃料电池负极反应式 (1 1)写出氧化还原的基本框架)写出氧化还原的基本框架(正极:氧化剂和还原产物;负极:还原剂和氧化产物)(正极:氧化剂和还原产物;负极:还原剂和氧化产物) (2 2)分析氧化还原的得失电子数,配平电子数)
23、分析氧化还原的得失电子数,配平电子数 (3 3)根据电荷守恒和溶液酸碱性,通过)根据电荷守恒和溶液酸碱性,通过H H+ +和和OHOH- - 配平电荷数配平电荷数 (4 4)根据元素守恒配)根据元素守恒配H H2 2O O4. 银锌电池银锌电池(电解质为(电解质为KOH)5. 海水电池海水电池(电解质溶液为海水)(电解质溶液为海水)负极:负极:4Al - 12e- = 4Al3+,正极:正极:3O2+ 6H2O + 12e- = 12OH-总反应:总反应:4Al + 3O2 + 6H2O = 4Al(OH)3负极:负极:Zn+ 2OHZn+ 2OH- - -2e-2e- - =ZnO+H=Zn
24、O+H2 2O O 正极:正极:AgAg2 2O+ HO+ H2 2OO +2e+2e- - =2Ag+ 2OH=2Ag+ 2OH- - 总反应:总反应:AgAg2 2O+ Zn =ZnO+ 2AgO+ Zn =ZnO+ 2Ag(09年海南化学年海南化学15)()(9分)分)LiSOCl2电池可用于心脏起搏器。该电池的电极材料分电池可用于心脏起搏器。该电池的电极材料分别为锂和碳,电解液是别为锂和碳,电解液是LiAlCl4SOCl2。电池的总反应可。电池的总反应可表示为:表示为:4Li+2SOCl2 =4LiCl+S +SO2。请回答下列问题:请回答下列问题:(1)电池的)电池的 负极材料为负极
25、材料为 ,发生的电极反应为,发生的电极反应为 ;(2)电池正极发生的电极反应为)电池正极发生的电极反应为 ;(3)SOCl2易挥发,实验室中常用易挥发,实验室中常用NaOH溶液吸收溶液吸收SOCl2,有有Na2SO3和和NaCl生成。生成。 如果把少量水滴到如果把少量水滴到SOCl2中,实中,实验现象是验现象是 ,反应的化学方程式为反应的化学方程式为 ;(4)组装该电池必须在无水、无氧的条件下进行,原因)组装该电池必须在无水、无氧的条件下进行,原因是是 。Li2e=Li(2分)分)锂锂2SOCl24e=4ClSSO2(2分)分)出现白雾,有刺激性气体生成出现白雾,有刺激性气体生成SOCl2H2
26、O=SO22HCl(3分)分)锂是活泼金属,易与锂是活泼金属,易与H2O、O2反应;反应;SOCl2也可与水反应(也可与水反应(2分)分)高考题再现高考题再现2010浙江浙江9. Li-Al/FeS电池是一种正在开发的车载电池是一种正在开发的车载电池,该电池中正极的电极反应式为:电池,该电池中正极的电极反应式为: 2Li+FeS+2e-Li2S+Fe 有关该电池的下列中,有关该电池的下列中, 正确的是正确的是A.Li-Al在电池中作为负极材料,该材料中在电池中作为负极材料,该材料中Li的化的化 合价为合价为+1价价B.该电池的电池反应式为:该电池的电池反应式为:2Li+FeSLi2S+FeC.
27、负极的电极反应式为负极的电极反应式为Al-3e-=Al3+来来D.充电时,阴极发生的电极反应式为:充电时,阴极发生的电极反应式为: 2Li s+Fe-22eLiFeSC高考题再现高考题再现练习练习6 6、高铁电池是一种新型可充电电池,与普通高能电、高铁电池是一种新型可充电电池,与普通高能电池相比,该电池长时间保持稳定的放电电压。高铁电池的池相比,该电池长时间保持稳定的放电电压。高铁电池的总反应为:总反应为:3Zn2K2FeO48H2O 3Zn(OH)22Fe(OH)34KOH,下列叙述不正确的是,下列叙述不正确的是 A. 放电时负极反应为:放电时负极反应为:Zn2e 2OH Zn(OH)2B 充电时阳极反应为:充电时阳极反应为: Fe OH 33e 5OH FeO42-4H2OC. 放电时每转移放电时每转移3 mol电子,正极有电子,正极有1 molK2FeO4被氧化被氧化 D. 放电时正极附近溶液的碱性增强放电时正极附近溶液的碱性增强C ( (燃料电池燃料电池) )宇宙飞船上的氢氧燃料电池,其电宇宙飞船上的氢氧燃料电池,其电池反应为:池反应为:2H2H2 2O O2 22H2H2 2O O,试写出电解质溶液为,试写出电解质溶液为盐酸时的电极反应式,并指出各电极和电解质溶盐酸时的电极反应式,并指出各电极和
温馨提示
- 1. 本站所有资源如无特殊说明,都需要本地电脑安装OFFICE2007和PDF阅读器。图纸软件为CAD,CAXA,PROE,UG,SolidWorks等.压缩文件请下载最新的WinRAR软件解压。
- 2. 本站的文档不包含任何第三方提供的附件图纸等,如果需要附件,请联系上传者。文件的所有权益归上传用户所有。
- 3. 本站RAR压缩包中若带图纸,网页内容里面会有图纸预览,若没有图纸预览就没有图纸。
- 4. 未经权益所有人同意不得将文件中的内容挪作商业或盈利用途。
- 5. 人人文库网仅提供信息存储空间,仅对用户上传内容的表现方式做保护处理,对用户上传分享的文档内容本身不做任何修改或编辑,并不能对任何下载内容负责。
- 6. 下载文件中如有侵权或不适当内容,请与我们联系,我们立即纠正。
- 7. 本站不保证下载资源的准确性、安全性和完整性, 同时也不承担用户因使用这些下载资源对自己和他人造成任何形式的伤害或损失。
最新文档
- 2024年陪诊师考试省时攻略与试题及答案
- 实施城市公交线路优化调整计划
- 兽医疾病控制方法试题及答案
- 2025年份第一季度餐饮业跨平台评价数据迁移保密条款
- 2025年贵州省安全员-A证考试题库附答案
- 兽医行业投资与市场拓展策略试题及答案
- 体育训练运动营养与恢复策略研究题
- 复习安排2024人力资源管理师考试试题及答案
- 2024年矿产资源开发试题及答案
- 高精度设备维修与保养手册
- 大学生创新创业训练计划项目申报书(模板)
- 争做最美班级主题班会课件
- 铁路职工政治理论应知应会题库
- 2020年交安A、B、C证(公路)考试题库1088题(含答案)
- 墙绘验收单模板
- 节后复工检查表
- 财务有哪些制度要上墙
- 医学教学课件:软组织肿瘤影像诊断
- 矿山矿石损失与贫化管理规程
- 安全生产晨会管理制度
- 直线导轨装配文档课件

评论
0/150
提交评论