



版权说明:本文档由用户提供并上传,收益归属内容提供方,若内容存在侵权,请进行举报或认领
文档简介
1、贵州省六盘水市第七中学2021-2021学年高一化学上学期期末考试试题考试时间:90分钟 试卷满分:100分 试题说明:1.本试卷共分为两卷。第I卷为选择题,共16个小题;第卷非选择题,共4个小题。 2.所以试题均在答题卡上作答。3.可能用到的相对原子质量:H 1 C 12 0 16 Na 23 Cl 35.5 Fe 56 第卷(选择题 共42分)一、选择题(共16小题,每小题3分,共48分,每小题四个选项中只有一个选项符合要求)1化学与生活密切相关。下列说法正确的是A医用消毒酒精中乙醇的浓度(体积分数)为95%B硅胶可用作瓶装药品、袋装食品的干燥剂C化石燃料完全燃烧不会造成大气污染D铁比铜金
2、属性强,FeCl3腐蚀Cu刻制印刷电路板2下列有关实验操作的叙述错误的是ACCl4萃取碘水中的I2,先从分液漏斗下口放出有机层,后从上口倒出水层B制备蒸馏水时向蒸馏烧瓶中加入碎瓷片,防止暴沸C金属钠着火时,立即使用泡沫灭火器灭火D用试管加热碳酸氢钠固体时,使试管口微向下倾斜3下列有关实验的操作正确的是实验目的实验操作A配制浓度为0.010的KMnO4溶液用托盘天平称取KMnO4固体0.158 g,放入100 mL容量瓶中,加水溶解并稀释至刻度B浓盐酸与MnO2反应制备纯净Cl2气体产物先通过浓硫酸,后通过饱和食盐水C配制稀硫酸先将浓硫酸加入烧杯中,后倒入蒸馏水D排水法收集KMnO4分解产生的O
3、2先移出导管,后熄灭酒精灯4设NA表示阿伏加德罗常数,下列叙述正确的是A常温常压下,22gCO2含有的氧原子数为NAB标准状况下,2.24 L CCl4含有的分子数为0.1NAC常温常压下,0.1molL1的MgCl2溶液中含Cl数为0.2NAD常温常压下,5.6g铁与足量Cl2完全反应,转移电子数为0.2NA 5根据胶体的相关性质,下列叙述错误的是A当光束通过Fe(OH)3胶体时,可以看到一条光亮的“通路” B制备Fe(OH)3胶体,将NaOH浓溶液滴加到饱和的FeCl3溶液中 C存在于污水中的胶体物质,则常用投明矾、硫酸铁等电解质的方法进行处理 D胶体化学的应有很广,是制备纳米材料的有效方
4、法之一6下列关于离子共存或离子反应的说法正确的是A某无色溶液中可能大量存在Fe3、H、I、MnO4B与Al反应能放出H2的溶液中:Fe2、K、ClO、SO42CFe2与H2O2在酸性溶液中的反应:2Fe2+H2O2+2H=2Fe3+2H2OD向Na2SiO3溶液中通入过量CO2:SiO32+ CO2+ H2O=H2SiO3+CO327化学与生活密切相关,下列应用中利用了物质氧化性的是A漂白粉用于生活用水的消毒 B氢氧化铝用于中和过多胃酸C食醋用于除水垢 D氢氟酸用于刻蚀玻璃8下列变化中,气体被还原的是ACO2使Na2O2固体变白 BCl2使KBr溶液变黄C一定条件下H2能使CuO固体变红 DN
5、H3使AlCl3溶液产生白色沉淀9下列有关叙述不正确的是A钠燃烧时生成氧化钠 B钠燃烧时发出黄色的火焰 C铝是地壳里含量最多的金属元素 D在常温下,铝与氧气作用生成致密氧化膜10向下列各物质水溶液中滴加稀硫酸或氯化钙溶液时,均有白色沉淀生成的是 ANaOH BNa2CO3 CNaClDNa2SiO311将足量固体或气体加入溶液中,反应后溶液的质量减少的是A将Al粉投入NaOH溶液 B将Fe粉投入CuSO4溶液C将Cl2通入澄清石灰水中 D将Fe粉投入FeCl3溶液12下列叙述正确的是A在酒精灯加热条件下,Na2CO3、NaHCO3固体都能发生分解BCl2是一种有毒气体,不可用于自来水的杀菌消毒
6、CSiO2既能和NaOH溶液反应又能和氢氟酸反应,所以是两性氧化物DNa2SiO3水溶液俗称水玻璃,是制备硅胶和木材防火剂等的原料13 有一包白色粉末,为鉴别其成分进行如下实验:()将部分白色粉末加入水中,振荡,有白色沉淀生成;()向()的悬浊液中加入过量的稀硝酸,白色沉淀全部消失,并有气泡产生;()取少量()的溶液滴入稀硫酸,有白色沉淀生成。ANaHCO3、NaOH BAgCl、NaNO3 CK2CO3、Ba(NO3)2 DKOH、CuSO414下列除杂(括号内为杂质)方案不正确的是选项待提纯的物质选用的试剂操作的方法ANaCl(HCl)蒸发BCu(CuO)稀硫酸溶解、过滤、洗涤CSiO2(
7、Al2O3)稀盐酸溶解、过滤、洗涤DFeCl2(FeCl3)氢氧化钠溶液溶解、过滤、洗涤15常温下,下列各组物质中,X既能与Y反应又能与Z反应的是YXZH2O(g)FeZnSO4溶液KOH溶液Al稀硫酸SiCl2H2酸性高锰酸钾溶液Fe2(aq)漂白液 A B C D16下列陈述、正确并且有因果关系的是选项陈述陈述A Fe3具有氧化性 Fe3遇KSCN溶液变红B Si是半导体材料 可用Si制备光导纤维C 溶解度:CaCO3Ca(HCO3)2 溶解度:Na2CO3NaHCO3D 二氧化氯(ClO2)具有氧化性 可用ClO2代替Cl2作为自来水新型消毒剂AA BB CC DD第卷(非选择题 共52
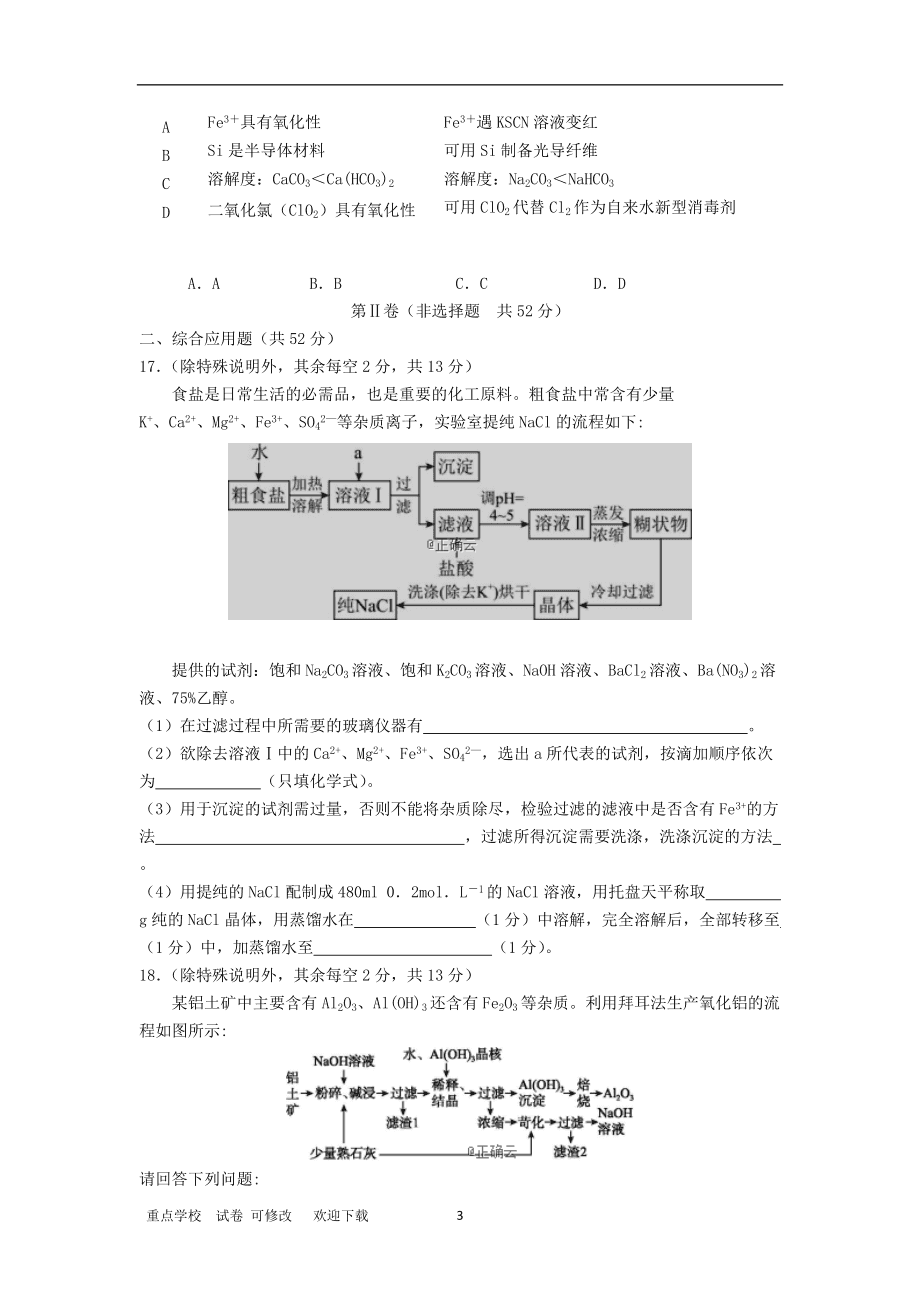
8、分)二、综合应用题(共52分)17(除特殊说明外,其余每空2分,共13分)食盐是日常生活的必需品,也是重要的化工原料。粗食盐中常含有少量K+、Ca2+、Mg2+、Fe3+、SO42等杂质离子,实验室提纯NaCl的流程如下:提供的试剂:饱和Na2CO3溶液、饱和K2CO3溶液、NaOH溶液、BaCl2溶液、Ba(NO3)2溶液、75%乙醇。(1)在过滤过程中所需要的玻璃仪器有 。(2)欲除去溶液中的Ca2+、Mg2+、Fe3+、SO42,选出a所代表的试剂,按滴加顺序依次为 (只填化学式)。(3)用于沉淀的试剂需过量,否则不能将杂质除尽,检验过滤的滤液中是否含有Fe3+的方法 ,过滤所得沉淀需要
9、洗涤,洗涤沉淀的方法 。(4)用提纯的NaCl配制成480ml 02molL1的NaCl溶液,用托盘天平称取 g纯的NaCl晶体,用蒸馏水在 (1分)中溶解,完全溶解后,全部转移至 (1分)中,加蒸馏水至 (1分)。18(除特殊说明外,其余每空2分,共13分)某铝土矿中主要含有Al2O3、Al(OH)3还含有Fe2O3等杂质。利用拜耳法生产氧化铝的流程如图所示:请回答下列问题:(1)粉碎后的铝土矿碱浸时应在较高温度下进行,其目的是 。滤渣1的主要成分为 。(1分)(2)Al2O3与NaOH溶液反应的离子方程式为 。(3)加Al(OH)3晶核的目的是促进Al(OH)3的析出。上述“稀释、结晶”工
10、艺,也可用通入足量的 气体的方法来代替。(已知:通入该气体后,其产物之一可用来做发酵粉)。(4)焙烧过程中发生的化学方程式为 。(5)浓缩所得的NaOH溶液由于吸收了空气中的CO2而含有杂质,该杂质可通过苛化(即与少量熟石灰反应)反应除去,写出苛化反应的化学方程式: 。(6)该生产流程能实现 (填化学式)的循环利用。19(除特殊说明外,其余每空2分,共13分)电子工业常用30%的FeCl3溶液腐蚀敷在绝缘板上的铜箔,制造印刷电路板。(1)写出FeCl3溶液与金属铜发生反应的化学方程式: 。(2)某工程师为了从使用过的腐蚀废液(主要含CuCl2、FeCl3溶液等)中回收铜,并重新获得纯净的FeC
11、l3溶液,准备采用如图所示流程:(已知:加过量为Fe;加过量为稀盐酸;通入为Cl2)上述实验中滤渣的主要物质为 (填化学式)(1分),写出向的合并液中通入的离子方程式: 。配制并保存FeCl2溶液时,需加入铁屑,其目的是 。要证明FeCl3溶液是否含有Fe2+,可选择下列选项中的 (已知:加入该物质后,溶液变蓝)。A加入 K3Fe(CN)6溶液 B加入NaOH溶液 C加入KSCN溶液(3)现有1.2 L含3 mol FeCl2的溶液恰好与0.6 mol HIO3完全反应,还原产物为 (填化学式,已知该物质遇淀粉溶液变蓝),该反应离子方程式为 。20(除特殊说明外,其余每空2分,共13分)ClO
12、2与Cl2的氧化性相近。在自来水消毒和果蔬保鲜等方面应用广泛。某兴趣小组通过图1装置(夹持装置略)对其制备、吸收、释放和应用进行了研究。(已知:装置C的作用是吸收Cl2)稀盐酸FAaNaClO3溶液稳定剂b淀粉+KI溶液图3图2图1(1)仪器B的名称是 (1分)。安装F中导管时,应选用图2中的 。(2)打开B的活塞,A中发生反应:2NaClO3+4HCl2ClO2+Cl2+2NaCl+2H2O为使ClO2在D中被稳定剂充分吸收,滴加稀盐酸的速度宜 (填“快”或“慢”)。(3)关闭B的活塞,ClO2在D中被稳定剂完全吸收生成NaClO2,NaClO2中Cl的化合价为 (1分)。(4)已知在酸性条
13、件下NaClO2可发生反应生成NaCl并释放出ClO2,该反应的离子方程式为 。(5)工业上可用KClO3与Na2SO3在H2SO4存在下制得ClO2,该反应离子方程式为 。(已知:在酸性条件下SO32被ClO3氧化为SO42)(6)已吸收ClO2气体的稳定剂和稳定剂,加酸后释放ClO2的浓度随时间的变化如图3所示,若将其用于水果保鲜,你认为效果较好的稳定剂是 ,(1分)原因是 。化学答案一、选择题(共16小题,每小题3分,共48分,每小题四个选项中只有一个选项符合要求)12345678BCDADCAB910111213141516ADBDCDCD二、综合应用题(共52分)17.(共13分)
14、(1) 漏斗、烧杯、玻璃棒(答对两个给2分) (2)NaOH溶液、BaCl2溶液、Na2CO3溶液(或BaCl2溶液、NaOH溶液、Na2CO3溶液)(2分) (3)取少量滤液加加入KSCN溶液,变红(2分) 沿玻璃棒向漏斗中加水,使水浸没沉淀,等水自然留下,重复23次(2分) (4)59 (2分) 烧杯(1分) 500ml容量瓶(1分) 刻度线(1分)18.(共13分)(1)加快反应速率(合理即给2分) Fe2O3(1分) (2)Al2O32OH2AlO2H2O(2分) (3) CO2(2分)(4)2Al(OH)3Al2O33H2O(2分)(5)Ca(OH)2 Na2CO3CaCO32NaOH(2分) (6)NaOH(2分)19.(共13分)(1)Cu2Fe3Cu22Fe2(2分) (2) Cu、Fe(答对一个给1分) Cl22Fe22Fe32Cl(2分)防止Fe2被氧化或2Fe3Fe3Fe2(2分)
温馨提示
- 1. 本站所有资源如无特殊说明,都需要本地电脑安装OFFICE2007和PDF阅读器。图纸软件为CAD,CAXA,PROE,UG,SolidWorks等.压缩文件请下载最新的WinRAR软件解压。
- 2. 本站的文档不包含任何第三方提供的附件图纸等,如果需要附件,请联系上传者。文件的所有权益归上传用户所有。
- 3. 本站RAR压缩包中若带图纸,网页内容里面会有图纸预览,若没有图纸预览就没有图纸。
- 4. 未经权益所有人同意不得将文件中的内容挪作商业或盈利用途。
- 5. 人人文库网仅提供信息存储空间,仅对用户上传内容的表现方式做保护处理,对用户上传分享的文档内容本身不做任何修改或编辑,并不能对任何下载内容负责。
- 6. 下载文件中如有侵权或不适当内容,请与我们联系,我们立即纠正。
- 7. 本站不保证下载资源的准确性、安全性和完整性, 同时也不承担用户因使用这些下载资源对自己和他人造成任何形式的伤害或损失。
最新文档
- 手工艺社团创意作品展示策划计划
- 净化车间装修工程合同样本
- 共同背债合同标准文本
- 加强财务管理的个人计划
- 中介与按揭合同标准文本
- 内部工程居间合同样本
- 农场鸡舍养殖合同样本
- 乐器代理合同范例
- 2025耕地流转合同范本AA
- 乡村诊所采购合同样本
- 2024年北京市燕山区九年级(初三)一模英语试卷及答案
- +广东省深圳市宝安区十校联考2023-2024学年七年级下学期期中数学试卷+
- 呼吸训练方法
- 建筑给排水施工技术培训
- 林长巡查工作实施方案
- 2024届江苏省宿迁市泗阳县中考化学五模试卷含解析
- (正式版)YBT 016-2024 废钢液压剪切机
- 天津市2024届九年级下学期中考一模考前训练数学试卷(含解析)
- 2023年福建省考评员考试题
- 纸箱厂质量管理制度模版
- 鼻窦炎的术后护理

评论
0/150
提交评论