



版权说明:本文档由用户提供并上传,收益归属内容提供方,若内容存在侵权,请进行举报或认领
文档简介
第三章
滴定分析§3.1滴定分析概述titrimetricanalysis滴定分析法的分类与滴定
反应的条件
标准溶液
标准溶液浓度表示法
滴定分析结果的计算2023/3/162023/3/162023/3/16§3.1滴定分析概述
概述
滴定分析法(titrimetricdetermination)
用滴定管将标准溶液滴加到待测物的溶液中,通过指示剂指示滴定终点的到达,根据标准溶液的浓度和所消耗的体积,算出待测组分的含量。传统分析方法;适用于常量分析;特点:简单、准确、费用低;动画2023/3/16传统分析方法;4标准溶液浓度表示法基准物(primarystandard)表示法:T待测物/滴定剂单位:g·mL-1适用于工业生产中批量分析:m(Fe)=T·V。2滴定分析法的分类与滴定反应的条件titrimetricanalysis——与每毫升标准溶液相当的待测组分的质量。物质的组成与化学式应完全符合;005682g铁,滴定终点(endpoint)(4)具有较大的摩尔质量不满足(2)时:采用反滴定法,如配位滴定法测定铝;(2)沉淀滴定法(容量沉淀法);用滴定管将标准溶液滴加到待测物的溶液中,通过指示剂指示滴定终点的到达,根据标准溶液的浓度和所消耗的体积,算出待测组分的含量。物质的组成与化学式应完全符合;
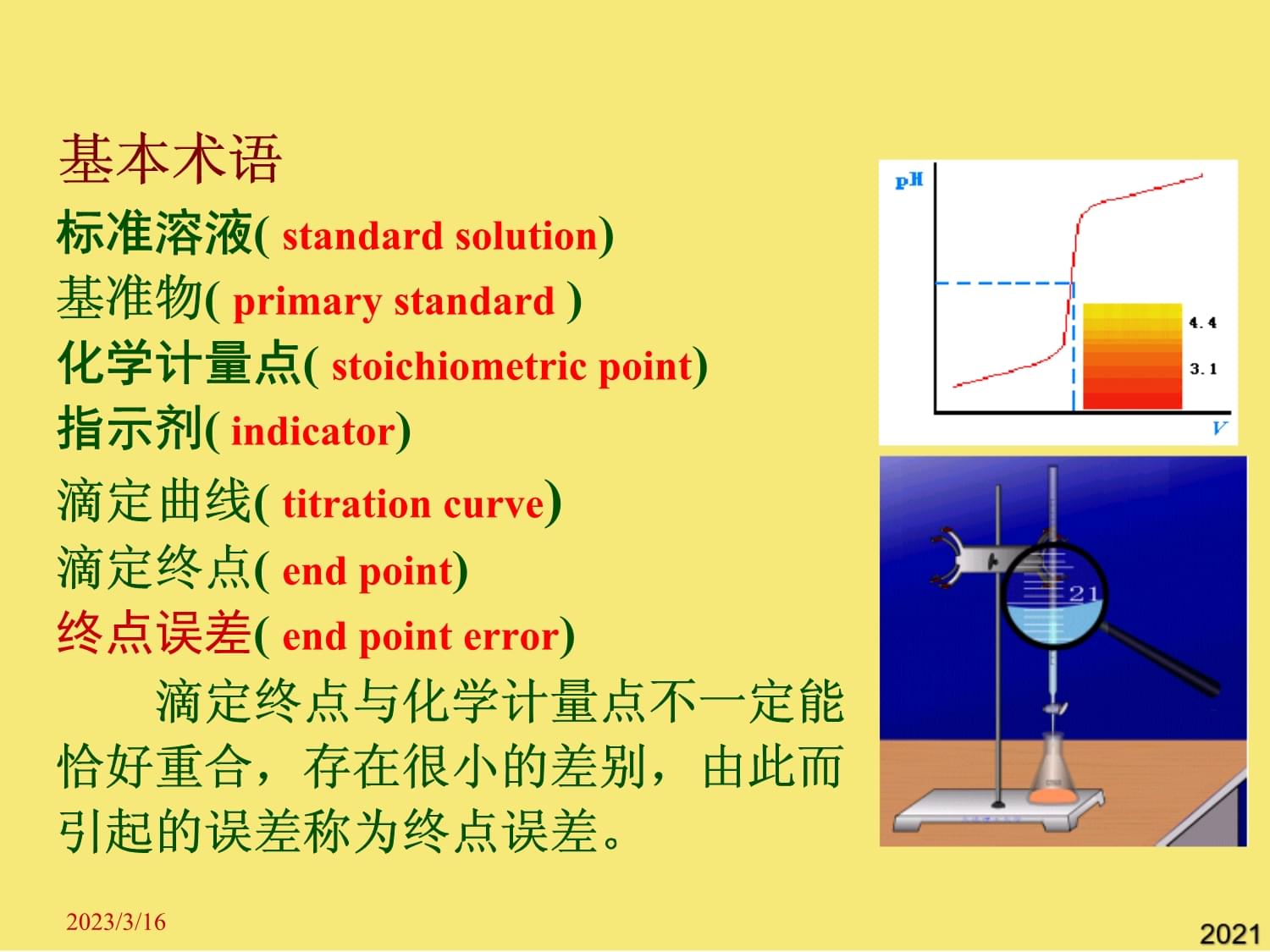
基本术语标准溶液(standardsolution)基准物(primarystandard
)化学计量点(stoichiometricpoint)指示剂(
indicator)滴定曲线(titrationcurve)滴定终点(endpoint)终点误差(endpointerror)
滴定终点与化学计量点不一定能恰好重合,存在很小的差别,由此而引起的误差称为终点误差。2023/3/16§3.2滴定分析法的分类与滴定反应的条件
滴定分析法分类(按照化学反应分类)(1)酸碱滴定法(中和法):以质子传递反应为基础。
H++B-
=HB(2)沉淀滴定法(容量沉淀法);以沉淀反应为基础。
Ag++Cl-
=AgC1↓(3)配位滴定法(络合滴定法):以配位反应为基础。
M2++Y4-
=MY2-(4)氧化还原滴定法:以氧化还原反应为基础。
MnO4-
+5Fe2++8H+=Mn2++5Fe3++4H2O2023/3/16(4)氧化还原滴定法:以氧化还原反应为基础。基准物(primarystandard)滴定终点与化学计量点不一定能恰好重合,存在很小的差别,由此而引起的误差称为终点误差。Ag++Cl-=AgC1↓——与每毫升标准溶液相当的待测组分的质量。表示:lmLKMnO4溶液相当于0.(3)有比较简便的方法确定反应终点titrimetricanalysis1000mol·L-1NaOH标准溶液对H2C2O4的滴定度。反应的条件2滴定分析法的分类与滴定反应的条件不满足(3)时:采用其他方法,如电位滴定。例:强酸滴定强碱。例:强酸滴定强碱。4标准溶液浓度表示法指示剂(indicator)M2++Y4-=MY2-按滴定方式分类:(1)直接滴定例:强酸滴定强碱。(2)间接滴定例:氧化还原法测定钙。(3)返滴定法例:配位滴定法测定铝。(4)置换滴定法例:AlY→AlF62-+Y4-→
ZnY2023/3/16采用:邻苯二甲酸氢钾?草酸?2滴定分析法的分类与滴定反应的条件标准溶液(standardsolution)滴定分析法分类(按照化学反应分类)若以VB为反应完成时标准溶液消耗的体积(mL),mA和MA分别代表物质A的质量(g)和摩尔质量。终点误差(endpointerror)滴定分析法(titrimetricdetermination)4标准溶液浓度表示法标准溶液(standardsolution)不满足(1)时:采用间接法,如碘量法;特点:简单、准确、费用低;(1)酸碱滴定法(中和法):以质子传递反应为基础。反应的条件3.2.1滴定分析对化学反应的要求1.反应定量完成2.反应速率快3.有比较简便的方法确定反应终点满足以上条件可进行直接滴定,否则:不满足(1)时:采用间接法,如碘量法;不满足(2)时:采用反滴定法,如配位滴定法测定铝;不满足(3)时:采用其他方法,如电位滴定。2023/3/16§3.3标准溶液
直接法配制标准溶液可用直接法配制标准溶液的物质,应具备的条件:
1.物质必须具有足够的纯度,即含量≥99.9%;2.物质的组成与化学式应完全符合;3.稳定。2023/3/162.标定
准确称取基准物,溶解后,滴定。间接配制(步骤)1.配制溶液
配制成近似所需浓度的溶液。3.确定浓度
由基准物质量和滴定液体积计算之。2023/3/16基准物应满足的条件:(1)反应定量完成(2)反应速率快(3)有比较简便的方法确定反应终点(4)具有较大的摩尔质量为什么?标定NaOH:采用:邻苯二甲酸氢钾?草酸?2023/3/16§3.4标准溶液浓度表示法1.物质的量浓度(简称浓度)
——单位体积溶液所含溶质的物质的量(nB)。V:溶液的体积。应指明基本单元:原子、分子、离子、电子或他们的组合。单位为mol·L-1。2023/3/16
——与每毫升标准溶液相当的待测组分的质量。
表示法:T待测物/滴定剂单位:g·mL-1例:测定铁含量的KMnO4标准溶液,其浓度表示:或表示:lmLKMnO4溶液相当于0.005682g铁,1mL的KMnO4标准溶液能把0.005682gFe2+→Fe3+。适用于工业生产中批量分析:
m(Fe)=T·V。若:2023/3/16例题:求0.1000mol·L-1NaOH标准溶液对H2C2O4的滴定度。解:NaOH与H2C2O4的反应为:
H2C2O4+2NaOH=Na2C2O4+2H2O2023/3/16浓度c与滴定度T之间关系
aA+bB
温馨提示
- 1. 本站所有资源如无特殊说明,都需要本地电脑安装OFFICE2007和PDF阅读器。图纸软件为CAD,CAXA,PROE,UG,SolidWorks等.压缩文件请下载最新的WinRAR软件解压。
- 2. 本站的文档不包含任何第三方提供的附件图纸等,如果需要附件,请联系上传者。文件的所有权益归上传用户所有。
- 3. 本站RAR压缩包中若带图纸,网页内容里面会有图纸预览,若没有图纸预览就没有图纸。
- 4. 未经权益所有人同意不得将文件中的内容挪作商业或盈利用途。
- 5. 人人文库网仅提供信息存储空间,仅对用户上传内容的表现方式做保护处理,对用户上传分享的文档内容本身不做任何修改或编辑,并不能对任何下载内容负责。
- 6. 下载文件中如有侵权或不适当内容,请与我们联系,我们立即纠正。
- 7. 本站不保证下载资源的准确性、安全性和完整性, 同时也不承担用户因使用这些下载资源对自己和他人造成任何形式的伤害或损失。
最新文档
- 融媒体编辑面试题及答案
- 备考技巧:2024年珠宝鉴定师考试试题及答案
- 2024年美容师行业内外竞争状况分析试题及答案
- 2025年劳动合同制改革要点
- 钢铁是怎样炼成的读书分享
- 2025企业财产保险合同范本
- 生成AI助力高等教育变革
- 2025版财务援助借款合同
- 新疆现代职业技术学院《企业战略管理》2023-2024学年第二学期期末试卷
- 厦门兴才职业技术学院《信息管理专业英语》2023-2024学年第二学期期末试卷
- 《陆上风电场工程概算定额》NBT 31010-2019
- 2023持续炎症-免疫抑制-分解代谢综合征(PICS)
- 炎症性肠病知识讲座
- 中国当代文学智慧树知到答案章节测试2023年青岛滨海学院
- 2023年金山职业技术学院高职单招(英语)试题库含答案解析
- 维生素D教学讲解课件
- 自考高级英语上下册中英翻译
- DB45-T 2228.1-2020公路养护预算编制办法及定额 第1部分:公路养护工程预算编制办法及定额-(高清可复制)
- 起重吊装作业安全卡控细则及工序卡控表
- 二氧化碳灭火器课件
- 《中华人民共和国民法典》宣传手册课件

评论
0/150
提交评论