



版权说明:本文档由用户提供并上传,收益归属内容提供方,若内容存在侵权,请进行举报或认领
文档简介
互变异构与双重反应性第一页,共三十五页,2022年,8月28日第二节、互变异构转变历程和类型
正离子移变:分子中原子或原子团以正离子形式发生转移,这种过程称正离子移变。负离子移变:分子中的原子或原子团以负离子形式发生转移,这种过程称负离子移变。
一、质子移变历程
1、单分子质子移变历程
这一历程表示,失去质子和得到质子是分步进行的。一般酸性较强的物质或在极性强的溶剂中,有利于这一历程进行。
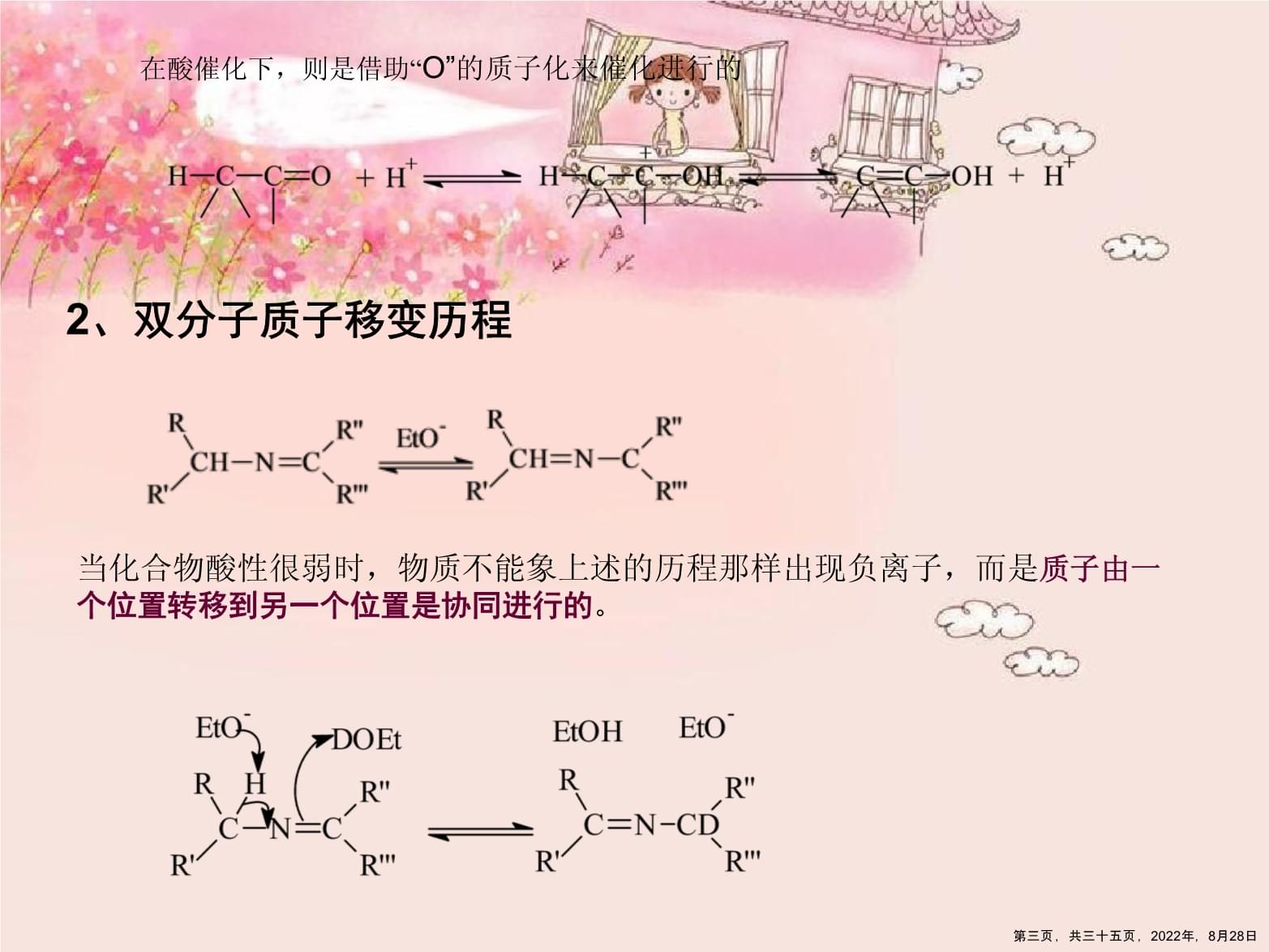
第二页,共三十五页,2022年,8月28日在酸催化下,则是借助“O”的质子化来催化进行的
2、双分子质子移变历程
当化合物酸性很弱时,物质不能象上述的历程那样出现负离子,而是质子由一个位置转移到另一个位置是协同进行的。
第三页,共三十五页,2022年,8月28日二、负离子移变过程(转移基团为负离子)
1、单分子历程:
特点:形成碳正离子中间体
2、双分子历程
特点:协同历程
第四页,共三十五页,2022年,8月28日3、分子内历程
邻苯二甲酸单酯在酸催化下的互变异构就是分子内的负离子移变。
第三节、酮-烯醇式互变异构
采用库尔特-迈依尔(Kart-Meyer)法可以测定酮化物中烯醇式含量,常温下,下列酮烯醇式含量如下表:
丙酮环戊酮环己酮2.5×10-4%
48×10-4%
2.5×10-2%
第五页,共三十五页,2022年,8月28日库尔特-迈依尔测定法简介:
在丙酮的稀的溶液中,加入过量的溴,实验发现,溴化速度与丙酮浓度成正比,和溴无关。因而,证明了溴化反应是通过丙酮的烯醇式加成后消除得到α-溴丙酮
历程:
由于第一步是慢反应,因而测定α-溴代丙酮的生成速度即为烯醇式互变异构速度。
第六页,共三十五页,2022年,8月28日一、分子结构对烯醇式含量的影响
表:酮式体系中,烯酮的平衡百分含量
化合物
烯醇的含量,%
第七页,共三十五页,2022年,8月28日
化合物
烯醇的含量,%
第八页,共三十五页,2022年,8月28日
化合物
烯醇的含量,%
第九页,共三十五页,2022年,8月28日
化合物
烯醇的含量,%
从上表分析得出以下结论:1、平衡状态下,丙酮以及其它简单酮几乎全部以酮式存在,如丙酮、环戊、环己酮等。
第十页,共三十五页,2022年,8月28日2、在表A部分中,当丙酮中H被羧乙酯(-COOEt)取代时,含量增加;若被乙酰基取代,增加的幅度更大(表B部分)。
a、羧乙酯基或乙酰基的吸电子效应,使α-碳上氢酸性增强,有利于烯醇式平衡产物的生成,
b、β二酮及β-二酯类的烯醇式烯醇是由于形成分子内氢键及碳碳双键与碳基共轭而稳定。
3、在C、D、E、F的数据表明,在体系中,烷基的存在,降低烯醇式的含量。因为R的+I效应。
4、在C和F数据表明,苯基存在有利于烯醇式的生成:由于烯醇和苯环产生了大共轭体系的原故
5、较大环烯醇含量较高,原因不明。
第十一页,共三十五页,2022年,8月28日二、溶剂对烯醇式的影响
极性溶剂有利于酮式存在,非极性溶剂有利于烯醇式存在。原因为烯醇式的极性比酮式极性小。因为在烯醇式结构中,存在分子内氢键,使正负电荷得到部分中和,而极性下降:
极性大
极性小,负氧被质子中和后,负性下降
第十二页,共三十五页,2022年,8月28日
表:乙酰乙酸乙酯在不同溶剂中烯醇含量(18℃)
溶剂烯醇(%)溶剂烯醇(%)水0.40丙酮7.325%甲醇0.83氯仿8.250%甲醇1.52硝基苯10.150%乙醇2.18乙酸乙酯12.9乙醇10.52苯16.2丙醇12.45乙醚27.1戊醇15.33二硫化碳32.4第十三页,共三十五页,2022年,8月28日三、烯醇形成的动力学和热力学比较
1、当羰基有不同的α-H时,可形成不同的烯醇式结构,但是若某一个α-碳上有吸电子基,则有利于此种烯醇式的形成:次要
主要
2、烯醇式混合物组分的动力学和热力学控制
动力学控制:产物的组成受到氢的相对活泼性控制。
主要次要第十四页,共三十五页,2022年,8月28日若在〔A〕和〔B〕之间可以建立平衡,即〔A〕、〔B〕可以相互转化,则建立了平衡控制,即热力学控制:第十五页,共三十五页,2022年,8月28日质子催化下的〔A〕、〔B〕之间的相互转化:
当有过量酮存在下,则是平衡控制产物动力学控制易生成取代较少的烯醇,而平衡控制则有利于生成取代基较多的产物;前者因为空间位阻少,后者由于生成的烯醇更稳定:第十六页,共三十五页,2022年,8月28日表:烯醇式混合物的组分
混合物
产物1产物2
动力学2872热力学
946
动力学1090
热力学
6634第十七页,共三十五页,2022年,8月28日动力学7525热力学
13
873、对于α、β-不饱和酮生成烯醇式,则主要生成共轭体系,即γ-碳上的氢被烯醇化:
(主要,稳定)
(次要,不稳定)
(主要)
第十八页,共三十五页,2022年,8月28日第四节、与酮-烯醇互变异构相关的互变异构
1、三碳系:
(双键位移)
2、硝基-酸式硝基系:3、亚硝基-肟系:
第十九页,共三十五页,2022年,8月28日4、酰胺-亚胺醇系:
5、腈-亚胺系:
6、亚胺-胺系:
第二十页,共三十五页,2022年,8月28日7、偶氮-腙系:
8、偶氮-胺系:
9、偶氮-亚硝基胺系:
第二十一页,共三十五页,2022年,8月28日一、三碳系(双键位移)
(98%,共轭)
(2%)
(86%,共轭)
(14%)
第二十二页,共三十五页,2022年,8月28日二、亚硝基-异亚硝基(肟)互变异构
在脂肪族亚硝基混合物中几乎全部是肟式结构,也就是说,脂肪醛和酮肟,不会转化为亚硝基混合物,但在芳香族混合物中,则是一个平衡体系:
光谱实验证明:固态时为醌式结构,而溶液时为两种异构体的平衡产物,但在这种互变异构体中,与烯醇式不同的是,平衡总是偏向于肟这一边。第二十三页,共三十五页,2022年,8月28日三、酰胺-亚胺醇互变异构
mp:
128℃mp:
123℃
在庚烷中得到的物质熔点为128℃的酰胺式;而在甲醇中得到是熔点为123℃的亚胺醇式结构。
例如:脲酸为2,6,8-三羟基嘌呤:
亚胺醇式
酰胺式
第二十四页,共三十五页,2022年,8月28日这类一个变化可以用来很好的解释一些反应的产物,如:
历程:
第二十五页,共三十五页,2022年,8月28日第五节、负离子移变
一、单分子历程:
历程:
例如:
第二十六页,共三十五页,2022年,8月28日例如:
例如:
对于1-苯基丙烯体系中,苯基的对位有甲基取代,迁移性能增加:
第二十七页,共三十五页,2022年,8月28日二、双分子历程
离去基团的离去和加成基团的加成同时进行,它们可以相同,也可以不同。如:
(唯一产物)
历程:
三、分子内历程
第二十八页,共三十五页,2022年,8月28日用取代丙烯醇和亚硫酰氯反应,也可以发生分子内负离子移变:
历程:
对于环状化合物来说,用SOCl2处理,除发生分子内移变外,顺反异构仍然保持:
第二十九页,共三十五页,2022年,8月28日历程:
第三十页,共三十五页,2022年,8月28日第六节、双重反应性能
长时间,人们认为双重反应是由于分子能产生双重的异构体而引起的,实际上,人们发现,双重反应性能比互变异构现象更为广泛。一般情况下,这是由于分子的共轭键所引起的:
对于烯醇钠盐来说有顺、反结构。由于体系中无质子存在(即过量的原料),顺反之间是不可相互转化的,也就是说,不能产生互变异构现象,即没有酮和烯醇式的互变异构。下列变化不会发生
:第三十一页,共三十五页,2022年,8月28日实验证明,顺反之间不能相互转化,即互变异构是不存在的,但是对这种钠盐进行羟基化或酰基化,却得到了两种产物,即C-衍生物和氧衍生物:
(碳衍生物)且顺、反构型保持不变。这就说明了双重反应性不一定是互变异构所导致的,再如:氯汞乙醛也有双重反应性能:
形成C或O衍生物与试剂的性质有关。结论:物质发生双重反应的根本原因不是平衡异构,而是共轭产生的极性的交替,因而,只有共轭键分子才有双重反应性,这种共轭含π-π共轭,P-π共轭。这种共轭存在,使得在外来试剂的影响下,π电子云重新分配,这就导致了双重反应性。第三十二页,共三十五页,2022年,8月28日存在两种产物的原因:有P-π共轭体系。即π34:
或存在共振结构:
第三十三页,共三十五页,2022年,8月28日例2:
例3:
π-π
温馨提示
- 1. 本站所有资源如无特殊说明,都需要本地电脑安装OFFICE2007和PDF阅读器。图纸软件为CAD,CAXA,PROE,UG,SolidWorks等.压缩文件请下载最新的WinRAR软件解压。
- 2. 本站的文档不包含任何第三方提供的附件图纸等,如果需要附件,请联系上传者。文件的所有权益归上传用户所有。
- 3. 本站RAR压缩包中若带图纸,网页内容里面会有图纸预览,若没有图纸预览就没有图纸。
- 4. 未经权益所有人同意不得将文件中的内容挪作商业或盈利用途。
- 5. 人人文库网仅提供信息存储空间,仅对用户上传内容的表现方式做保护处理,对用户上传分享的文档内容本身不做任何修改或编辑,并不能对任何下载内容负责。
- 6. 下载文件中如有侵权或不适当内容,请与我们联系,我们立即纠正。
- 7. 本站不保证下载资源的准确性、安全性和完整性, 同时也不承担用户因使用这些下载资源对自己和他人造成任何形式的伤害或损失。
最新文档
- 2025年度便利店员工劳务合同(健康生活支持计划)
- 2025年度智能家居安防版房屋租赁合同
- 科技在提升企业决策效率中的作用
- 遗忘曲线复习计划
- 事业编制人员聘用合同范本
- 公住房买卖合同范本
- 买石合同范本
- 2025-2030年中国锅炉鼓引风机项目投资可行性研究分析报告
- 企业抵押贷款合同范本
- 全脑课合同范本
- 2023-2024学年高中信息技术必修一沪科版(2019)第三单元项目六《 解决温标转换问题-认识程序和程序设计语言》教学设计
- 【湘教版】2024-2025学年七年级数学下册教学工作计划(及进度表)
- 《急性左心衰》课件
- 二零二五版洗煤厂与矿业公司合作洗煤业务合同3篇
- 上海市第一至十八届高一物理基础知识竞赛试题及答案
- 2024李娜一建管理讲义修订版
- 2024院感培训课件
- 护理试讲考核15分钟
- 2025天猫服饰春夏趋势白皮书
- 电力工程施工的重点和难点及保证措施
- 人教版七年级音乐教学计划

评论
0/150
提交评论