



版权说明:本文档由用户提供并上传,收益归属内容提供方,若内容存在侵权,请进行举报或认领
文档简介
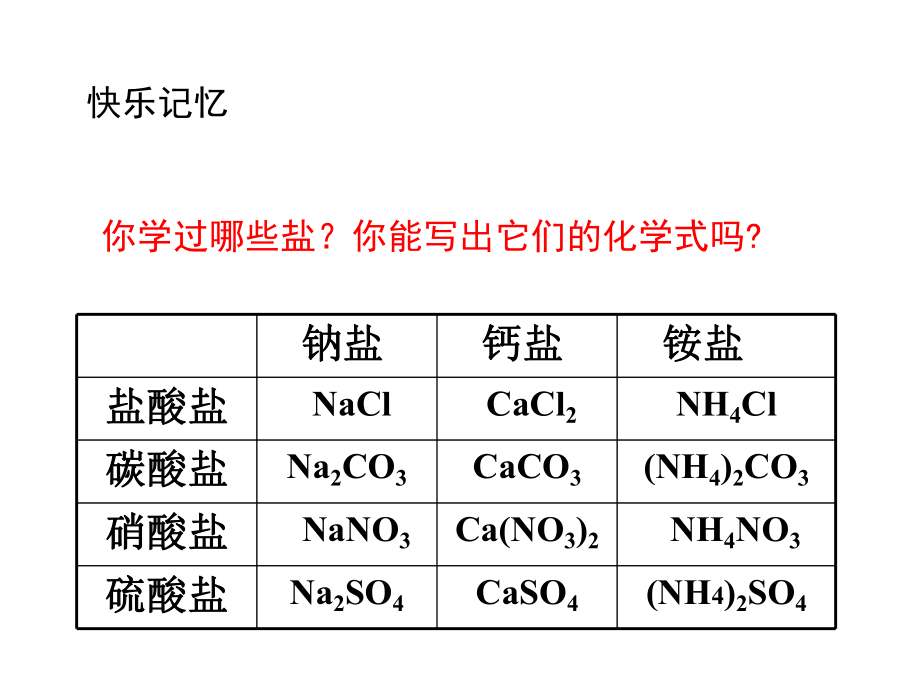
1、盐 化肥课题一生活中常见的盐原从水中来,不敢水中行,人人都要我,无我食不成。盐与食盐是否同一物质?猜猜我是谁?课堂导入不一定食盐是盐,盐不一定是食盐;盐是一类物质的总称。食盐(NH4)2SO4CaSO4Na2SO4硫酸盐硫酸盐 NH4NO3Ca(NO3)2 NaNO3硝酸盐硝酸盐(NH4)2CO3CaCO3Na2CO3碳酸盐碳酸盐NH4Cl CaCl2 NaCl盐酸盐盐酸盐 铵盐铵盐 钙盐钙盐 钠盐钠盐你学过哪些盐?你能写出它们的化学式吗?快乐记忆一、氯化钠(NaCl)俗称:食盐物理性质:白色晶体,易溶于水,水溶液有咸味 1、重要的调味品 2、人体正常生理不可缺少的物质 3、医疗 生理盐水是0
2、.9%的氯化钠溶液 4、农业 氯化钠可以用来选种 5、工业的原料:氯碱工业 6、日常生活中用来腌制食品 7、交通 公路上的积雪用氯化钠来消除融雪机撒盐融雪融雪机撒盐融雪氯化钠的用途一、氯化钠海水晒盐海水晒盐盐矿挖盐盐矿挖盐盐湖捞盐盐湖捞盐盐井水煮盐盐井水煮盐粗盐粗盐盐矿挖盐盐矿挖盐海水晒盐海水晒盐一、氯化钠粗盐粗盐精盐精盐溶解、沉淀、过滤、溶解、沉淀、过滤、蒸发、结晶蒸发、结晶你看到过粗盐在夏天“出汗”吗? 这是粗盐里含的杂质(CaCl2,MgCl2)吸收空气里的水分变潮的结果,纯净的食盐是不容易受潮风吹日晒,海水蒸发,溶剂的量减少,食盐晶体析出。海水晒盐的原理是什么?活动与探究实验步骤:实验
3、目的:除去粗盐中的不溶性杂质 溶解 过滤 蒸发 粗盐提纯烧杯、玻璃棒铁架台、漏斗、烧杯、玻璃棒铁架台、蒸发皿、酒精灯、玻璃棒活动与探究实验操作及注意事项溶解过滤蒸发玻璃棒: 搅拌, 加速溶解 玻璃棒: 引流,玻璃棒:搅拌, 防止液滴飞溅一贴、 两低、三靠出现较多固体时就停止加热 粗盐提纯活动与探究一、氯化钠社会实践 调查研究,你家使用食盐的情况是否合理? (1)你家使用的是否是加碘食盐?从食盐包装袋上可以获得哪些信息? (2)按一段时间统计计算,你家每人每天平均食用食盐约多少克?是否在合理的范围之内? (3)通过查阅资料或调查,了解食盐还有什么用途? (4)你自己还想了解有关食盐的那些问题?一
4、、氯化钠NaCl( MgCl2 CaCl2 )如何用化学方法除去NaCl中含有MgCl2、CaCl2 等可溶性杂质。过量的过量的NaOH过过 滤滤Mg(OH)2NaCl(NaOH CaCl2 )过量的过量的Na2CO3过过 滤滤CaCO3NaCl(NaOH Na2CO3 )适量稀盐酸适量稀盐酸NaCl溶液溶液蒸发蒸发结晶结晶NaCl晶体晶体课堂思考 名 称 主 要 用 途 碳酸钠苏打、纯碱用于生产玻璃、造纸、纺织、洗涤剂 碳酸氢钠小苏打发酵粉的主要成分、治疗胃酸过多的药剂 碳酸钙可作作补钙剂。石灰石、大理石作建筑材料、也用于实验室制取二氧化碳二、碳酸钠、碳酸氢钠和碳酸钙1)洁白纯净的碳酸钙岩石
5、叫汉白玉。2)因含杂质而有花纹的碳酸钙叫大理石。 3)质地致密的碳酸钙岩石叫石灰石。贝 壳 - - - 主 要 成 分CaCO3 二、碳酸钠、碳酸氢钠和碳酸钙 现有碳酸钠, 碳酸钙、 碳酸氢钠、 氯化钠、 盐酸,请用序号完成(1)人体胃液中存在帮助消化的液体是_(2)发酵粉的主要成分之一是_(3)日常生活中重要的调味品是_(4)天安门前华表的主要成份是_(5)广泛用于制造玻璃的原材料是_课堂练习请回忆实验室制取二氧化碳的化学方程式?生成的气体是如何检验的呢?盐酸滴到含CaCO3的建材上二、碳酸钠、碳酸氢钠和碳酸钙碳酸钠碳酸钠 盐盐酸酸 碳酸氢钠盐碳酸氢钠盐酸酸现现 象象分分 析析白色固体溶解,
6、放出使澄清石灰水变白色固体溶解,放出使澄清石灰水变浑浊的无色气体浑浊的无色气体碳酸钠(或碳酸氢钠)与盐酸反应碳酸钠(或碳酸氢钠)与盐酸反应生成了生成了CO2气体气体【实验111】 Na2CO3和NaHCO3能否与稀盐酸反应?如果能反应,请问它们又会生成什么物质?二、碳酸钠、碳酸氢钠和碳酸钙【总结】碳酸盐(即CO32- 、HCO3-)的检验方法实验操作实验现象实验结论向少量样品中加入稀盐酸,将产生的气体通入澄清石灰水。有无色气体生成,澄清石灰水变浑浊。该样品是碳酸盐。某同学往一无色溶液中滴加稀盐酸,发现生成一种无色气体,将生成的气体通入澄清石灰水,发现石灰水变浑浊,于是他得出了该溶液中含有碳酸根
7、离子,你认为他的结论正确么?为什么?课后思考二、碳酸钠、碳酸氢钠和碳酸钙不正确,因为还可能是碳酸根离子实验11-2 向盛有少量碳酸钠溶液的试管里滴入澄清的石灰水,观察现象。现象分析溶液变浑浊Na2CO3 + Ca(OH)2 = CaCO3+ 2NaOHNaOH的工业制取纯碱Na2CO3和熟石灰Ca(OH)2制取烧碱Na2CO3 + Ca(OH)2 = CaCO3+ 2NaOH由纯碱制烧碱由纯碱制烧碱纯碱纯碱烧碱烧碱二、碳酸钠、碳酸氢钠和碳酸钙二、碳酸钠、碳酸氢钠和碳酸钙复分解反应条件 生成物:生成水或沉淀或气体【 注:不溶于水的固体只能和酸反应,如:CuO、Cu(OH)2、CaCO3 】 (
8、AgCl、BaSO4和酸也不反应 ) 反应物:一般要溶于水总结:AB+CD AD+CB特点:双交换、价不变 两种化合物在反应时互相交换成分生成另外两种化合物的反应。复分解反应3. 生成沉淀酸酸 + 碳酸盐碳酸盐 新盐新盐 + H2O + CO2酸酸 + 碱碱 盐盐 + H2O酸 + 金属氧化物 盐 + H H2 2O O2. 生成气体(CO2)1. 生成H2OMg(OH)2、Cu(OH)2、Fe(OH)3 AgCl、BaSO4、CaCO3、BaCO3 H+ + OH- - H2O例: Ca2+ + CO32- - CaCO3 Mg2+ + OH- - Mg(OH)2 H+ + CO32- -
9、H2O + CO2生成H2O 、或 复分解反应的条件二、碳酸钠、碳酸氢钠和碳酸钙课后练习:1、 判断下列复分解反应能否发生,并写出可行的化学方程式。1. H2SO4 + CuO 2. Ba(OH)2 + H2SO43. Na2CO3 + HCl 4. H2SO4 + ZnCl25. Ca(OH)2 + K2CO36. HCl + AgNO3= CuSO4 + H2O= 2NaCl + H2O + CO22= 2KOH + CaCO3= AgCl + HNO3= BaSO4 + 2H2O生成H2O 、或 复分解反应的条件二、碳酸钠、碳酸氢钠和碳酸钙例: 下列各组离子,在溶液中能 大量共存的是(
10、) A. H+、Ba2+、SO42- -、NO3- - B. Ca2+、 H+、OH- -、NO3- - C. H+、Na+、Cl- -、SO42- - D. H+、 Na+、 Cl- -、CO32- -C在溶液中能大量共存:即不能发生反应,不能生成 H2O 、或 生成H2O 、或 复分解反应的条件( BaSO4)( H2O )( H2O + CO2)二、碳酸钠、碳酸氢钠和碳酸钙OH-NO3-Cl-SO42-CO32-H+溶、挥溶、挥溶、挥溶、挥溶溶溶、挥溶、挥NH4+溶、挥溶、挥溶溶溶溶溶溶溶溶K+溶溶溶溶溶溶溶溶溶溶Na+溶溶溶溶溶溶溶溶溶溶Ba2+溶溶溶溶溶溶不不不不Ca2+微微溶溶溶溶
11、微微不不Mg2+不不溶溶溶溶溶溶微微Al3+不不溶溶溶溶溶溶Mn2+不不溶溶溶溶溶溶不不Zn2+不不溶溶溶溶溶溶不不Fe2+不不溶溶溶溶溶溶不不Fe3+不不溶溶溶溶溶溶Cu2+不不溶溶溶溶溶溶Ag+溶溶不不微微不不说出酸、碱、盐的溶解性规律(20)制取Na2CO3 侯氏制碱法拓展视野 1942年我国科学家侯德榜发明了“侯氏制碱法” NaCl + NH3 + CO2 + H2O = NaHCO3+ NH4Cl 2NaHCO3 = Na2CO3 + H2O + CO2习题探究1.下列各种离子在溶液中能大量共存的( ) A. K+、 Cu2+、 NO3- - 、 OH- - B. Ca2+、 Ba2
12、+ 、 Cl- - 、 NO3- - C. Ca2+ 、 Cu2+、 CO32- -、 Cl- - D. Mg2+ 、 NO3- -、 OH- - 、 H+B2、下列各组离子,能大量共存且形成无色溶液的是( ) A. H+、Ag+、Cl- -、NO3- - B. Na+、Fe3+、Cl- -、NO3- - C. H+、Na+、Cl- -、CO32- - D. H+、Na+、Cl- -、NO3- -(黄色,能共存)(黄色,能共存)D习题探究3. 甲乙两个车间, 排放的澄清透明废水含 H+ Na+ Cu2+ Cl- OH- CO32- 甲车间含 3 种离子,呈碱性。则甲中含 。 乙中含 。Na+
13、OH- - CO32- -H+ Cu2+ Cl- - 习题探究4.只用酚酞试液,如何鉴别 稀盐酸、氯化钠、氢氧化钠三种无色溶液。第步NaOH和酚酞和酚酞混合液混合液剩余剩余液体液体第步能使红色消失的是稀盐酸;不能则是NaCl溶液。NaOH溶液溶液习题探究5. 向H2SO4和CuSO4的混合溶液中,不断滴加NaOH溶液,下图曲线正确的是( )NaOH溶液沉淀质量0(没有沉淀)NaOH溶液沉淀质量0NaOH溶液沉淀质量0NaOH溶液沉淀质量0A BC D习题探究5.向H2SO4和CuSO4的混合溶液中, 不断滴加NaOH溶液分析:2NaOH+ H2SO4 = Na2SO4 + 2H2O2NaOH+
14、 CuSO4 = Na2SO4 + Cu(OH)2NaOH溶液溶液H2SO4 CuSO4Cu(OH)2+ H2SO4 = CuSO4 + 2H2O生成的Cu(OH)2沉淀又溶解在过量的硫酸中【 注:只有NaOH将硫酸消耗完了,生成的Cu(OH)2才会随NaOH质量的增加而增加 】 答案为:习题探究D(2012聊城)某化学兴趣小组的同学对碳酸钙高温加热一段时间剩余固体的成分进行探究. 【提出问题】剩余固体成分是什么?【猜想与假设】剩余固体成分为:A.全部是碳酸钙 B.既有碳酸钙,也有氧化钙 C.全部是氧化钙【设计并完成实验】 【实验结论】该化学兴趣小组同学得出的结论:剩余固体成分与【猜想与假设】
15、中的_ (填“A”或“B”或“C”) 。 【交流与反思】实验操作产生的气体是_,如何检验是该气体_ _;剩余固体的成分若与C相符,则两步操作的实验现象_ _(填“”或“”或“”)不同.实验操作实验现象实验结论(1)取少量固体于试管中,加适量水振荡后静置,再滴几滴无色酚酞试液溶液变红说明固体成分中一定含有 (2)再取少量固体于另一试管中滴加过量稀盐酸 有气泡生成说明固体成分中一定含有氧化钙碳酸钙B BCOCO2 2COCO2 2 (2012济宁)甲乙丙丁四小组同学分别对实验废液中成分进行分析检测,结果见下表; 其中,检测结果合理的是() A甲组、乙组B丙组、丁组 C甲组、丙组D乙组、丁组检测小组
16、检测小组检测结果检测结果甲组甲组KClKCl、KNOKNO3 3、KOHKOH、HClHCl乙组乙组KClKCl、KNOKNO3 3、K K2 2COCO3 3、HClHCl丙组丙组KClKCl、KNOKNO3 3、K K2 2SOSO3 3、KOHKOH丁组丁组KClKCl、KNOKNO3 3、K K2 2COCO3 3、KOHKOHB B习题探究 (2012济宁)亚硝酸钠是工业用盐,因有咸味、外观酷似食盐而常被误食亚硝酸盐能致癌,因有良好的着色防腐作用,广泛用于肉类食品添加剂,但用量严格限制亚硝酸钠易溶于水,其水溶液呈碱性,暴露于空气中能与氧气反应生成硝酸钠加热至320以上或遇强酸则分解出红棕色有毒有刺激性的二氧化氮气体请根据信息回答: (1)亚硝酸钠的保存方式是 ,原因是 ; (2)试设计出两种区别亚硝酸钠和食盐的简单方案(简单叙述即可): 方案一: ; 方案二: 密封保存因为亚硝酸钠暴露于空气中能与氧气反应生成硝酸钠各取少量固体溶于水,滴加酚酞试液,溶液变红色的是亚硝酸钠的溶液,不变色的是氯化钠的溶液各取少量固体放于试管中,滴加稀盐酸,有红棕色气体出现的是亚硝酸钠,无现象的是氯化钠C (20
温馨提示
- 1. 本站所有资源如无特殊说明,都需要本地电脑安装OFFICE2007和PDF阅读器。图纸软件为CAD,CAXA,PROE,UG,SolidWorks等.压缩文件请下载最新的WinRAR软件解压。
- 2. 本站的文档不包含任何第三方提供的附件图纸等,如果需要附件,请联系上传者。文件的所有权益归上传用户所有。
- 3. 本站RAR压缩包中若带图纸,网页内容里面会有图纸预览,若没有图纸预览就没有图纸。
- 4. 未经权益所有人同意不得将文件中的内容挪作商业或盈利用途。
- 5. 人人文库网仅提供信息存储空间,仅对用户上传内容的表现方式做保护处理,对用户上传分享的文档内容本身不做任何修改或编辑,并不能对任何下载内容负责。
- 6. 下载文件中如有侵权或不适当内容,请与我们联系,我们立即纠正。
- 7. 本站不保证下载资源的准确性、安全性和完整性, 同时也不承担用户因使用这些下载资源对自己和他人造成任何形式的伤害或损失。
最新文档
- 时尚品牌创新策略-打造合作创新的品牌生态圈
- 2024年采购管理师考生必看试题及答案
- 微生物与疾病的关联性:试题及答案
- 个案分析2024年国际物流师试题与答案
- DB1302T 590-2024农村大集食品经营质量规范
- 深度剖析2024年SCMP试题及答案技巧
- 初一上册英语各单元知识点总结
- 初二科学下册知识点总结
- 染色体结构的特点试题及答案
- 2024年供应链管理师高效应对试题及答案
- 介入手术术中安全护理措施
- 高中语文整本书阅读教学研究
- 2024年苏州农业职业技术学院高职单招语文历年参考题库含答案解析
- 投资银行学第4版- 课件汇 马晓军 第1-4章 投资银行概述-上市公司再融资
- 2025年月度工作日历含农历节假日电子表格版
- 中国近现代史纲要心得体会
- 竣工结算审计服务投标方案(2024修订版)(技术方案)
- 2025年中考语文复习课件 模块三 语言综合运用
- 《年产2000吨果汁型茶饮料的生产工艺设计》4600字(论文)
- 中建落地式脚手架施工方案
- 基因检测销售培训

评论
0/150
提交评论