



版权说明:本文档由用户提供并上传,收益归属内容提供方,若内容存在侵权,请进行举报或认领
文档简介
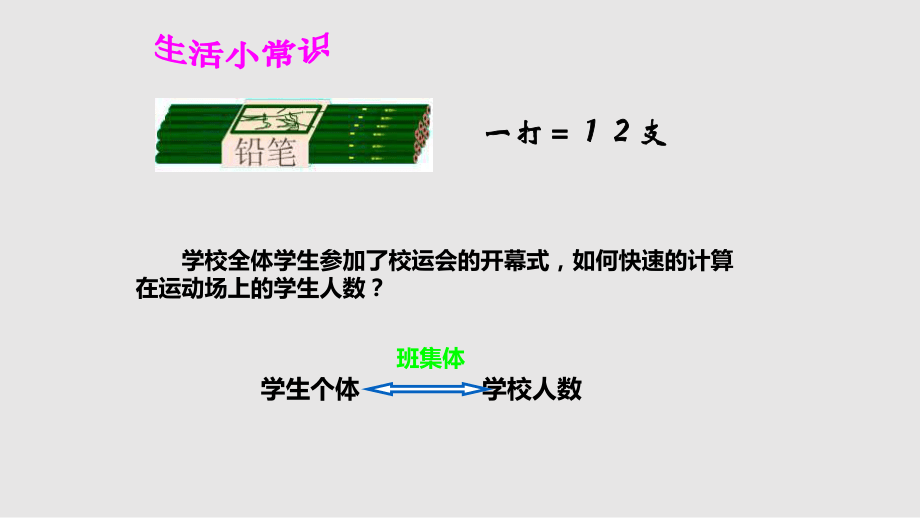
1、化学计量在实验化学计量在实验中的应用中的应用想一想?1.你知道古代曹冲称象的故事吗?曹冲在称象时的主导思想是什么? 化整为零,化大为小2.已知托盘天平的最小刻度为0.1克,你能用它称量一粒大米的质量吗?你的主导思想又是什么? 积小成大,聚微为宏一打支一打支学校全体学生参加了校运会的开幕式,如何快速的计算在运动场上的学生人数?学生个体 学校人数班集体你知道吗?你知道吗?个体数量大时,人们习惯以集体为单位统计个体数量。个体数量大时,人们习惯以集体为单位统计个体数量。微观粒子的数量很大,我们将以微观粒子的数量很大,我们将以集体集体为单位对其进行为单位对其进行计算计算(单位)(物理量) 摩尔物质的量一
2、、物质的量(一、物质的量(n) 表示含有一定数目粒子的集体的物理量 单位为摩尔(简称“摩”)(mol)如 H2SO4 的 物质的量 不能简化为 H2SO4的量 也不能写成 H2SO4的质量或 H2SO4的数量 物质的量是一个专有名词,由四个字组成 ,是一个 整体,不能分割,也不可加字、减字;粒子指微观可数的分子、原子、离子、电子、质子、中子等;粒子要指明,一般用化学式表示。注意物 理 量单 位 名 称单 位 符 号长 度质 量时 间电 流 强 度热力学温度发 光 强 度米千 克秒安 培开尔文坎德拉摩 尔mkgsAKcdmol 国际单位制(国际单位制(SISI)的七个基本物理量)的七个基本物理量
3、物 质 的 量 米:1791年法国决定把通过巴黎的地球子午线从赤道到北极的长度的1/千万规定为一米。后来根据测量结果把这个长度用铂铱合金制成了标准米原器,保存在巴黎国际计量局。1983年第17届国际计量大会决定用光速定米,规定1米等于光在真空中于1/2 9979 2458秒时间间隔内所经路径的长度。 千克:国际千克原器的质量为1kg。国际千克原器是1889年第一届国际计量大会批准制造的。它是一个高度和直径均为39mm用铂铱合金制成的圆柱体。原形保存在巴黎国际计量局。思考:1mol到底有多大,其衡量基准是什么?生平简介 意大利化学家。1776年8月9日生于都灵市一个律师家庭,1856年7月9日卒
4、于都灵市。1792年进都灵大学法律系学习,取得法学博士学位后,曾开业当律师。1800年弃法从理,十分勤奋,1820年被聘任都灵大学理科教授。自 18年被选为都灵科学院院士后,还担任过意大利教育委员和度量衡学会会长国际规定:1mol任何粒子集体都含有阿伏加德罗常数(NA)的值个微粒。国际规定:0.012kg 12C所含有的碳原子数即阿伏加德罗常数,约6.026.0210102323个 即 NA6.021023mol-1注意不能认为 6.021023就是阿伏加德罗常数也不能认为1mol粒子=6.021023个国际规定:1mol任何粒子集体都含有阿伏加德罗常数(NA)的值个微粒。判断判断 下面叙述是
5、否正确(A)每摩尔物质含有 6.021023个微粒(B)摩尔是七个基本物理量之一(C)摩尔是物质的质量单位(D)1摩尔的大米约含有 6.021023个米粒填空填空(1)1 mol 碳原子含有约 个碳原子 1 6.021023(2)0.3 mol 硫酸分子含有约 个硫酸分子 0.36.021023(3)10 mol 钠离子含有约 个钠离子 106.021023物质的量表示微粒的集体,可以用分数或小数表示。物质的量 (n) = 物质所含微粒数目 (N)阿伏加德罗常数 (NA)讨论讨论 1 molH2O中氢原子、 氧原子的物质的量为多少? H2O 11 molNA2HO212NANA1 mol2 m
6、ol 结论:微粒之间的个数之比也就是物质的量之比微粒个数微粒集团物质的量填空填空(4)1 mol Na2SO4含有 mol Na+ 2 mol SO42 1 个氧原子 0.5 mol Na2SO4含有 mol Na+ 1 mol SO42 0.5个氧原子约26.021023约46.021023填空填空(5)1 mol OH含有 mol 质子 有 个 电子 含有 5.4181023 个质子的 OH离子的物质的量约为 摩尔9 约106.021023(5.4181023) (96.021023) = 0.1 选择选择 0.1 mol KClO3 和 0.1 mol KClO 中所含微粒数相等的是 (
7、 ) (A) 钾离子 (B)氯离子(C) 氯原子 (D)氧原子 A C KClO3 = K + ClO3KClO = K + ClO知识链接知识链接微粒个数个个个物质的量 molmolmol微粒个数物质的量个个个molmolmol实验中,如何取出实验中,如何取出molmol或或molmol粒子、或更多物质的量的物质粒子、或更多物质的量的物质启示启示假如每颗米的质量都一样,现知道每万颗米的质量都为公斤那么要取万颗米时,你用数的还是用称的?请找出请找出1mol物质的质量有什么规律物质的质量有什么规律l一个分子或一个分子或原子的质量原子的质量2.6572.6571010-23-23g g4.4854
8、.4851010-23-23g g3.2943.2941010-24-24g g2.9902.9901010-23-23g g物质的量物质的量molmolmolmol相对分子或相对分子或原子质量原子质量mol物质物质的质量的质量gggg摩尔质量摩尔质量定义:单位:1 摩尔物质具有的质量。 用 M 表示克/摩符号:g/mol 或 g .mol1数值:等于该物质的式量。物质的量 (mol) 物质的质量 (g)摩尔质量 (g/mol)n = m M=例 1 90克水相当于多少摩水?解: 水的式量是18, 水的摩尔质量是 18g/mol 。n (H2O) = 90g18g/mol= 5 mol答:90
9、克水相当于5mol水。注意解题注意解题格式格式例 2 4. 9 克硫酸里含有多少个硫酸分子?解: 硫酸的式量是98,硫酸的摩尔质量是 98g/mol 。n (H2SO4) = 4. 9 g98g/mol= 0.05 mol答:4.9克硫酸里含有 (3.011022)个硫酸分子。N (H2SO4) = (0.05 mol) (6.021023)/mol= (3.011022)1 摩尔混合气体具有的质量叫做混合气体气的摩尔质量 。用 M 表示单位:克/摩g/mol 或 g .mol1混合气体的平均摩尔质量 (g/mol)混合气体的总质量 (g)混合气体的总物质的量 (mol) =特特别别提提示示小
10、试牛刀 标准状况下,有标准状况下,有O2和和CO2的组成混合气体的组成混合气体0.3mol,其质量为,其质量为11.4克,则混合克,则混合气体中氧气的质量分数为气体中氧气的质量分数为 。答案答案:42%小小 结结 通过物质的量把可称量的宏观物质与难以称量的微观粒子有机地联系起来。 物质的量微粒数 NA.NA.MM质量NA 阿伏加德罗常数 (6.021023/mol)M 摩尔质量 (g/mol)你知道吗?你知道吗?个体数量大时,人们习惯以集体为单位统计个体数量。个体数量大时,人们习惯以集体为单位统计个体数量。微观粒子的数量很大,我们将以微观粒子的数量很大,我们将以集体集体为单位对其进行为单位对其
11、进行计算计算(单位)(物理量) 摩尔物质的量一、物质的量(一、物质的量(n) 表示含有一定数目粒子的集体的物理量 单位为摩尔(简称“摩”)(mol)如 H2SO4 的 物质的量 不能简化为 H2SO4的量 也不能写成 H2SO4的质量或 H2SO4的数量 物质的量是一个专有名词,由四个字组成 ,是一个 整体,不能分割,也不可加字、减字;粒子指微观可数的分子、原子、离子、电子、质子、中子等;粒子要指明,一般用化学式表示。注意一、物质的量(一、物质的量(n) 表示含有一定数目粒子的集体的物理量 单位为摩尔(简称“摩”)(mol)如 H2SO4 的 物质的量 不能简化为 H2SO4的量 也不能写成 H2SO4的质量或 H2SO4的数量 物质的量是一个专有名词,由四个字组成 ,是一个 整体,不能分割,也不可加字、减字;粒子指微观可数的分子、原子、离子、电子、质子、中子等;粒子要指明,一般用化学式表示。注意填空填空(5)1 mol OH含有 mol 质子 有 个 电子 含有 5.4181023 个质子的 OH离子的物质的量约为 摩尔9 约106.021023(5.4181023) (96.021023) = 0.1 填空填空(5)1 mol OH含有 m
温馨提示
- 1. 本站所有资源如无特殊说明,都需要本地电脑安装OFFICE2007和PDF阅读器。图纸软件为CAD,CAXA,PROE,UG,SolidWorks等.压缩文件请下载最新的WinRAR软件解压。
- 2. 本站的文档不包含任何第三方提供的附件图纸等,如果需要附件,请联系上传者。文件的所有权益归上传用户所有。
- 3. 本站RAR压缩包中若带图纸,网页内容里面会有图纸预览,若没有图纸预览就没有图纸。
- 4. 未经权益所有人同意不得将文件中的内容挪作商业或盈利用途。
- 5. 人人文库网仅提供信息存储空间,仅对用户上传内容的表现方式做保护处理,对用户上传分享的文档内容本身不做任何修改或编辑,并不能对任何下载内容负责。
- 6. 下载文件中如有侵权或不适当内容,请与我们联系,我们立即纠正。
- 7. 本站不保证下载资源的准确性、安全性和完整性, 同时也不承担用户因使用这些下载资源对自己和他人造成任何形式的伤害或损失。
最新文档
- 店面解除合同范本
- 跨国企业商标使用权转让合同解析
- 购销菌菇类合同范本
- 垒墙拆墙合同范本
- 投资入股合同范本
- 安装电表劳务合同范本
- 受伤赔偿合同范例
- 主播拟合同范本
- 双方个人调解合同范例
- 临时用工解聘合同范例
- 抵押权优先受偿申请书
- 广东省2024年中考数学试卷【附真题答案】
- 紧急状态下使用开放杆救援乘客说明
- CJJT15-2011 城市道路公共交通站、场、厂工程设计规范
- 【课件】勃兰登堡协奏曲Ⅱ+课件高一上学期音乐人音版(2019)必修音乐鉴赏
- 挖掘机出厂检测报告
- 2024年四川长虹电子控股集团有限公司校园招聘考试试题必考题
- 钢芯铝绞线长度与重量
- clsim100-32药敏试验标准2023中文版
- (正式版)HGT 22820-2024 化工安全仪表系统工程设计规范
- 教科版(2017)科学五年下册《地球-宇宙的奇迹》说课(附反思、板书)课件

评论
0/150
提交评论