



版权说明:本文档由用户提供并上传,收益归属内容提供方,若内容存在侵权,请进行举报或认领
文档简介
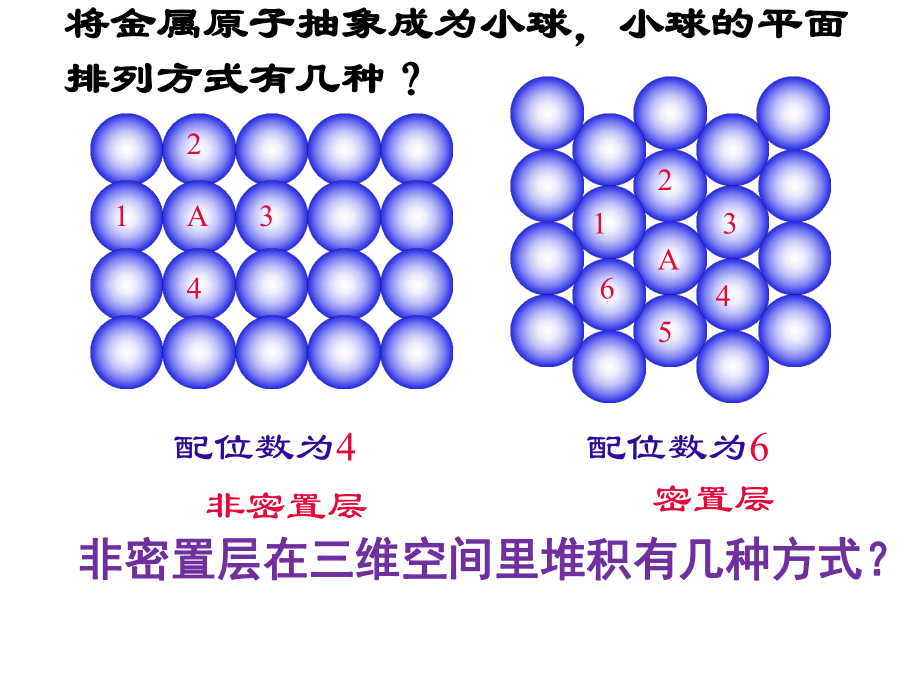
1、晶体的微观模型晶体的微观模型 以金属晶体中原子的堆积模型为例以金属晶体中原子的堆积模型为例将金属原子抽象成为小球,小球的平面将金属原子抽象成为小球,小球的平面排列方式有几种?排列方式有几种?非密置层A143213642A5密置层配位数为4配位数为6非密置层在三维空间里堆积有几种方式?非密置层在三维空间里堆积有几种方式?1 1、简单立方堆积:、简单立方堆积:非最紧密堆积,空间利用率低非最紧密堆积,空间利用率低配位数是配位数是 个。个。6金属晶体基本构型金属晶体基本构型:一、非最紧密堆积的两种构型一、非最紧密堆积的两种构型 1、空间利用率:指构成晶体的原子、离子或、空间利用率:指构成晶体的原子、离
2、子或分子在整个晶体空间中所占有的体积百分比。分子在整个晶体空间中所占有的体积百分比。 球体积球体积 空间利用率空间利用率 = 100% 晶胞体积晶胞体积空间利用率的计算空间利用率的计算(1)计算晶胞中的微粒数)计算晶胞中的微粒数2、空间利用率的计算步骤:、空间利用率的计算步骤:(2)计算晶胞的体积)计算晶胞的体积简单立方:在立方体顶点的微粒为简单立方:在立方体顶点的微粒为8个晶个晶胞共享,胞共享,空间利用率:空间利用率:(2r)(2r)3 34r4r3 3/3/3= 52.36%= 52.36%微粒数为:微粒数为:81/8 = 12 2、钾型、钾型( (体心立方堆积体心立方堆积) )( IAI
3、A碱金属,碱金属,VBVB,VIBVIB)每个晶胞含每个晶胞含 个原子,配位数为个原子,配位数为 ,空间利用空间利用率不高率不高许多金属(如许多金属(如NaNa、K K、FeFe等)等)采取这种堆积方式。采取这种堆积方式。1234567882( IA,VB,VIB)体心立方:在立方体顶点的微粒为体心立方:在立方体顶点的微粒为8个晶个晶胞共享,处于体心的金属原子全部属于该胞共享,处于体心的金属原子全部属于该晶胞。晶胞。1个晶胞所含微粒数为:个晶胞所含微粒数为:81/8 + 1 = 2请计算:空间利用率?请计算:空间利用率?二、金属晶体的两种最密堆积方式二、金属晶体的两种最密堆积方式镁型和铜镁型和
4、铜型(六方紧密堆积和面心立方堆积)型(六方紧密堆积和面心立方堆积)镁型(六方最密)镁型(六方最密)铜型(面心立方)铜型(面心立方)1、镁型、镁型六方密堆积六方密堆积(Be Mg B B B Be Mg B B B )123456123456123456ABABA1200找镁型的晶胞找镁型的晶胞配位数:配位数:空间占有率:空间占有率:每个晶胞含原子数:每个晶胞含原子数:12122 2四点间的夹角均为四点间的夹角均为6060六方密堆积(镁型)六方密堆积(镁型)的空间利用率计算:的空间利用率计算:在镁型堆积中取出六方晶胞,平行六面体的底是在镁型堆积中取出六方晶胞,平行六面体的底是平行四边形,各边长平
5、行四边形,各边长a=2r,则平行四边形的面积:,则平行四边形的面积: 平行六面体的高:平行六面体的高:22360sinaaaSaaah3623622的四面体高边长为先求先求S再求再求h)2(3423个球晶胞中有球rV%05.74%100晶胞球VV1234561234561234562、铜型、铜型 第三层的另一种排列方式,是将球第三层的另一种排列方式,是将球对准第一层的对准第一层的 2,4,6 位,不同于位,不同于 AB 两层的位置,这是两层的位置,这是 C 层。层。此种立方紧密堆积的前视图此种立方紧密堆积的前视图ABCAABC铜型铜型123456789101112属于最密置层堆集,配位数为属于
6、最密置层堆集,配位数为 ,这种堆积这种堆积晶胞空间利用率高,晶胞空间利用率高,许多金属(如许多金属(如Cu Ag AuCu Ag Au等)等)采取这种堆积方式。采取这种堆积方式。1212找铜型的晶胞找铜型的晶胞BCA面心立方(铜型)空间利用率计算:面心立方(铜型)空间利用率计算:在立方体顶点的微粒为在立方体顶点的微粒为8个晶胞共有,在面个晶胞共有,在面心的为心的为2个晶胞共有。个晶胞共有。属于属于1个晶胞微粒数为:个晶胞微粒数为:81/8 + 61/2 = 4 请计算:空间利用率?请计算:空间利用率?面心立方堆积方式的空间利用率计算面心立方堆积方式的空间利用率计算aa4R面心面心面心立方堆积方
7、式的空间利用率计算面心立方堆积方式的空间利用率计算aa4R面心面心面心立方空间利用率:面心立方空间利用率:属于属于1个晶胞微粒数为:个晶胞微粒数为:81/8 + 61/2 = 4 空间利用率:空间利用率:(2(21.414r)1.414r)3 34 44r4r3 3/3/3= 74.05%= 74.05%堆积方式堆积方式 晶胞类型晶胞类型空间利空间利用率用率配位数配位数实例实例面心立方面心立方最密堆积最密堆积堆积方式及性质小结堆积方式及性质小结简单立简单立方堆积方堆积体心立方体心立方密堆积密堆积六方最六方最密堆积密堆积面心立方面心立方六方六方体心立方体心立方简单立方简单立方74%74%68%5
8、2121286Cu、Ag、AuMg、Zn、TiNa、K、FePoa4R练练1:金属钨晶胞是一个立方体,在该晶胞金属钨晶胞是一个立方体,在该晶胞中每个顶角各有一个钨原子,中心有一个中每个顶角各有一个钨原子,中心有一个钨原子,实验测得金属钨原子的相对原子钨原子,实验测得金属钨原子的相对原子质量为质量为183.9,半径为半径为0.137nm0.137nm。求晶胞的边长;计算金属钨的密度。求晶胞的边长;计算金属钨的密度。晶胞中每个顶角各有一个钨原子,这个钨原子为晶胞中每个顶角各有一个钨原子,这个钨原子为8个晶胞个晶胞共用,每个钨原子有共用,每个钨原子有1/8属于该晶胞,体心有一个金属属于该晶胞,体心有
9、一个金属原子,那么,这个晶胞中含钨原子为原子,那么,这个晶胞中含钨原子为2 个,个,则则=2 2183.983.9/ /6.026.0210102323(0.316(0.3161010-7-7) )3 3=19.36g/cm=19.36g/cm3 3 钾型钾型体心立方晶胞体心立方晶胞金属钨的晶胞与已金属钨的晶胞与已经学过的哪种晶型经学过的哪种晶型类似?类似?1nm=10-9m=10-7cm复习复习1pm=10-12m现有甲、乙、丙、丁四种晶胞,可推知甲晶体中与的粒子个数比为;乙晶体 的化学式为 ;丙晶体的化学式为 ;丁晶体的化学式为。ABCDFEZXY Y1:1DC2或C2DEF或FEXY2Z
10、甲乙丙丁练练2:上图甲、乙、丙分别为体心堆积、面心立方堆积、上图甲、乙、丙分别为体心堆积、面心立方堆积、六方堆积的结构单元,则甲、乙、丙三种结构单六方堆积的结构单元,则甲、乙、丙三种结构单元中,金属原子个数比为元中,金属原子个数比为。甲甲 乙乙 丙丙1:2:3乙晶胞中所含金属原子数为乙晶胞中所含金属原子数为81/8+61/2=4晶胞中所含金属原子数为晶胞中所含金属原子数为121/6+21/2+3=6练练3: 1、已知金属铜为面心立方晶体,如图所示,、已知金属铜为面心立方晶体,如图所示,铜的相对原子质量为铜的相对原子质量为63.54,密度为,密度为8.936g/cm3,试求试求(1)图中正方形边
11、长)图中正方形边长 a,(2)铜的原子半径)铜的原子半径 RaRRorr课外练习aRR1、已知金属、已知金属铜铜为为面面心立方晶体,如图所心立方晶体,如图所示,铜的相对原子质量为示,铜的相对原子质量为63.54,密度为,密度为8.936g/cm3,试求,试求(1)图中正方形边长)图中正方形边长 a,(2)铜的原子半径)铜的原子半径 R晶胞中每个顶角各有晶胞中每个顶角各有1个铜原子,这个铜原子为个铜原子,这个铜原子为8个晶胞个晶胞共用,每个铜原子有共用,每个铜原子有1/8属于该晶胞,面心有属于该晶胞,面心有6个金属个金属原子,有原子,有1/6属于该晶胞,属于该晶胞,1个晶胞中含铜原子个晶胞中含铜原子4 个,个,则则= 4 463.543.54/ /6.026.0210102323(R(R1010-7-7) )3 3 =8.936g/cm=8.936g/cm3 31nm=10-9m=10-7cm复习复习1pm=10-12mR= nm1 1、某些金属晶体、某些金属晶体(Cu、Ag、Au)的原子的原子按面心立方的形式紧密堆积,即在晶体结按面心立方的形式紧密堆积,即在晶体结构中可以划出一块正立方体的结构单元,构中可以划出一块正立方体的结构单元,金属原子处于正立方体的八个顶点和六个金属原子处于正立方体的八个顶点和
温馨提示
- 1. 本站所有资源如无特殊说明,都需要本地电脑安装OFFICE2007和PDF阅读器。图纸软件为CAD,CAXA,PROE,UG,SolidWorks等.压缩文件请下载最新的WinRAR软件解压。
- 2. 本站的文档不包含任何第三方提供的附件图纸等,如果需要附件,请联系上传者。文件的所有权益归上传用户所有。
- 3. 本站RAR压缩包中若带图纸,网页内容里面会有图纸预览,若没有图纸预览就没有图纸。
- 4. 未经权益所有人同意不得将文件中的内容挪作商业或盈利用途。
- 5. 人人文库网仅提供信息存储空间,仅对用户上传内容的表现方式做保护处理,对用户上传分享的文档内容本身不做任何修改或编辑,并不能对任何下载内容负责。
- 6. 下载文件中如有侵权或不适当内容,请与我们联系,我们立即纠正。
- 7. 本站不保证下载资源的准确性、安全性和完整性, 同时也不承担用户因使用这些下载资源对自己和他人造成任何形式的伤害或损失。
最新文档
- 茭白收购合同范本
- 护士留学中介合同范本
- 工资欠条协议合同范本
- 单位院子维修合同范本
- 人车出租合同范本
- 还款合同协议书(2025年版)
- 停薪留职合同样本二零二五年
- 施工班组承包合同
- 最高额抵押合同范例
- 个体工商户雇工劳动合同样书二零二五年
- 2025年AR眼镜行业市场规模及主要企业市占率分析报告
- 日常小学生防性侵安全教育课件
- 浙江首考2025年1月普通高等学校招生全国统一考试 历史 含解析
- 市政城市环境管理
- 2025办公楼租赁合同书范本
- 16J914-1 公用建筑卫生间
- 教学课件:《新时代新征程》
- 信息技术2.0微能力:小学五年级道德与法治上(第四单元) 民族瑰宝-中小学作业设计大赛获奖优秀作品模板-《义务教育道德与法治课程标准(2022年版)》
- 全球松子分析预测报告
- 英国FBA超重标签
- 环境艺术与室内设计专业室内设计手绘表现技法教学课件(图文)

评论
0/150
提交评论