



版权说明:本文档由用户提供并上传,收益归属内容提供方,若内容存在侵权,请进行举报或认领
文档简介
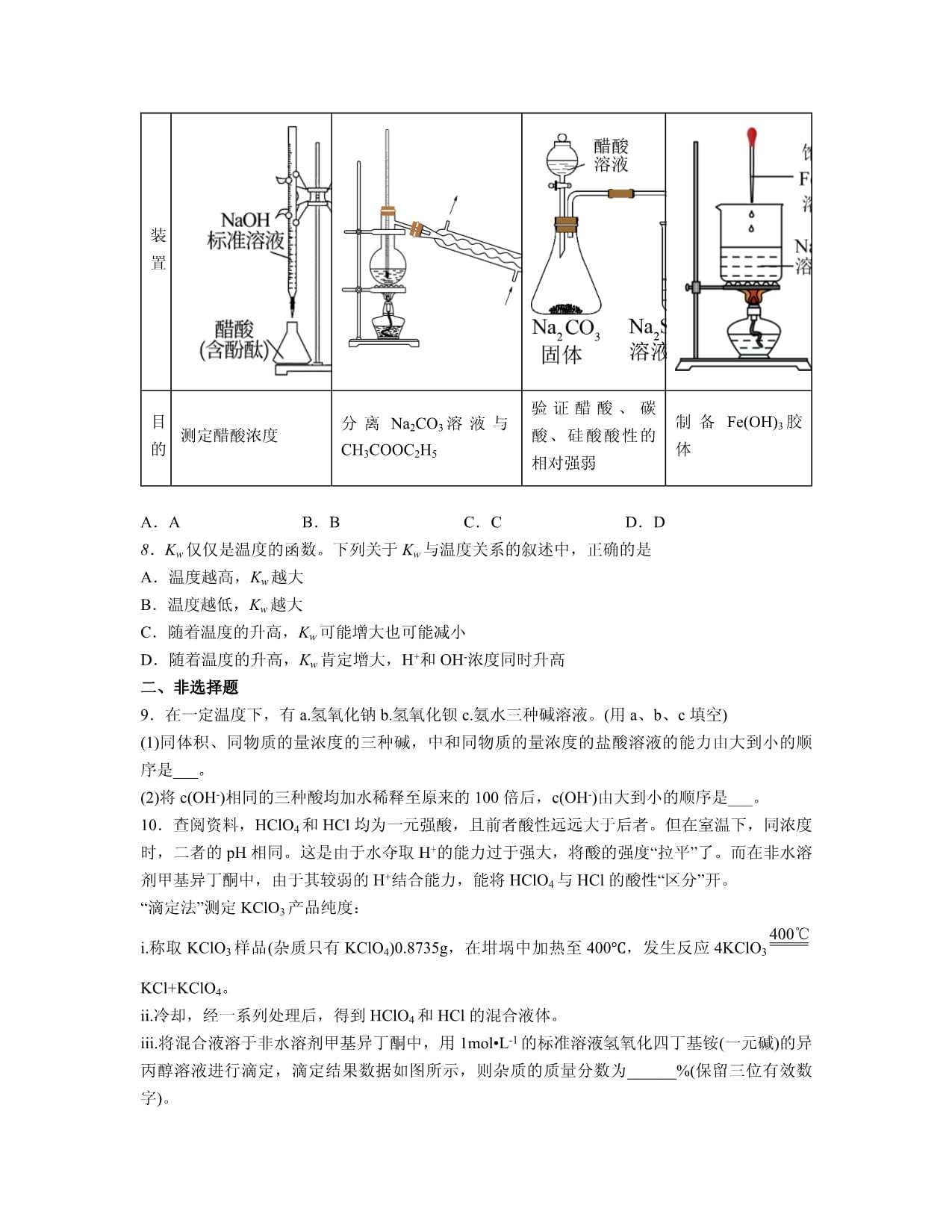
3.2水的电离和溶液的PH同步练习题一、选择题1.下列物质中属于电解质,且促进水的电离的是A.Cu B.溶液 C. D.HCl2.用标准NaOH溶液滴定未知浓度的盐酸,若测定结果偏低,则原因可能是A.用滴定管量取标准液时,先俯视后仰视B.锥形瓶洗净后瓶内残留有少量蒸馏水C.滴定到终点读数时,发现滴定管尖嘴处悬挂了一滴溶液D.配制标准溶液的固体NaOH中混有Na2O杂质3.下列说法正确的是A.在任何条件下,纯水的pH=7B.pH=6的溶液一定显酸性C.c(H+)<c(OH-)的溶液一定显碱性D.c(OH-)=1×10-6mol/L的溶液一定显酸性4.下列溶液中肯定为酸性的是A.含的溶液 B.的溶液C.的溶液 D.能和NaOH发生反应的溶液5.用盐酸来滴定未知浓度的氢氧化钠溶液,用甲基橙作指示剂,达到终点时,溶液颜色的变化是A.从黄色→橙色 B.从橙色→黄色 C.从红色→橙色 D.从橙色→红色6.常温下,将溶液与溶液等体积混合(忽略溶液体积变化)进行反应,恢复室温后溶液的为A.2 B.5 C.9 D.127.下列装置能达到实验目的的是选项装置目的测定醋酸浓度分离Na2CO3溶液与CH3COOC2H5验证醋酸、碳酸、硅酸酸性的相对强弱制备Fe(OH)3胶体A.A B.B C.C D.D8.Kw仅仅是温度的函数。下列关于Kw与温度关系的叙述中,正确的是A.温度越高,Kw越大B.温度越低,Kw越大C.随着温度的升高,Kw可能增大也可能减小D.随着温度的升高,Kw肯定增大,H+和OH-浓度同时升高二、非选择题9.在一定温度下,有a.氢氧化钠b.氢氧化钡c.氨水三种碱溶液。(用a、b、c填空)(1)同体积、同物质的量浓度的三种碱,中和同物质的量浓度的盐酸溶液的能力由大到小的顺序是___。(2)将c(OH-)相同的三种酸均加水稀释至原来的100倍后,c(OH-)由大到小的顺序是___。10.查阅资料,HClO4和HCl均为一元强酸,且前者酸性远远大于后者。但在室温下,同浓度时,二者的pH相同。这是由于水夺取H+的能力过于强大,将酸的强度“拉平”了。而在非水溶剂甲基异丁酮中,由于其较弱的H+结合能力,能将HClO4与HCl的酸性“区分”开。“滴定法”测定KClO3产品纯度:i.称取KClO3样品(杂质只有KClO4)0.8735g,在坩埚中加热至400℃,发生反应4KClO3KCl+KClO4。ii.冷却,经一系列处理后,得到HClO4和HCl的混合液体。iii.将混合液溶于非水溶剂甲基异丁酮中,用1mol•L-1的标准溶液氢氧化四丁基铵(一元碱)的异丙醇溶液进行滴定,滴定结果数据如图所示,则杂质的质量分数为______%(保留三位有效数字)。【参考答案】一、选择题1.C解析:A.铜是单质,既不是电解质也不是非电解质,A错误;B.溶液是混合物,既不是电解质也不是非电解质,B错误;C.是电解质,铵根离子水解促进水的电离,C正确;D.HCl是电解质,是强酸,抑制水的电离,D错误;故选C。2.D【分析】根据c(酸)=判断不当操作对相关物理量的影响。解析:A.仰视使读数偏大,俯视读数偏小,先仰视后俯视,量取的标准液体积偏大,则测定结果偏高,故A错误;B.锥形瓶洗净后瓶内残留有少量蒸馏水,盛装的是位置浓度的盐酸,操作正确,对测定结果不产生影响,故B错误;C.滴定到终点读数时,发现滴定管尖嘴处悬挂了一滴溶液,占了标准液体积但未参加反应,所以NaOH溶液体积偏大,使测定结果偏高,故C错误;D.配制标准溶液的固体NaOH中混有Na2O杂质,Na2O与水反应生成NaOH,使NaOH浓度增大,消耗的体积少,则使测定浓度偏小,故D正确;故答案选D。3.C解析:A.若为常温下,pH=7的溶液显中性,但温度未知,不能确定酸碱性,故A错误;B.100℃时pH=6的溶液显中性,故B错误;C.由c(H+)<c(OH−)可知,溶液一定显碱性,故C正确;D.c(OH−)=1×10−6mol/L的溶液,不能确定与氢离子浓度关系,不能确定酸碱性,故D错误;故选C。4.C【分析】溶液呈酸碱性的实质是c(H+)与c(OH-)的相对大小,不能只看pH,一定温度下pH=6的溶液也可能显中性,也可能显酸性,应注意温度。另外,要注意区分溶液组成和性质的关系,酸性溶液不一定是酸溶液,碱性溶液不一定是碱溶液。解析:A.水溶液中存在水的电离,一定含有氢离子,与溶液酸碱性无关,A项错误;B.如100℃时,水的离子积常数是10-12,当pH=6时溶液呈中性,B项错误;C.c(OH-)<c(H+)的溶液一定呈酸性,C项正确;D.能和NaOH发生反应的溶液不一定呈酸性,比如碳酸氢钠溶液呈碱性,碳酸氢根却可以和氢氧根反应生成水和碳酸根,D错误;故选C。5.A解析:甲基橙的变色范围为3.1-4.4,碱性时显黄色,变色范围为橙色,强酸性时显红色;故选A。6.D解析:设两溶液的体积均为,,,,,即,D项符合题意。7.A解析:A.用标准氢氧化钠溶液滴定一定体积未知浓度的醋酸,且需用酚酞作指示剂,根据消耗标准碱的体积可计算确定醋酸的浓度,故A正确;B.Na2CO3溶液与CH3COOC2H5互不相溶,应用分液法分离,故B错误;C.醋酸具有挥发性,挥发出的醋酸也会进入硅酸钠中反应生成硅酸,不能确定是二氧化碳的反应,故C错误;D.氢氧化铁胶体制备应将饱和氯化铁滴入沸水中,不能直接滴入氢氧化钠溶液中,故D错误;故选:A。8.A解析:A.Kw是水的离子积,水电离过程是吸热过程,温度越高,Kw越大,A项正确;B.Kw是水的离子积,水电离过程是吸热过程,温度越低,Kw越小,B项错误;C.Kw是水的离子积,水电离过程是吸热过程,温度越高,Kw越大,C项错误;D.随着温度的升高,Kw肯定增大,水电离出的H+和OH-浓度同时升高,若是溶解度随温度降低的酸溶液或碱溶液,温度升高,饱和溶液中H+和OH-浓度不是同时升高,D项错误;故答案选A。二、非选择题9.b>a=cc>a=b解析:同体积、同物质的量浓度的三种碱,二元碱消耗的盐酸比一元碱多,所以氢氧化钡消耗的盐酸最多,氢氧化钠与氨水消耗的盐酸相同,则中和同物质的量浓度的盐酸溶液的能力由大到小的顺序是,故答案为:;一水合氨是弱电解质,加水稀释能促进一水合氨的电离,所以氨水中氢氧根离子浓度变化小,即氨水中氢氧根离子浓度大,所以将相同的
温馨提示
- 1. 本站所有资源如无特殊说明,都需要本地电脑安装OFFICE2007和PDF阅读器。图纸软件为CAD,CAXA,PROE,UG,SolidWorks等.压缩文件请下载最新的WinRAR软件解压。
- 2. 本站的文档不包含任何第三方提供的附件图纸等,如果需要附件,请联系上传者。文件的所有权益归上传用户所有。
- 3. 本站RAR压缩包中若带图纸,网页内容里面会有图纸预览,若没有图纸预览就没有图纸。
- 4. 未经权益所有人同意不得将文件中的内容挪作商业或盈利用途。
- 5. 人人文库网仅提供信息存储空间,仅对用户上传内容的表现方式做保护处理,对用户上传分享的文档内容本身不做任何修改或编辑,并不能对任何下载内容负责。
- 6. 下载文件中如有侵权或不适当内容,请与我们联系,我们立即纠正。
- 7. 本站不保证下载资源的准确性、安全性和完整性, 同时也不承担用户因使用这些下载资源对自己和他人造成任何形式的伤害或损失。
最新文档
- 大型体育赛事医疗救援流程优化
- 2025-2030中国有机食品行业市场发展趋势与前景展望战略研究报告
- 2025-2030中国有机美容产品行业市场现状供需分析及投资评估规划分析研究报告
- 2025-2030中国有机椰子奶油市场消费趋势与营销渠道战略规划研究报告
- 2025-2030中国有机乳制品行业市场发展趋势与前景展望战略研究报告
- 2025-2030中国智能睡眠跟踪装置行业市场发展趋势与前景展望战略研究报告
- 2025-2030中国智能浴室柜市场发展现状调研及市场前景研究报告
- 2025-2030中国智能手机行业市场发展分析及发展前景与投资研究报告
- 2025-2030中国智慧门诊行业经营管理风险及发展趋势预判研究报告
- 2025-2030中国智慧屏行业运营现状及未来经营效益建议研究报告
- mil-std-1916抽样标准(中文版)
- 支气管镜麻醉
- 2024年LED手电筒行业技术趋势分析
- 医疗器械经营与药品经营的区别
- 钢丝绳吊装时最大允许吊装重物对应表
- 专题四“挺膺担当”主题团课
- 设计报价单模板
- 钦州卓达生物能源有限公司年产1500吨木炭项目环境影响报告表
- 汽车修理厂维修结算清单
- DB43-T+2181-2021学校治安反恐防范要求
- 内河船舶安全检查

评论
0/150
提交评论