



版权说明:本文档由用户提供并上传,收益归属内容提供方,若内容存在侵权,请进行举报或认领
文档简介
1、- PAGE 6 -基本概念练习(一)1.两种盐的固体混合物:加热时有气体产生,加水溶解时有沉淀生成,且沉淀溶于稀盐酸。满足上述条件的混合物是A . BaCl2和(NH4)2S03 B . AgNO3和NH4Cl CFeCl3和NaHCO3 D. KCl和Na2CO32.下列说法中正确的是A医用酒精的浓度通常为95%B单质硅是将太阳能转化为电能的常用材料C淀粉、纤维素和油脂都属于天然高分子化合物D合成纤维和光导纤维都是新型无机非金属材料3.下列有关化学用语能确定为丙烯的是4.高炉炼铁过程中既被氧化又被还原的元素是A铁 B氮 C氧 D碳5.下列化合物中,在常温常压下以液态形式存在的是A.甲醇 B
2、. 乙炔 C. 丙烯 D. 丁烷6.磷钨酸H3PW12O40等杂多酸可代替浓硫酸用于乙酸乙酯的制备。下列说法不正确的是AH3PW12O40在该酯化反应中其催化作用B杂多酸盐Na2HPW12O40与Na3PW12O40都是强电解质CH3PW12O40、KH2PW12O40与Na3PW12O40中都有相同的原子团D硅钨酸H4 SiW12O40也是一种杂多酸,其中W的化合价为+87.下列化合物的分子中,所有原子都处于同一平面的有A.乙烷 B. 甲苯 C. 氟苯 D. 四氯乙烯8.“碳捕捉技术”是指通过一定的方法将工业生产中产生的CO2分离出来并利用。如可利用NaOH溶液来“捕捉”CO2,其基本过程如
3、下图所示(部分条件及物质未标出)。下列有关该方法的叙述中正确的是A.能耗大是该方法的一大缺点B.整个过程中,只有一种物质可以循环利用C.“反应分离”环节中,分离物质的基本操作是蒸发结晶。过滤D.该方法可减少碳排放,捕捉到的CO2还可用来制备甲醇等产品9.某反应的H=+100kJmol-1,下列有关该反应的叙述正确的是A.正反应活化能小于100kJmol-1B.逆反应活化能一定小于100kJmol-1C.正反应活化能不小于100kJmol-1D.正反应活化能比逆反应活化能大100kJmol-110.Al、Fe、Cu都是重要的金属元素。下列说法正确的是A.三者对应的氧化物均为碱性氧化物B.三者的单
4、质放置在空气中均只生成氧化物C.制备AlCl3、FeCl3、CuCl2均不能采用将溶液直接蒸干的方法D.电解AlCl3、FeCl3、CuCl2的混合溶液时阴极上依次析出Al、Fe、Cu11.下列说法不正确的是A化学反应有新物质生成,并遵循质量守恒定律和能量守恒定律B原子吸收光谱仪可用于测定物质中的金属元素,红外光谱仪可用于测定化合物的官能团C分子间作用力比化学键弱得多,但它对物质熔点、沸点有较大影响,而对溶解度无影响D酶催化反应具有高效、专一、条件温和等特点,化学模拟生物酶对绿色化学、环境保护及节能减排具有重要意义12.下列说法中,不正确的是A使用可再生资源、用超临界二氧化碳替代有机溶剂、注重
5、原子的经济性、采用低能耗生产工艺等都是绿色化学的内容B拉瓦锡发现的质量守恒定律、阿伦尼乌斯创立的电离学说、波尔提出的氢原子模型都对化学学科的发展作出了重要的贡献C同位素示踪法是研究化学反应历程的手段之一D淀粉、纤维素、蔗糖、纤维二糖水解后的产物都是葡萄糖13.下列与化学反应能量变化相关的叙述正确的是A.生成物能量一定低于反应物总能量B.放热反应的反应速率总是大于吸热反应的反应速率C.应用盖斯定律,可计算某些难以直接测量的反应焓变D.同温同压下,H2(g)+Cl(g)2HCl(g)在光照和点燃条件下的H不同14.下列推断正确的是A.SiO2是酸性氧化物,能与NaOH溶液反应B.Na2O、Na2O
6、2组成元素相同,与CO2反应产物也相同C.CO、NO、NO2都是大气污染气体,在空气中都能稳定存在D.新制氯水显酸性,向其中滴加少量紫色石蕊试液,充分震荡后溶液呈红色15.下表各选项中,不能利用置换反应通过Y得到W的一组化合物是ABCDYCO2Fe2O3C2H5OHFeCl3WMgOAl2O3C2H5ONaCuCl216.下列有关物质结构的表述正确的是A次氯酸的电子式 B二氧化硅的分子式SiO2C硫原子的最外层电子排布式3s23p4D钠离子的结构示意图17.下列判断正确的是A酸酐一定是氧化物B.晶体中一定存在化学键 C.碱性氧化物一定是金属氧化物D正四面体分子中键角一定是109O 2818.水
7、是最宝贵的资源之一。下列表述正确的是AH2O的电子式为 B4时,纯水的pH=7CD216O中,质量数之和是质子数之和的两倍D273K、101kPa,水分子间的平均距离d:d(气态)d(液态)d(固态)19.在相同条件下,下列说法错误的是A氯气在饱和食盐水中的溶解度小于在纯水中的溶解度B碘在碘化钾溶液中的溶解度大于在纯水中的溶解度C醋酸在醋酸钠溶液中电离的程度大于在纯水中电离的程度D工业上生产硫酸的过程中使用过量的空气可提高SO2的利用率20.下列热化学方程式或离子方程式中,正确的是:A、甲烷的标准燃烧热为-890.3kJmol-1,则甲烷燃烧的热化学方程式可表示为:CH4(g)+2O2(g)C
8、O2(g)2H2O(g) H=-890.3kJmol-1B.500、30MPa下,将0.5molN2和1.5mol H2置于密闭容器中充分反应生成NH3(g),放热19.3kJ,其热化学方程式为:N2(g)+3H2(g) 2NH3(g) H=-38.6kJmol-1C.氯化镁溶液与氨水反应:Mg2+2OHMg(OH)2D.氧化铝溶于NaOH溶液:Al2O3+2OH+3H2O2Al(OH)421.固硫剂是把煤燃烧时生成的二氧化硫以盐的形式固定在炉渣中的物质,可减少二氧化硫对大气的污染。下列物质中可用做固硫剂的有ACaO BNa2CO3 CNH4N03 D. P20522.正极材料为LiCoO2的
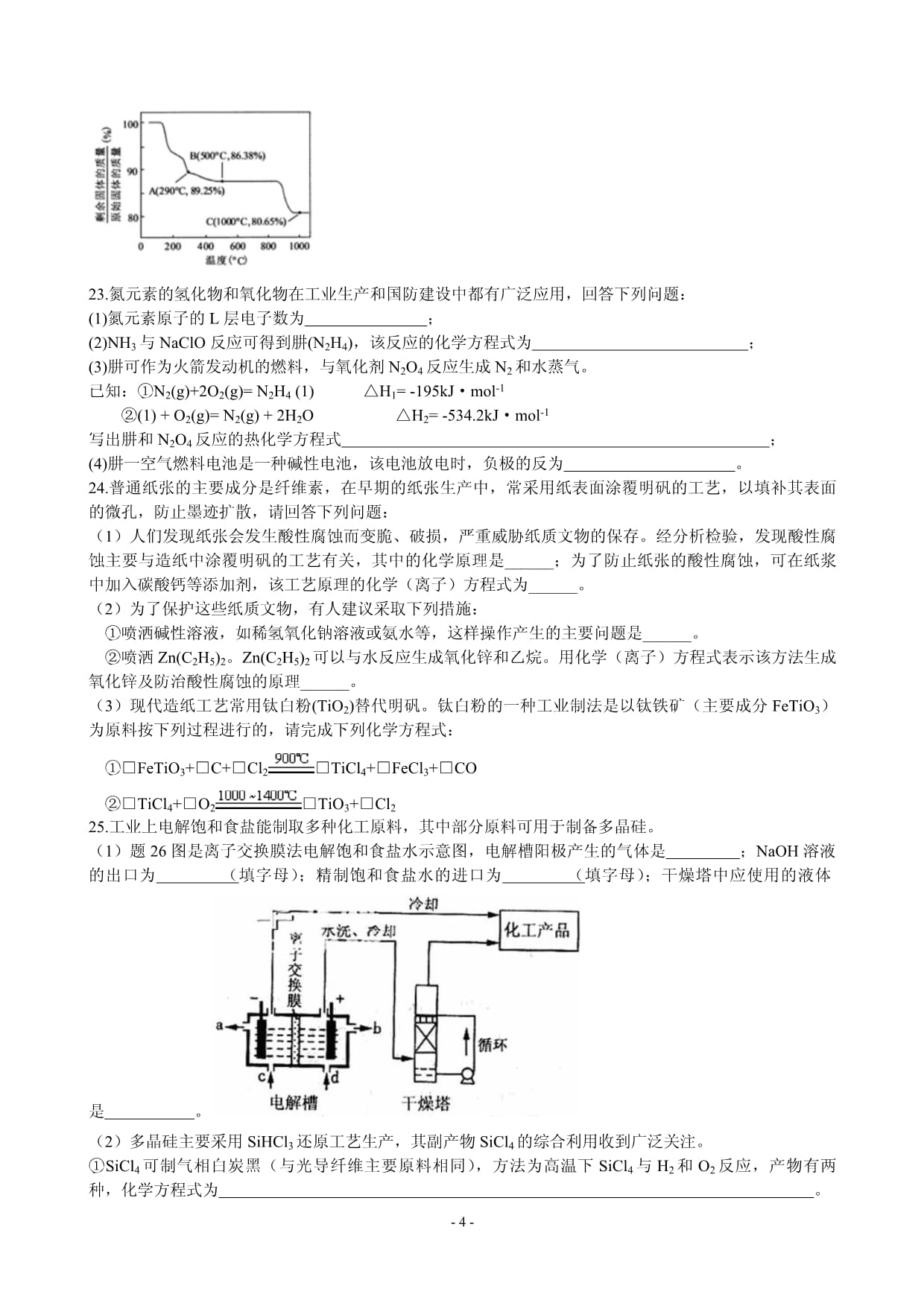
9、锂离子电池已被广泛用作便携式电源。但钴的资源匮乏限制了其进一步发展。(1)橄榄石型LiFePO4是一种潜在的锂离子电池正极材料,它可以通过(NH4)2Fe(SO4)2、H3PO4与LiOH溶液发生共沉淀反应,所得沉淀经80真空干燥、高温成型而制得。共沉淀反应投料时,不将(NH4)2Fe(SO4)2和LiOH溶液直接混合的原因是 。共沉淀反应的化学方程式为 。高温成型前,常向LiFePO4中加入少量活性炭黑,其作用除了可以改善成型后的LiFePO4的导电性能外,还能 。(2)废旧锂离子电池的正极材料试样(主要含有LiCoO2及少量AI、Fe等)可通过下列实验方法回收钴、锂。在上述溶解过程中,S2
10、O32被氧化成SO42,LiCoO2在溶解过程中反应的化学方程式为 。Co(OH)2在空气中加热时,固体残留率随温度的变化如右图所示。已知钴的氢氧化物加热至290时已完全脱水,则1000时,剩余固体的成分为 。(填化学式);在350400范围内,剩余固体的成分为 。(填化学式)。23.氮元素的氢化物和氧化物在工业生产和国防建设中都有广泛应用,回答下列问题: (1)氮元素原子的L层电子数为 ;(2)NH3与NaClO反应可得到肼(N2H4),该反应的化学方程式为 ; (3)肼可作为火箭发动机的燃料,与氧化剂N2O4反应生成N2和水蒸气。已知:N2(g)+2O2(g)= N2H4 (1)H1= -
11、195kJmol-1(1) + O2(g)= N2(g) + 2H2OH2= -534.2kJmol-1写出肼和N2O4反应的热化学方程式 ;(4)肼一空气燃料电池是一种碱性电池,该电池放电时,负极的反为 。24.普通纸张的主要成分是纤维素,在早期的纸张生产中,常采用纸表面涂覆明矾的工艺,以填补其表面的微孔,防止墨迹扩散,请回答下列问题:(1)人们发现纸张会发生酸性腐蚀而变脆、破损,严重威胁纸质文物的保存。经分析检验,发现酸性腐蚀主要与造纸中涂覆明矾的工艺有关,其中的化学原理是_;为了防止纸张的酸性腐蚀,可在纸浆中加入碳酸钙等添加剂,该工艺原理的化学(离子)方程式为_。(2)为了保护这些纸质文
12、物,有人建议采取下列措施:喷洒碱性溶液,如稀氢氧化钠溶液或氨水等,这样操作产生的主要问题是_。喷洒Zn(C2H5)2。Zn(C2H5)2可以与水反应生成氧化锌和乙烷。用化学(离子)方程式表示该方法生成氧化锌及防治酸性腐蚀的原理_。(3)现代造纸工艺常用钛白粉(TiO2)替代明矾。钛白粉的一种工业制法是以钛铁矿(主要成分FeTiO3)为原料按下列过程进行的,请完成下列化学方程式:FeTiO3+C+Cl2TiCl4+FeCl3+COTiCl4+O2TiO3+Cl225.工业上电解饱和食盐能制取多种化工原料,其中部分原料可用于制备多晶硅。(1)题26图是离子交换膜法电解饱和食盐水示意图,电解槽阳极产
13、生的气体是 ;NaOH溶液的出口为(填字母);精制饱和食盐水的进口为(填字母);干燥塔中应使用的液体是 。(2)多晶硅主要采用SiHCl3还原工艺生产,其副产物SiCl4的综合利用收到广泛关注。SiCl4可制气相白炭黑(与光导纤维主要原料相同),方法为高温下SiCl4与H2和O2反应,产物有两种,化学方程式为 。SiCl4可转化为SiHCl3而循环使用。一定条件下,在20L恒容密闭容器中的反应: 3 SiCl4(g)+2 H2(g)+Si(g)4 SiHCl3(g)达平衡后,H2与SiHCl3物质的量浓度分别为0.140mol/L和0.020mol/L,若H2全部来源于离子交换膜法的电解产物,
14、理论上需消耗纯NaCl的质量为 kg。(3)采用无膜电解槽电解饱和食盐水,可制取氯酸钠,同时生成氢气,现制得氯酸钠 213.0kg,则生成氢气 m3(标准状况)。26.请回答氯碱的如下问题:(1)氯气、烧碱是电解食盐水时按照固定的比率k(质量比)生成的产品。理论上k_(要求计算表达式和结果);(2)原料粗盐中常含有泥沙和Ca2、Mg2、Fe3、SO24等杂质,必须精制后才能供电解使用。精制时,粗盐溶于水过滤后,还要加入的试剂分别为Na2CO3、HCl(盐酸)BaCl2,这3种试剂添加的合理顺序是_(填序号)(3)氯碱工业是高耗能产业,一种将电解池与燃料电池相组合的新工艺可以节(电)能30以上。
15、在这种工艺设计中,相关物料的传输与转化关系如下图所示,其中的电极未标出,所用的离子膜都只允许阳离子通过。a%NaOH溶液 图中X、Y分别是_、_(填化学式),分析比较图示中氢氧化钠质量分数a与b的大小_;分别写出燃料电池B中正极、负极上发生的电极反应正极:_;负极:_;这样设计的主要节(电)能之处在于(写出2处)_、_。27.某工厂生产硼砂过程中产生的固体废料,主要含有MgCO3、MgSiO3、CaMg(CO3)2、Al2O3和Fe2O3等,回收其中镁的工艺流程如下:沉淀物Fe(OH)3Al(OH)3Mg(OH)2PH3.25.212.4部分阳离子以氢氧化物形式完全深沉时溶液的pH由见上表,请
16、回答下列问题:(1)“浸出”步骤中,为提高镁的浸出率,可采取的措施有 (要求写出两条)。(2)滤渣I的主要成分有 。(3)从滤渣中可回收利用的主要物质有 。(4)Mg(ClO3)2在农业上可用作脱叶剂、催熟剂,可采用复分解反应制备:MgCl2+2NaClO3=Mg(ClO3)2+2NaCl已知四种化合物的溶解度(S)随温度(T)变化曲线如下图所示:将反应物按化学反应方程式计量数比混合制备Mg(ClO3)2。简述可制备Mg(ClO3)2的原因: 。按中条件进行制备实验。在冷却降温析出Mg(ClO3)2过程中,常伴有NaCl析出,原因是: 。除去产品中该杂质的方法是: 。28.废旧印刷电路板的回收利用可实现资源再生,并减少污染。废旧印刷电路板经粉碎分离,能得到非金属粉末和金属粉末。(1)下列处理印刷电路板的回收利用可实现资源再生,并减污染。废旧印刷电路板经粉碎分离,能得到非金属粉末和金属粉末。A热裂解形成燃油B露天焚烧C作为有机复合建筑材料的原料D直接填埋(2)用H2O2和H2SO4的混合溶液可溶出印刷电路板金属粉末中的铜。已知:Cu(S)+2H+(aq)= Cu2+(aq)+H2(g)H=6439kJmol12H2O2(I)=2H2O(I)+O2(g)H=19646kJmol1H2(g)+O2(g)=H2O(I)H=28584kJmol1在H2SO4溶
温馨提示
- 1. 本站所有资源如无特殊说明,都需要本地电脑安装OFFICE2007和PDF阅读器。图纸软件为CAD,CAXA,PROE,UG,SolidWorks等.压缩文件请下载最新的WinRAR软件解压。
- 2. 本站的文档不包含任何第三方提供的附件图纸等,如果需要附件,请联系上传者。文件的所有权益归上传用户所有。
- 3. 本站RAR压缩包中若带图纸,网页内容里面会有图纸预览,若没有图纸预览就没有图纸。
- 4. 未经权益所有人同意不得将文件中的内容挪作商业或盈利用途。
- 5. 人人文库网仅提供信息存储空间,仅对用户上传内容的表现方式做保护处理,对用户上传分享的文档内容本身不做任何修改或编辑,并不能对任何下载内容负责。
- 6. 下载文件中如有侵权或不适当内容,请与我们联系,我们立即纠正。
- 7. 本站不保证下载资源的准确性、安全性和完整性, 同时也不承担用户因使用这些下载资源对自己和他人造成任何形式的伤害或损失。
最新文档
- 2024年度租赁期满后购买选择权的合同条款
- 2024年度企业间借款合同的还款来源保障3篇
- 2024年度大连市环保服务合同
- 2024经营合同股份有限公司合并合同范本
- 2024模具加工合同范文
- 2024年度保险经纪服务-合作协议
- 2024年度切削液市场开发与代理销售合同3篇
- 2024年度合作开发合同标的为新能源技术的协议3篇
- 聘请司机合同协议
- 公司法人之间的借款协议
- 血清转氨酶异常病因分析
- DB37T 4243-2020 单井地热资源储量评价技术规程
- PDCA提高护理管道标识规范率
- 世界未解之谜英文版
- 中小跨径公路桥梁设计课件
- 最新国家开放大学电大《课程与教学论》网络核心课形考网考作业及答案
- 放射培训考试习题及答案
- 硫磺制酸工艺
- 译林牛津版9A-Unit8-Detective-Stories-Reading-2公开课优质课件
- 邯郸市政府采购办事指南
- 浙江大学现代教学管理信息系统介绍

评论
0/150
提交评论