



版权说明:本文档由用户提供并上传,收益归属内容提供方,若内容存在侵权,请进行举报或认领
文档简介
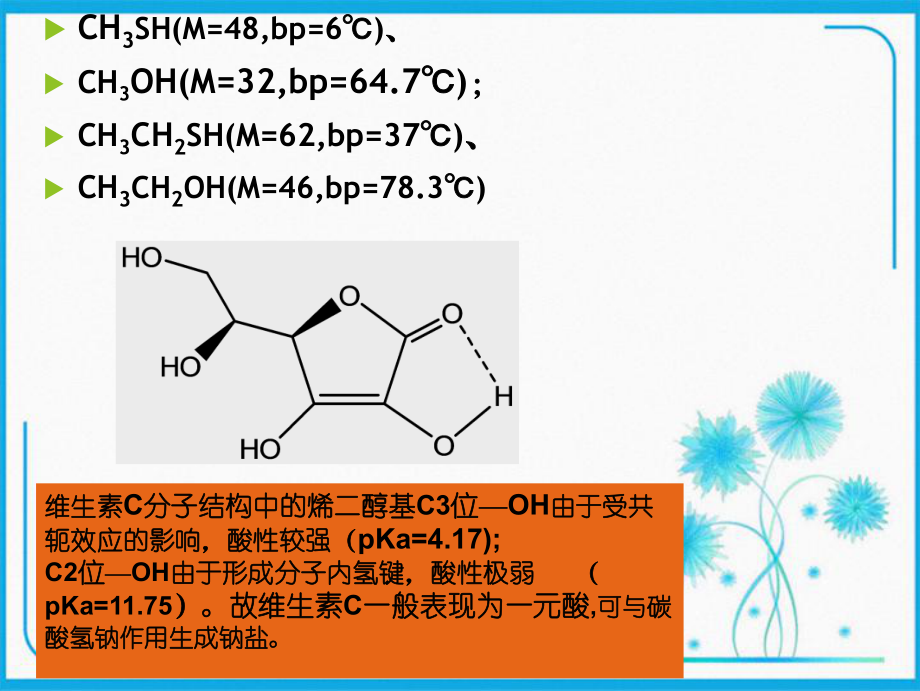
1、醇、酚、醚和羰基化合物化学竞赛 醇分子间能形成氢键,醚分子中不含醇分子间能形成氢键,醚分子中不含羟基分子间不能形成氢键,硫醇不能羟基分子间不能形成氢键,硫醇不能形成氢键,如:形成氢键,如:CH3SH(M=48,bp=6)、 CH3OH(M=32,bp=64.7); CH3CH2SH(M=62,bp=37)、CH3CH2OH(M=46,bp=78.3) 维生素维生素C分子结构中的烯二醇基分子结构中的烯二醇基C3位位OH由于受共由于受共轭效应的影响,酸性较强(轭效应的影响,酸性较强(pKa=4.17);C2位位OH由于形成分子内氢键,酸性极弱由于形成分子内氢键,酸性极弱 (pKa=11.75)。故
2、维生素)。故维生素C一般表现为一元酸一般表现为一元酸,可与碳可与碳酸氢钠作用生成钠盐。酸氢钠作用生成钠盐。对羟基苯甲醛的分子间氢键对羟基苯甲醛的分子间氢键邻羟基苯甲醛的分邻羟基苯甲醛的分子内氢键子内氢键BP: 196.5 BP: 246.6 对羟基苯甲醛的酸性大于苯酚对羟基苯甲醛的酸性大于苯酚邻羟基苯甲醛的酸性小于苯酚邻羟基苯甲醛的酸性小于苯酚分子中羟基越多形成的氢键越多,如:分子中羟基越多形成的氢键越多,如: Bp: 197 125 84 硫醇的酸性比醇强硫醇的酸性比醇强 CH3CH2SH:pka=10.5;CH3CH2OH:pka=17 1.制备:制备:(1) 烯烃的水合烯烃的水合 (B)
3、间接水合间接水合 (a)加硫酸(遵循马氏)加硫酸(遵循马氏) (A)(A)直接水合(遵循马氏)直接水合(遵循马氏) (b)硼氢化)硼氢化-氧化(反马氏)氧化(反马氏) (2)卤代烃的水解卤代烃的水解 (3)羰基化合物的还原羰基化合物的还原 醛酮的还原:醛酮的还原: 催化加氢催化加氢/Pd、Pt、Ni, NaBH4(不还原碳碳双键、碳碳叁键、氰不还原碳碳双键、碳碳叁键、氰基、硝基基、硝基),LiAlH4(不还原碳碳双键、碳(不还原碳碳双键、碳碳叁键)碳叁键) 羧酸、酯的还原:羧酸、酯的还原: 催化加氢/Pd、Pt、Ni LiAlH4 乙硼烷还原羧酸羧酸很难用催化氢化法还原,一般转化为酯再还原 (
4、4)格氏反应格氏反应 醛和酮与醛和酮与Grignard试剂(试剂(RMgX)发生加)发生加成反应,加成产物水解生成醇。成反应,加成产物水解生成醇。甲醛与RMgX反应用于合成伯醇;其它醛与RMgX反应用于合成仲醇; 酮与RMgX反应用于合成叔醇。酰卤、酯、酸酐与Grignard试剂(RMgX)发生加成-消去反应生成酮,进而再与RMgX反应生成叔醇。 低温酰卤、酸酐与RMgX反应可停留在酮阶段用于制备酮。腈与RMgX反应生成酮与活泼金属反应得到的醇金属盐一般用作强碱,与与活泼金属反应得到的醇金属盐一般用作强碱,与活性氢反应生成碳负离子作为亲核试剂进行取代或活性氢反应生成碳负离子作为亲核试剂进行取代
5、或加成反应。常用于酯加成反应。常用于酯-酯缩合,酮酯缩合,酮-酯缩合,迈克尔酯缩合,迈克尔加成等。加成等。 3 反应:反应: (1)与活泼金属的反应(与活泼金属的反应(Na、K、Al)对于氢活性较弱的可以用更强的碱,如对于氢活性较弱的可以用更强的碱,如氢化钠、氨基钠等氢化钠、氨基钠等.(2)与卤化氢的反应:与卤化氢的反应:Lucas试剂试剂 HX = HI, HBr, HCl 活性依次减弱。活性依次减弱。叔醇叔醇 仲醇仲醇 伯醇伯醇Lucas试剂(浓盐酸试剂(浓盐酸/无水氯化锌)无水氯化锌) (3) 与卤化磷和亚硫酰氯作用 (4)与无机酸成酯-硝酸甘油酯、硫酸氢甲酯和硫酸二甲酯 (4)脱水反应
6、)脱水反应 扎依采夫规则:脱去的是羟基和含氢扎依采夫规则:脱去的是羟基和含氢较少的碳上的氢较少的碳上的氢。 也有一些不符合扎依采夫规则扎依采夫规则 (5)氧化氧化(KMnO4/H2SO4、Na2Cr2O7/H2SO4) (6) 邻二醇的制备和氧化开裂邻二醇的制备和氧化开裂 烯烃氧化制备1,2-二醇(顺式) 环氧化合物水解制备1,2-二醇(反式) 邻二醇的氧化开裂邻二醇的氧化开裂 二、酚二、酚1制备:制备:(1)磺化碱熔)磺化碱熔 (2) 芳卤的水解芳卤的水解 2. 反应:反应:(1)酚羟基上的反应酚羟基上的反应酸性(与醇对比)酸性(与醇对比) 苯酚的苯酚的pKa=10,它的酸性比醇强(乙醇,它
7、的酸性比醇强(乙醇的的pKa=17;环己醇的;环己醇的pKa=18),比碳酸),比碳酸弱(弱(pKa=6.38) 与FeCl3的颜色反应(凡是具有烯醇式结构的脂肪族化合物都反应) 与酰氯、酸酐成酯与酰氯、酸酐成酯 (2) 与溴水反应与溴水反应 三、醚三、醚 1制备:制备: (1)醇分子间脱水(制备单醚)醇分子间脱水(制备单醚)(2)Williamson醚的制备醚的制备 乙基叔丁基醚的制备:乙基叔丁基醚的制备:酚醚的制备:酚醚的制备: 2反应:反应:(1)醚键的开裂醚键的开裂三溴化硼和三氯化铝等路易斯酸也三溴化硼和三氯化铝等路易斯酸也能使醚键断裂,如:能使醚键断裂,如:合成上常用苄基醚保护羟基,
8、再采用催化氢化还原脱保护。 (2)环氧乙烷的开裂:环氧乙烷的开裂:酸催化开裂酸催化开裂: 碱催化开裂:碱催化开裂: 不对称环氧化合物的开裂:不对称环氧化合物的开裂: 抗生素麦咪诺的合成 例题一种含硅阻燃剂的合成 1制备:制备:(1)醇的氧化)醇的氧化常用的氧化剂:常用的氧化剂:四、醛酮化合物四、醛酮化合物重铬酸钾重铬酸钾/硫酸;高锰酸钾硫酸;高锰酸钾/硫酸。硫酸。只适应制备低级的挥发性高的醛(采只适应制备低级的挥发性高的醛(采用边滴加边蒸馏)用边滴加边蒸馏),高级醛会进一步,高级醛会进一步氧化成羧酸;氧化成羧酸;KMnO4一般不用于仲醇氧化成酮的制备一般不用于仲醇氧化成酮的制备,会发生碳链断裂
9、。,会发生碳链断裂。 Collins试剂(CrO3Py2),PDC(重铬酸重铬酸Py2)或PCC(氯氯铬酸铬酸Py2)用于氧化伯醇至用于氧化伯醇至醛醛类的氧化剂,对于氧化类的氧化剂,对于氧化仲醇至仲醇至酮酮类同样适用类同样适用;分子中如存在不饱和键不受影响。分子中如存在不饱和键不受影响。 OppenauerOppenauer氧化氧化( (丙酮丙酮-异丙醇铝异丙醇铝)和和JonesJones试剂试剂(CrO(CrO3 3-H-H2 2SOSO4 4)不饱和不饱和仲醇用丙酮仲醇用丙酮-异丙醇铝异丙醇铝或或JonesJones试剂试剂为为氧化剂氧化剂,可得相应不饱和酮;,可得相应不饱和酮;Oppen
10、auerOppenauer氧化氧化不适合伯醇,生成的醛在不适合伯醇,生成的醛在碱性条件下可自身或与丙酮发生羟醛缩合。碱性条件下可自身或与丙酮发生羟醛缩合。JonesJones试剂可将伯醇试剂可将伯醇氧化为羧酸。活性二氧化锰活性二氧化锰活性二氧化锰活性二氧化锰可以氧化可以氧化不饱和伯、仲醇不饱和伯、仲醇(烯丙醇或苄醇)为相应的不饱和醛、酮(烯丙醇或苄醇)为相应的不饱和醛、酮。(2)炔烃的水合)炔烃的水合 (3)傅克酰基化反应傅克酰基化反应 3反应:反应:(1)亲核加成(亲核加成(HCN、NaHSO3、 醇、格醇、格氏试剂、氨的衍生物)氏试剂、氨的衍生物)(A)与氢氰酸的加成反应)与氢氰酸的加成反
11、应脂肪族酮发生加成反应,生成脂肪族酮发生加成反应,生成 羟基腈羟基腈(即氰醇)(即氰醇)由于由于HCN为弱酸,加入碱使其离解为为弱酸,加入碱使其离解为CN-,从而加速反应。从而加速反应。 氰醇氰醇中,氰基可以水解成羧基然后酯化,中,氰基可以水解成羧基然后酯化,也可还原成氨基甲基,羟基可脱水和氨也可还原成氨基甲基,羟基可脱水和氨基化。有机玻璃单体和基化。有机玻璃单体和噁噁唑烷酮可以此唑烷酮可以此为原料合成。为原料合成。有机玻璃单体有机玻璃单体: -甲甲基丙烯酸甲酯基丙烯酸甲酯噁噁唑烷酮唑烷酮(B) 与亚硫酸氢钠的加成反应与亚硫酸氢钠的加成反应大多数醛和脂肪族甲基酮能与亚硫酸氢钠大多数醛和脂肪族甲
12、基酮能与亚硫酸氢钠发生加成反应,生成发生加成反应,生成 羟基磺酸。羟基磺酸。 羟基磺酸易溶于水,但不溶于饱和的羟基磺酸易溶于水,但不溶于饱和的亚硫酸氢钠溶液,故可用于鉴别醛和酮亚硫酸氢钠溶液,故可用于鉴别醛和酮。 (C)与醇的加成反应与醇的加成反应 在无水在无水HCl或其它无水强酸的催化下,或其它无水强酸的催化下,醛(酮)与一分子醇反应生成半缩醛醛(酮)与一分子醇反应生成半缩醛(半缩酮),进一步与一分子醇缩合(半缩酮),进一步与一分子醇缩合生成缩醛(缩酮)。生成缩醛(缩酮)。由于缩醛(缩酮)对氧化剂和碱稳定,由于缩醛(缩酮)对氧化剂和碱稳定,可以用来保护羰基,等反应结束后在酸可以用来保护羰基,
13、等反应结束后在酸的水溶液中加热水解去掉保护,重生羰的水溶液中加热水解去掉保护,重生羰基。基。D)与与Grignard试剂的加成反应试剂的加成反应 醛和酮与醛和酮与Grignard试剂(试剂(RMgX)发生加成)发生加成反应,加成产物水解生成醇。反应,加成产物水解生成醇。 甲醛与甲醛与RMgX反应用于合成伯醇;反应用于合成伯醇; 其它醛与其它醛与RMgX反应用于合成仲醇;反应用于合成仲醇; 酮与酮与RMgX反应用于合成叔醇。反应用于合成叔醇。 (E) 与氨的衍生物加成反应与氨的衍生物加成反应 醛和酮与氨的衍生物(羟胺、肼、醛和酮与氨的衍生物(羟胺、肼、2,4-二硝基苯肼、氨基脲)作用,分别生成二
14、硝基苯肼、氨基脲)作用,分别生成肟、腙、肟、腙、2,4-二硝基苯腙、缩氨脲。二硝基苯腙、缩氨脲。 (2) 氢的活泼性:氢的活泼性: 醛、酮与氨的衍生物的反应,除了合成醛、酮与氨的衍生物的反应,除了合成意义外,常常用于羰基化合物的鉴别与意义外,常常用于羰基化合物的鉴别与分离。因为反应后的生成物大部分是分离。因为反应后的生成物大部分是固固体,且具有一定的熔点,可利用来鉴别体,且具有一定的熔点,可利用来鉴别醛、酮。在稀酸作用下,又水解成原来醛、酮。在稀酸作用下,又水解成原来的醛、酮,可利用来分离和提纯醛、酮的醛、酮,可利用来分离和提纯醛、酮. . (A)烯醇互变异构烯醇互变异构 (B) 羟醛缩合反应
15、羟醛缩合反应 在稀碱存在下,两分子醛(酮)相互作用,在稀碱存在下,两分子醛(酮)相互作用,一分子的一分子的氢加到另一分子的羰基的氧原子氢加到另一分子的羰基的氧原子上,而其余部分加到另一分子的羰基的碳原上,而其余部分加到另一分子的羰基的碳原子上,生成子上,生成 羟基醛(酮),羟基醛(酮),羟基醛(酮)羟基醛(酮)受热生成受热生成,-不饱和醛(酮)。不饱和醛(酮)。 含含氢的两种醛(酮)之间的产物有四种在氢的两种醛(酮)之间的产物有四种在合成中没有意义;如果两者之一不含合成中没有意义;如果两者之一不含氢氢(如甲醛、苯甲醛、糠醛),则产物为两种,(如甲醛、苯甲醛、糠醛),则产物为两种,在合成中有着重
16、要意义。在合成中有着重要意义。(C) 醛醛(不含的不含的氢醛氢醛)与硝基化合物的缩合与硝基化合物的缩合(D)酮与不含)酮与不含氢酯的缩合氢酯的缩合不含不含氢酯:苯甲酸酯、甲酸酯、碳氢酯:苯甲酸酯、甲酸酯、碳 酸酯、草酸二酯等酸酯、草酸二酯等 (E)Mannich反应反应 (F)卤代及卤仿反应)卤代及卤仿反应 卤代反应:卤代反应:p286.4. 卤仿反应:卤仿反应: 凡具有凡具有CH3CO-结构的醛、酮,或具有结构的醛、酮,或具有CH3CH(OH)- 结构的醇能发生卤仿反应。结构的醇能发生卤仿反应。由于碘仿是不溶于水的黄色的固体,且具由于碘仿是不溶于水的黄色的固体,且具有特殊的气味,可用于鉴别。
17、有特殊的气味,可用于鉴别。(3) 氧化还原反应氧化还原反应(A)氧化反应)氧化反应醛易被氧化,可被弱的氧化剂醛易被氧化,可被弱的氧化剂Fehling试剂试剂(以酒石酸盐为络合剂的碱性氢氧化铜)(以酒石酸盐为络合剂的碱性氢氧化铜)或或Tollen试剂(硝酸银的氨溶液)氧化,试剂(硝酸银的氨溶液)氧化,而碳碳不饱和键双键不受影响。而碳碳不饱和键双键不受影响。 RCHO + Cu(OH)2 + NaOH RCOONa + Cu2O RCHO + Ag(NH3)OH RCOONH4 + Ag 酮不易被氧化,在强烈氧化条件下,发生酮不易被氧化,在强烈氧化条件下,发生碳碳键的氧化开裂,一般在合成上没有意碳
18、碳键的氧化开裂,一般在合成上没有意义。义。(B)还原反应)还原反应(a)催化氢化)催化氢化 醛、酮在醛、酮在Ni、Cu、Pt、Pd等的催化作用下等的催化作用下与氢反应生成醇。与氢反应生成醇。(b) 金属氢化物还原金属氢化物还原 (c) Clemmenson 还原还原醛和酮用锌汞齐加盐酸可还原为烃。醛和酮用锌汞齐加盐酸可还原为烃。 (d) Wolff-Kishner-黄鸣龙黄鸣龙醛和酮与肼在高沸点溶剂如一缩二乙二醇醛和酮与肼在高沸点溶剂如一缩二乙二醇中,首先与肼生成腙,腙在碱性条件下加热中,首先与肼生成腙,腙在碱性条件下加热失去氮,羰基转变为亚甲基。失去氮,羰基转变为亚甲基。Clemmenson 还原和还原和Wolff-Kishner-黄鸣龙黄鸣龙还原都可将羰基还原为亚甲基,前者在酸性性条还原都可将羰
温馨提示
- 1. 本站所有资源如无特殊说明,都需要本地电脑安装OFFICE2007和PDF阅读器。图纸软件为CAD,CAXA,PROE,UG,SolidWorks等.压缩文件请下载最新的WinRAR软件解压。
- 2. 本站的文档不包含任何第三方提供的附件图纸等,如果需要附件,请联系上传者。文件的所有权益归上传用户所有。
- 3. 本站RAR压缩包中若带图纸,网页内容里面会有图纸预览,若没有图纸预览就没有图纸。
- 4. 未经权益所有人同意不得将文件中的内容挪作商业或盈利用途。
- 5. 人人文库网仅提供信息存储空间,仅对用户上传内容的表现方式做保护处理,对用户上传分享的文档内容本身不做任何修改或编辑,并不能对任何下载内容负责。
- 6. 下载文件中如有侵权或不适当内容,请与我们联系,我们立即纠正。
- 7. 本站不保证下载资源的准确性、安全性和完整性, 同时也不承担用户因使用这些下载资源对自己和他人造成任何形式的伤害或损失。
最新文档
- 炸鸡店打工员工合同范本
- 液压闸刀转让协议书范本
- 物品转让协议书合同范本
- 特色餐饮服务合同协议书
- 物业管道修理合同协议书
- 香蕉生意转让协议书范本
- 火锅串串店合伙人协议书
- 测绘承包合同协议书范本
- 砌墙抹灰包工合同协议书
- 江苏劳动仲裁协议书范本
- 消防通风排烟劳务合同范本
- 六年级语文毕业总复习教案
- 江苏省苏州市苏州地区学校2024届七年级英语第二学期期末统考试题含答案
- 电商客服周工作计划
- 新青岛版六三制五年级上册科学全册知识点
- DL∕T 1563-2016 中压配电网可靠性评估导则
- Vericut培训教程(可修改)
- 校级课题结题报告会方案
- 高三英语一轮复习人教版(2019)必修第一至三册一词多义和熟词生义清单
- 《电力建设土建工程施工技术检验规范》
- 四年级【语文(统编版)】牛和鹅(第一课时)课件

评论
0/150
提交评论