



版权说明:本文档由用户提供并上传,收益归属内容提供方,若内容存在侵权,请进行举报或认领
文档简介
1、专题三 常见的烃 第一单元 脂肪烃基本要求:1、 能正确区分脂肪烃、芳香烃、饱和烃和不饱和烃。2、 了解烷烃、烯烃、炔烃物理性质的变化与分子中碳原子数的关系。3、 以典型代表物为例,掌握烷烃、烯烃、炔烃等有机化合物的化学性质,进一步掌握取代反应、加成反应、加聚反应等典型的有机反应类型。4、 了解不饱和烃与氢气、水、卤化氢等物质的加成反应。5、 能根据烯烃的加聚反应分析有机高分子的链接和单体。6、 知道脂肪烃的来源,了解石油化学工业中分馏、裂化、裂解等处理方法的主要原理及产物,了解石油化工产品对人们生活的影响。发展要求:了解合成常见高分子化合物的方法说明:1、烯烃的不对称加成反应及马氏规则不作要
2、求。 2、环状脂肪烃的结构与性质不作要求。第1、2课时 脂肪烃的性质一、 烷烃(又可称饱和烃) 1、结构特点:可用“ 单 ”、“ 链 ”、“ 饱 ”概括。(单键、锯齿、四面体)分子式通式:CnH2n+2 2、物理性质:(1)熔沸点:碳原子数越多,相对分子质量越大,熔沸点越高;(如:甲烷 乙烷 丙烷 正丁烷) 碳原子数相同时,支链数越多,熔沸点越低。 (如:正丁烷 异丁烷;正戊烷 异戊烷 新戊烷) 常温常压下是气体的烷烃,其碳原子数小于等于4,此外,新戊烷常温常压下也是气体。随着分子中碳原子数目的增加,状态由气态逐渐过渡到液态和固态。(2)密度:碳原子数越多,密度越大;液态烷烃的密度小于水的密度
3、。(3)溶解性:不溶于水,易溶于有机溶剂。有的液态烷烃本身就是有机溶剂,如己烷、汽油、煤油等。3、化学性质: 一般比较稳定。与酸、碱、氧化剂都不发生反应,也难与其它物质化合。(1)取代反应 写出CH4光照下与Cl2反应的方程式 (2)氧化反应( 使酸性KMnO4溶液褪色) 燃烧的通式: 甲烷燃烧的现象: 随着碳原子数的增加,往往燃烧越来越不充分(烷烃CnH2n+2中,n越大,w(C)越大),火焰明亮,并伴有黑烟。(3)高温分解反应:甲烷隔绝空气高温下可分解成碳和氢气;长链烷烃高温下可分解成短链烷烃和烯烃,这在石油化工上有很重要的应用,称为_。 二、烯烃(分子中含有 碳碳双键 的不饱和
4、烃) 1、单烯烃: 分子中含有一个碳碳双键 多烯烃: 分子中含有两个及以上碳碳双键 单烯烃(简称烯烃) 分子式的通式:CnH2n组成特点: 碳氢原子个数比1:2 二烯烃:分子中含有二个碳碳双键。二烯烃又可分为孤立二烯烃和共轭二烯烃;共轭二烯烃的结构特点是单双键交替排列,在加成反应时不同于一般的单烯烃;而孤立二烯烃是在二个双键之间相隔二个或二个以上的单键,化学性质和单烯烃相同。2、物理性质(类似于烷烃)3、化学性质:(1)加成反应(与H2、X2、HX、H2O、HCN等)例:写出下列反应的化学方程式:乙烯通入溴水中:乙烯与水的反应:乙烯与溴化氢反应: 阅读课本42 “马氏加成规则”,丙烯与氯化氢、
5、H2O反应后,会生成什么产物呢?试写出反应方程式。 1,3-丁二烯与溴单质可能发生的两种加成反应,试写出反应方程式。 1,2-加成: 1,4-加成: (双键中一根键容易断裂)CH2CHCHCH2 Br2 BrBrBrBr1 2 3 41 2 3 41 2 3 41,2加成801 2 3 4BrBr1,4加成601 2 3 4BrBr(2)氧化反应 燃烧:用通式表示烯烃的燃烧化学方程式_ 烯烃CnH2n中,w(C)不变 乙烯燃烧的现象: 烯烃可使酸性KMnO4溶液褪色,烯烃被氧化的产物的对应关系为:烯烃被氧化的部位= CH2氧化产物例:现已知某烯烃的化学式为C5H10,它与酸性高锰酸钾溶液反应后
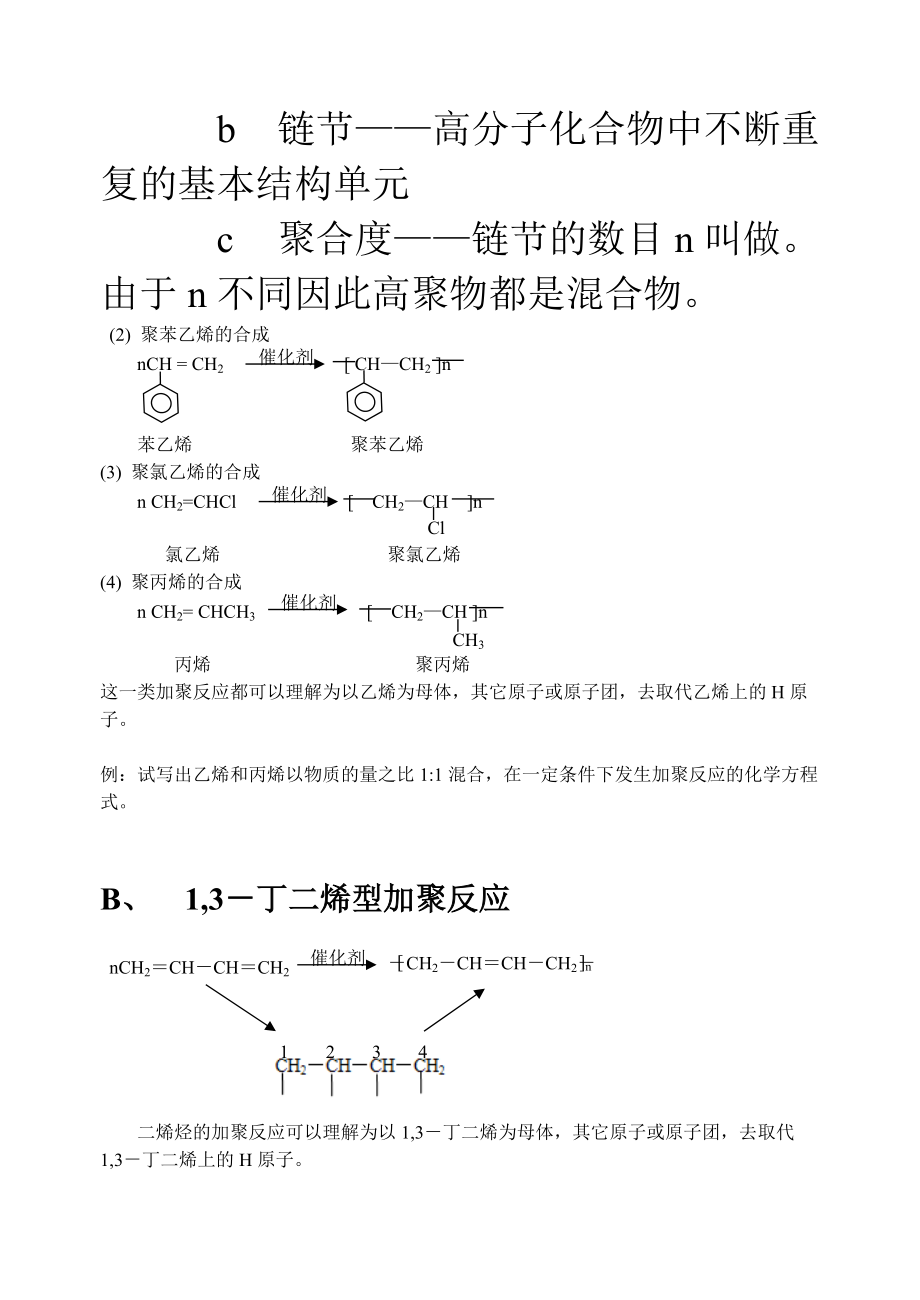
6、得到的产物为乙酸和丙酸,推测出此烯烃的结构简式为 。若与酸性高锰酸钾溶CH3CH2CCH3O 液反应后得到的产物是二氧化碳和丁酮 ,则此烯烃的结构简式为 (3)加聚反应CH2CH2A 、乙烯型加聚反应(1)聚乙烯的合成:nCH2= CH2 n 乙烯 聚乙烯注意:a 单体用以形成高分子化合物的小分子物质b 链节高分子化合物中不断重复的基本结构单元c 聚合度链节的数目n叫做。由于n不同因此高聚物都是混合物。催化剂(2) 聚苯乙烯的合成nCH = CH2 CHCH2 n 苯乙烯 聚苯乙烯催化剂(3) 聚氯乙烯的合成Cln CH2=CHCl CH2CH n 氯乙烯 聚氯乙烯催化剂(4) 聚丙烯的合成C
7、H3n CH2= CHCH3 CH2CH n 丙烯 聚丙烯这一类加聚反应都可以理解为以乙烯为母体,其它原子或原子团,去取代乙烯上的H原子。例:试写出乙烯和丙烯以物质的量之比1:1混合,在一定条件下发生加聚反应的化学方程式。B、 1,3丁二烯型加聚反应CH2CHCHCH2 n催化剂nCH2CHCHCH2 1 2 3 4二烯烃的加聚反应可以理解为以1,3丁二烯为母体,其它原子或原子团,去取代1,3丁二烯上的H原子。CH3例:天然橡胶是异戊二烯(CH2CCHCH2通过加聚反应形成的一类高分子物质。写出相关的化学方程式。CH2CHCHCH2 nCH3催化剂CH3nCH2CCHCH2 小结:对于加聚反应
8、所形成的高分子物质,其主链碳原子是原来的不饱和碳原子。三、炔烃(分子中含有 碳碳叁键 的不饱和烃) 1、单炔烃: 分子中含有一个碳碳叁键烃 其分子式的通式为CnH2n2,与同碳原子数的 二烯烃 、 环烯烃 互为同分异构体。 2、物理性质(类似于烷烃)3、化学性质:(1)加成反应(与H2、X2、HX、H2O、HCN等,按1:1或1:2的比例)乙炔与氢气1:2反应_丙炔与氯化氢1:1反应_乙炔与水反应_(2)氧化反应 写出乙炔燃烧反应的化学方程式_乙炔燃烧的现象_,与甲烷、乙烯燃烧对比,出现不同的现象的原因是 炔烃CnH2n2中,n越大,w(C)越小 炔烃可使酸性KMnO4溶液褪色,炔烃被氧化的产
9、物的对应关系为: HC氧化为CO2 R-C氧化为 R-COOH (3)聚合反应第3课时 脂肪烃的来源1、 实验室制法(1)乙烯的实验室制法原理:CH3CH2OH CH2CH2 H2O (消去反应)装置:液 + 液 气体注意事项: 浓H2SO4 的作用:催化剂,吸水剂碎瓷片的作用是防止反应液暴沸温度必须达到170否则会有其它产物生成 温度计应插入反应液中,作用是测量反应液的温度,以便控制反应的进行。(2)乙炔的实验室制法原理:CaC2 2H2O CHCH Ca(OH)2 装置:固 + 液 气收集方法:排水收集法注意事项:一般用饱和食盐水与CaC2反应,这样可以减缓反应速率制取H2、CO2、H2S
10、可用启普发生气,但制乙炔不能用。制取乙炔时,应在导气管附近塞入少量棉花。在点燃乙炔前必须先检查纯度,否则易出现爆炸事故。制得的乙炔有臭味是因为含H2S、PH3,除杂宜用硫酸铜溶液。2、 工业来源(1)石油的成分各种烃的混合物(2)石油炼制方法A 分馏根据石油中各物质的沸点不同,用加热的方法,使各成分分离,是石油炼制过程中最常用的方法B 裂化为了提高轻质油(如汽油)的产量,用加热或催化剂使石油中碳链较长的有机物分解为碳链较短的物质,通常分为热裂化和催化裂化C 裂解深度裂化,目的是为了获得小分子的烯烃D 催化重整获得芳香烃的主要途径E 催化加氢石油的炼 制方法分馏裂化石油的裂解常压减压热裂化催化裂化原理用蒸发冷凝的方法把石油分成不同沸点范围的蒸馏产物在加热或催化剂存在的条件下,
温馨提示
- 1. 本站所有资源如无特殊说明,都需要本地电脑安装OFFICE2007和PDF阅读器。图纸软件为CAD,CAXA,PROE,UG,SolidWorks等.压缩文件请下载最新的WinRAR软件解压。
- 2. 本站的文档不包含任何第三方提供的附件图纸等,如果需要附件,请联系上传者。文件的所有权益归上传用户所有。
- 3. 本站RAR压缩包中若带图纸,网页内容里面会有图纸预览,若没有图纸预览就没有图纸。
- 4. 未经权益所有人同意不得将文件中的内容挪作商业或盈利用途。
- 5. 人人文库网仅提供信息存储空间,仅对用户上传内容的表现方式做保护处理,对用户上传分享的文档内容本身不做任何修改或编辑,并不能对任何下载内容负责。
- 6. 下载文件中如有侵权或不适当内容,请与我们联系,我们立即纠正。
- 7. 本站不保证下载资源的准确性、安全性和完整性, 同时也不承担用户因使用这些下载资源对自己和他人造成任何形式的伤害或损失。
最新文档
- GB/T 13465.1-2024不透性石墨材料试验方法第1部分:总则
- 废旧家电回收利用行业营销策略方案
- 离心碾磨机细分市场深度研究报告
- 人力资源流程再造行业市场调研分析报告
- 相框边条项目运营指导方案
- 乐器销售行业营销策略方案
- 数据管理用计算机产品供应链分析
- 纺织品制壁挂细分市场深度研究报告
- 书法培训行业相关项目经营管理报告
- 茶壶项目运营指导方案
- 第4章-动车组列车餐饮服务操作技能《高速铁路列车餐饮服务》
- 安徽省宿州市砀山县2023-2024学年九年级上学期12月质量调研语文试题(含答案)
- 高教社新国规中职教材《英语1基础模块》英语1-U1-220905改
- 大学生婚恋观调查问卷
- 第五章-纳滤讲解
- 托育机构备案书及备案承诺书范本
- 第14课池塘里的世界(教学课件)六年级科学上册(冀人版)
- 南宁市事业单位分类目录
- IOS9001:2015内审检查表(各部门)
- 第一讲 伟大事业都始于梦想(课件)
- 管道补偿器安装检验记录

评论
0/150
提交评论