



版权说明:本文档由用户提供并上传,收益归属内容提供方,若内容存在侵权,请进行举报或认领
文档简介
1、玉溪一中高2013届高三上学期第三次月考化学试题相对原子质量:Li7,C12,N14,O16,S32,Cl35.5,Na23,Mg24,Al27,K39,Fe56,Cu64,Zn65, I-127说明:测试时间120分钟,满分100分。第I卷(选择题共48分)一、选择题(本题包括24小题,每小题2分,共48分。每小题只有一个选项符合题意)1人体内产生的活性氧能加速人体衰老,被称为“生命杀手”。化学家尝试用Na2SeO3消除人体内活性氧,Na2SeO3在体内的作用是A氧化剂B还原剂C既是氧化剂又是还原剂D既不是氧化剂又不是还原剂2.下列说法中,不正确的是同一元素的不同核素互称为同位素化学键可以使
2、离子相结合,也可以使原子相结合金属腐蚀的实质是金属原子失去电子被还原的过程Ksp不仅与难溶电解质的性质和温度有关,而且还与溶液中的离子浓度有关铅蓄电池在放电过程中,负极质量减少,正极质量增加Al和Fe在一定条件下都能与某些氧化物反应干冰和氨都属于弱电解质汽油和花生油的主要成份都是油脂A B C D3.下列叙述正确的是A同一主族的元素,原子半径越大,其单质的熔点一定越高B同一周期元素的原子,半径越小一定越容易失去电子C稀有气体元素的原子序数越大,其单质的熔、沸点一定越高D同一主族的元素的氢化物,相对分子质量越大,它的沸点一定越高4.下列实验方案不能达到预期目的的是选项实验方案预期目的A.将含有H
3、Cl的CO2气体通过饱和NaHCO3溶液除去CO2中的HClB.向X溶液中滴加盐酸酸化的BaCl2溶液检验X溶液中是否含有SO42-C.向醋酸钠溶液中滴入酚酞试液,加热后若红色加深证明盐类的水解是吸热的D.向含有少量苯酚的苯中加入NaOH溶液,振荡、静置、分液除去苯中的苯酚5.下列叙述中,正确的是 A1.00 L 1.00 mol·L-1盐酸中含有6.02×1023个HCl分子 B25、101 kPa下,42 g N2和CO混合气体中含有的原子数为3NA C112 L C02含有的分子数为O5 NAD配制1.0 L 1.0 mol·L-1的CuSO4溶液,可将25
4、0.0 g CuSO4·5H2O溶于1.0 L水6.下列化合物的一氯代物的数目排列顺序正确的是CH3CH2CH2CH2CH2CH3(CH3)2CHCH(CH3)2(CH3)3CCH2CH3(CH3)3CC(CH3)3A > > > B > = > C > > >D = > > 7下列说法中,不正确的是 A有机化合物中每个碳原子最多形成4个共价键 B油脂、淀粉、蛋白质在一定条件下都能发生水解反应 C用溴水既可以鉴别甲烷和乙烯,也可以除去甲烷中的乙烯 D乙烯和苯均能发生氧化反应,说明乙烯和苯分子中均有碳碳双键 8有一种锂电池,用
5、金属锂和石墨作电极材料,电解质溶液是由四氯铝锂(LiAlCl4)溶解在亚硫酰氯()中而形成的,电池总反应方程式为:8Li3SOCl2=6LiClLi2SO32S,下列叙述中正确的是A电解质溶液中混入水,对电池反应无影响B金属锂作电池的正极,石墨作电池的负极C电池工作过程中,亚硫酰氯(SOCl2)被还原为Li2SO3 D电池工作过程中,金属锂提供的电子与正极区析出硫的物质的量之比为419.已知118号元素的离子aW3+、bX+、cY2-、dZ-具有相同电子层结构,下列关系正确的是 A.原子半径:W>YB.离子半径:Y2- < Z-C.热稳定性:H2Y>HZ D.碱性:W(OH)
6、3 > XOH10.下列叙述中,正确的是A.直径介于1nm至100nm之间的微粒称为胶体B. Fe(OH)3胶体是纯净物C.利用丁达尔效应可以区别溶液和胶体D.胶体粒子很小可以透过半透膜11以下实验原理或操作中,正确的是A分液操作中,待下层液体流出后,再将上层液体从分液漏斗下口放出B焰色反应实验中,铂丝在蘸取待测溶液前,应先用稀硫酸洗净并灼烧C中和滴定实验中,如用于盛放待测溶液的锥形瓶洗净后未干燥,不影响测定结果D测定溶液pH时,可用pH试纸蘸取少量待测液,并与标准比色卡比较12短周期元素E的氯化物ECl2的熔点为-78°,沸点为59°C,分子中各原子均满足8电子稳定
7、结构,下列判断错误的是AE是一种非金属元素B在ECl2中E与Cl之间形成共价键CE的一种氧化物为EO2DE位于元素周期表的IVA族13下列反应的离子方程式正确的是 向苯酚钠溶液中通人少量的CO2:2C6H5O-+CO2+H2O2C6H5OH+CO32-将金属钠加入水中:2Na + 2H2O = 2Na+ + 2OH + H2石灰石溶于醋酸:CaCO32CH3COOH=2CH3COO+ Ca2+CO2+H2O碳酸钠水解:CO32-+2H2OH2CO3+2OH-向氢氧化钡中滴加硫酸:Ba2+ + SO42- + H+ + OH- = BaSO4 + H2O次氯酸钙溶液中通入过量二氧化碳:Ca2+2
8、 ClO- + CO2 + H2O =CaCO3+ 2HClO氯化铝的溶液中加入过量氨水:Al3+4NH3·H2O=AlO2+4NH4+2H2O氯气与水反应:Cl2 + H2O = 2H+ + Cl + ClO-纯碱溶液中滴加少量盐酸:CO32-+ H+= HCO3-A B C D14根据碘与氢气反应的热化学方程式,下列判断正确的是 A254g I2(g)中通入2g H2(g),反应放热9.48 kJ B当反应吸收52.96kJ热量时转移2mole C反应的反应物总能量比反应的反应物总能量低 D1 mol固态碘与1 mol气态碘所含能量相差17.00 kJ15下列各组离子能大量共存的
9、是 “84”消毒液的水溶液中:Fe2+、Cl、Ca2+、Na+ 加入KSCN显红色的溶液:K+、NH4+、Cl、S2 能够与金属Cu常温下反应放出气体的溶液;Fe3+、Al3+、SO42、K+ pH=2的溶液中:NH4+、Na+、Cl、Cu2+ 无色溶液中:K+、CH3COO、HCO3、MnO4 A B C D16金属镍有广泛的用途粗镍中含有少量Fe、Zn、Cu、Pt杂质,可用电解法制备高纯度的镍,下列叙述正确的是(已知:氧化性Fe2<Ni2<Cu2)A阳极发生还原反应,其电极反应式:Ni22e=NiB电解过程中,阳极质量的减少与阴极质量的增加相等C电解后,溶液中存在的金属阳离子只
10、有Fe2和Zn2D电解后,电解槽底部的阳极泥中有Cu和Pt17.X、Y、Z、W是分别位于第2、3周期的元素,原子序数依次递增。X与Z位于同一主族,Y元素的单质既能与盐酸反应也能与NaOH溶液反应,Z原子的最外层电子数是次外层电子数的一半,Y、Z、W原子的最外层电子数之和为14。下列说法正确的是 A原子半径由小到大的顺序:X< Y < Z< W BZ的最高价氧化物能与水反应生成相应的酸CY单质在一定条件下可以与氧化铁发生置换反应 D室温下,0.1 mol/L W的气态氢化物的水溶液的pH >118用来表示可逆反应:2A(g)B(g)2C(g) H<0 的正确图象是下
11、图中的 A B C D19由化学能转变的热能或电能仍然是人类使用的主要能源根据下图所示的装置,判断下列说法不正确的是A该装置中Cu极为阳极 B当铜片的质量变化了128 g时,a极上 消耗的O2在标准状况下的体积为224 L C该装置中b极的电极反应式是:H22OH2e=2H2O D该装置中a极为正极,发生氧化反应20.膳食纤维具有突出的保健功能,人体的“第七营养素”木质素是一种非糖类膳食纤维,其单体之一是芥子醇,结构简式如图所示。下列有关芥子醇的说法正确的是 A.芥子醇的分子式是C11H14O4,属于芳香烃B.芥子醇与浓溴水既能发生取代反应又能发生加成反应 C.芥子醇能发生氧化、取代、加成、聚
12、合反应D.1mol芥子醇能与含2mol NaOH的水溶液完全反应21X、Y、Z、W有如图所示的转化关系,则X、W可能是C、O2AlCl3、NaOHFe、HNO3S、O2A BC D22常温下,浓度均为01mol/L的三种溶液:CH3COOH溶液NaOH溶液CH3COONa溶液,下列说法中不正确的是(忽略混合前后溶液体积变化) A.溶液的pH值: B.水电离出的c(OH):C.和等体积混合后的溶液:c(CH3COOH)+ c(CH3COO)01mol/LD.和等体积混合后的溶液:c(Na+)+ c(H+)c(OH)+c(CH3COO)23.将mol钠和mol铝一同投入g足量水中,所得溶液密度为g
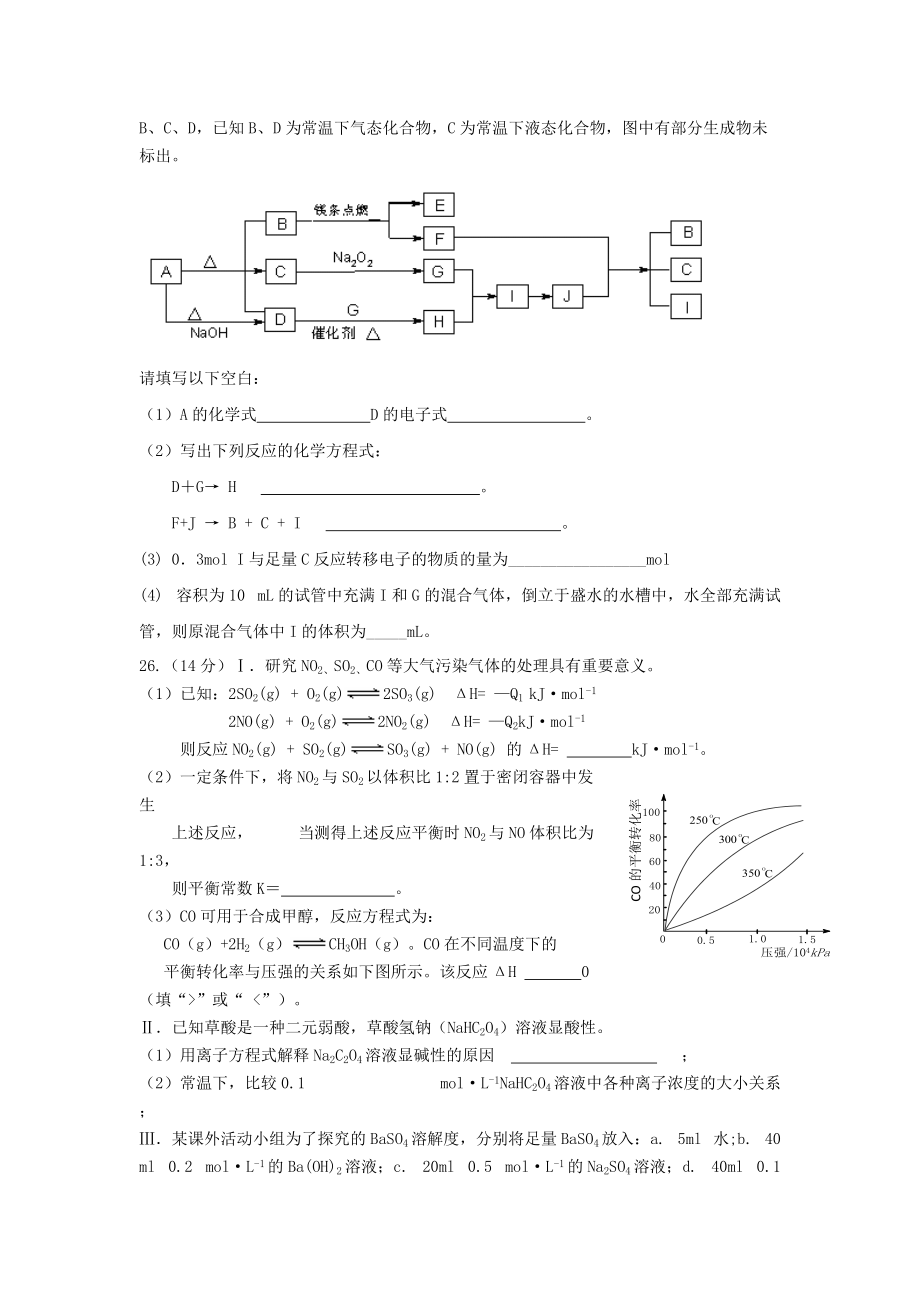
13、·mL1,该溶液的溶质质量分数为A B C D24某同学对未知物A盐的水溶液进行了鉴定,实验过程及现象如图所示:现对A、B、C、D作出的如下推断中,不正确的是A盐A一定是FeBr3 B浅黄色沉淀B是AgBrC滤液C中一定含Fe3 DD溶液中有Fe(SCN)3第卷(非选择题共52分)二非选择题(包括必考题和选考题两部分;第25至27题为必考题,每个试题都必须作答。第28题和29题为选考题。)(一)必考题(本题包括3个小题,共39分)25.(12分)下图中AJ分别代表相关反应中的一种物质,已知A分解得到等物质的量的B、C、D,已知B、D为常温下气态化合物,C为常温下液态化合物,图中有部分
14、生成物未标出。请填写以下空白:(1)A的化学式 D的电子式 。 (2)写出下列反应的化学方程式:DG H 。F+J B + C + I 。(3) 03mol I与足量C反应转移电子的物质的量为_mol(4) 容积为10 mL的试管中充满I和G的混合气体,倒立于盛水的水槽中,水全部充满试管,则原混合气体中I的体积为_mL。26.(14分)研究NO2、SO2、CO等大气污染气体的处理具有重要意义。(1)已知:2SO2(g) + O2(g)2SO3(g) H= Q1 kJ·mol-12NO(g) + O2(g)2NO2(g) H= Q2kJ·mol-1 则反应NO2(g) + S
15、O2(g)SO3(g) + NO(g) 的H= kJ·mol-1。CO的平衡转化率/%(2)一定条件下,将NO2与SO2以体积比1:2置于密闭容器中发生 上述反应, 当测得上述反应平衡时NO2与NO体积比为1:3,则平衡常数K 。(3)CO可用于合成甲醇,反应方程式为:CO(g)+2H2(g)CH3OH(g)。CO在不同温度下的平衡转化率与压强的关系如下图所示。该反应H 0(填“>”或“ <”)。已知草酸是一种二元弱酸,草酸氢钠(NaHC2O4)溶液显酸性。(1)用离子方程式解释Na2C2O4溶液显碱性的原因 ;(2)常温下,比较0.1 mol·L-1NaHC2
16、O4溶液中各种离子浓度的大小关系 ;某课外活动小组为了探究的BaSO4溶解度,分别将足量BaSO4放入:a. 5ml 水;b. 40 ml 0.2 mol·L-1的Ba(OH)2溶液;c. 20ml 0.5 mol·L-1的Na2SO4溶液;d. 40ml 0.1 mol·L-1的H2SO4溶液中,溶解至饱和。(1)以上各溶液中,的浓度由大到小的顺序为 ;A.b>a>c>d B.b>a>d>c C.a>d>c>b D.a>b>d>c(2)某同学取同样的溶液b和溶液d直接混合,则混合溶液的pH值
17、为 (设混合溶液的体积为混合前两溶液的体积之和)。27.(13分)某实验小组同学为了探究铜与浓硫酸的反应,进行了如下系列实验。【实验1】铜与浓硫酸反应,实验装置如图所示。实验步骤:先连接好装置,检验气密性,加入试剂;加热A试管直到B中品红褪色,熄灭酒精灯;将Cu丝上提离开液面。(1)装置A中发生反应的化学方程式为 。(2)熄灭酒精灯后,因为有导管D的存在,B中的液体不会倒吸,其原因是 。(3)拆除装置前,不需打开胶塞,就可使装置中残留气体完全被吸收,应当采取的操作是 。【实验2】实验中发现试管内除了产生白色固体外,在铜丝表面还产生黑色固体甲,其中可能含有氧化铜、硫化铜、硫化亚铜,以及被掩蔽的氧
18、化亚铜。查阅资料:氧化亚铜在酸性环境下会发生自身氧化还原反应生成Cu2+和铜单质,在氧气流中煅烧,可以转化为氧化铜。硫化铜和硫化亚铜常温下都不溶于稀盐酸,在氧气流中煅烧,硫化铜和硫化亚铜都转化为氧化铜和二氧化硫。固体甲加入稀盐酸过滤蓝色滤液滤渣洗涤干燥 氧气流中煅烧、冷却称量至恒重 固体乙称取2.00g固体丙1.84g为了研究甲的成分,该小组同学在收集到足够量的固体甲后,进行了如图的实验: (4)中检验滤渣是否洗涤干净的实验方法是 。(5)中在煅烧过程中一定发生的反应的化学方程式为 。(6)下列对于固体甲的成分的判断中,正确的是(填字母选项) 。 A固体甲中,CuS和Cu2S不能同时存在 B固
19、体甲中,CuO和Cu2O至少有一种 C固体甲中若没有Cu2O,则一定有Cu2S D固体甲中若存在Cu2O,也可能有Cu2S(二)选考题(13分。从给出的2道小题中任选一题作答。如果多做,则按所做的第一小题计分)28【 物质结构与性质 】(13分)氯化铬酰(CrO2Cl2)在有机合成中可作氧化剂或氯化剂,能与许多有机物反应,请回答下列问题: (1)写出铬原子的基态电子排布式_,与铬同周期的所有元素的基态原子中最外层电子数与铬原子相同的元素有_(填元素符号),其中一种金属的阳离子易与H2O或NH3通过_结合在一起。 (2)CrO2Cl2常温下为深红色液体,能与CCl4、CS2等互溶,据此可判断Cr
20、O2Cl2是_(填“极性”或“非极性”)分子。(3)在乙烯、SO32-、BF3、H2O、CCl4 SO3五种有机溶剂中,碳原子采取sp2杂化的分子有_(填序号),CS2分子的空间构型是_。29. 【 有机化学基础 】(13分)某有机物X(C7H8O)与另一有机物Y发生如下反应生成化合物Z(C11H14O2)。XYZH2O(1)、X是下列化合物之一,已知X不能与FeCl3溶液发生显色反应,则X是 。ABCD(2)、Y的分子式是 ,可能的结构简式是 和 。(3)、Y有多种同分异构体,其中一种同分异构体E发生银镜反应后,其产物经酸化可得到F(C4H8O3)。F可发生如下反应:FH2O该反应的类型是_,E的结构简式是_。(4)、若Y与E具有相同的碳链,则Z的结构简式为_。玉溪一中2013届高三上学期第三次月考化学试卷答案123456789101112BCCBBDDDACCD131415161718192021222324BCDDCCDCACCA25.(12分) (1) N
温馨提示
- 1. 本站所有资源如无特殊说明,都需要本地电脑安装OFFICE2007和PDF阅读器。图纸软件为CAD,CAXA,PROE,UG,SolidWorks等.压缩文件请下载最新的WinRAR软件解压。
- 2. 本站的文档不包含任何第三方提供的附件图纸等,如果需要附件,请联系上传者。文件的所有权益归上传用户所有。
- 3. 本站RAR压缩包中若带图纸,网页内容里面会有图纸预览,若没有图纸预览就没有图纸。
- 4. 未经权益所有人同意不得将文件中的内容挪作商业或盈利用途。
- 5. 人人文库网仅提供信息存储空间,仅对用户上传内容的表现方式做保护处理,对用户上传分享的文档内容本身不做任何修改或编辑,并不能对任何下载内容负责。
- 6. 下载文件中如有侵权或不适当内容,请与我们联系,我们立即纠正。
- 7. 本站不保证下载资源的准确性、安全性和完整性, 同时也不承担用户因使用这些下载资源对自己和他人造成任何形式的伤害或损失。
最新文档
- 收养家庭育儿指导服务平台构建路径考核试卷
- 木片尺寸精度与自动化检测考核试卷
- 煤炭产业政策建议与展望考核试卷
- 摄影摄像器材租赁服务要点考核试卷
- 搪瓷制品的质量保证体系与认证考核试卷
- 活动背景板租赁业务操作要领考核试卷
- 灌溉与农业生态环境保护规划考核试卷
- 日用品生产设备操作安全防护设备的选择与应用考核试卷
- 农村合股经营合同标准文本
- 海洋测绘软件考核试卷
- 2025届四川省成都市高三二诊生物试题(原卷版+解析版)
- 2025年度粤医云、国培卫健全科医学临床医学2月题目及答案
- 校园消费进行时青春权益不掉队-3·15消费者权益日教育宣传主题班会课件
- 大学生舞蹈创新创业计划书
- 英语-安徽省滁州市2025年(届)高三下学期第一次教学质量监测(滁州一模)试题和答案
- 人教版六年级下学期数学第四单元《比例》典型题型专项练习(含答案)
- 污水处理设施运维服务投标方案(技术标)
- 发票红冲申请书
- DL5190.5-2019电力建设施工技术规范第5部分:管道及系统
- 国开电大软件工程形考作业3参考答案
- 通用电子嘉宾礼薄

评论
0/150
提交评论