



版权说明:本文档由用户提供并上传,收益归属内容提供方,若内容存在侵权,请进行举报或认领
文档简介
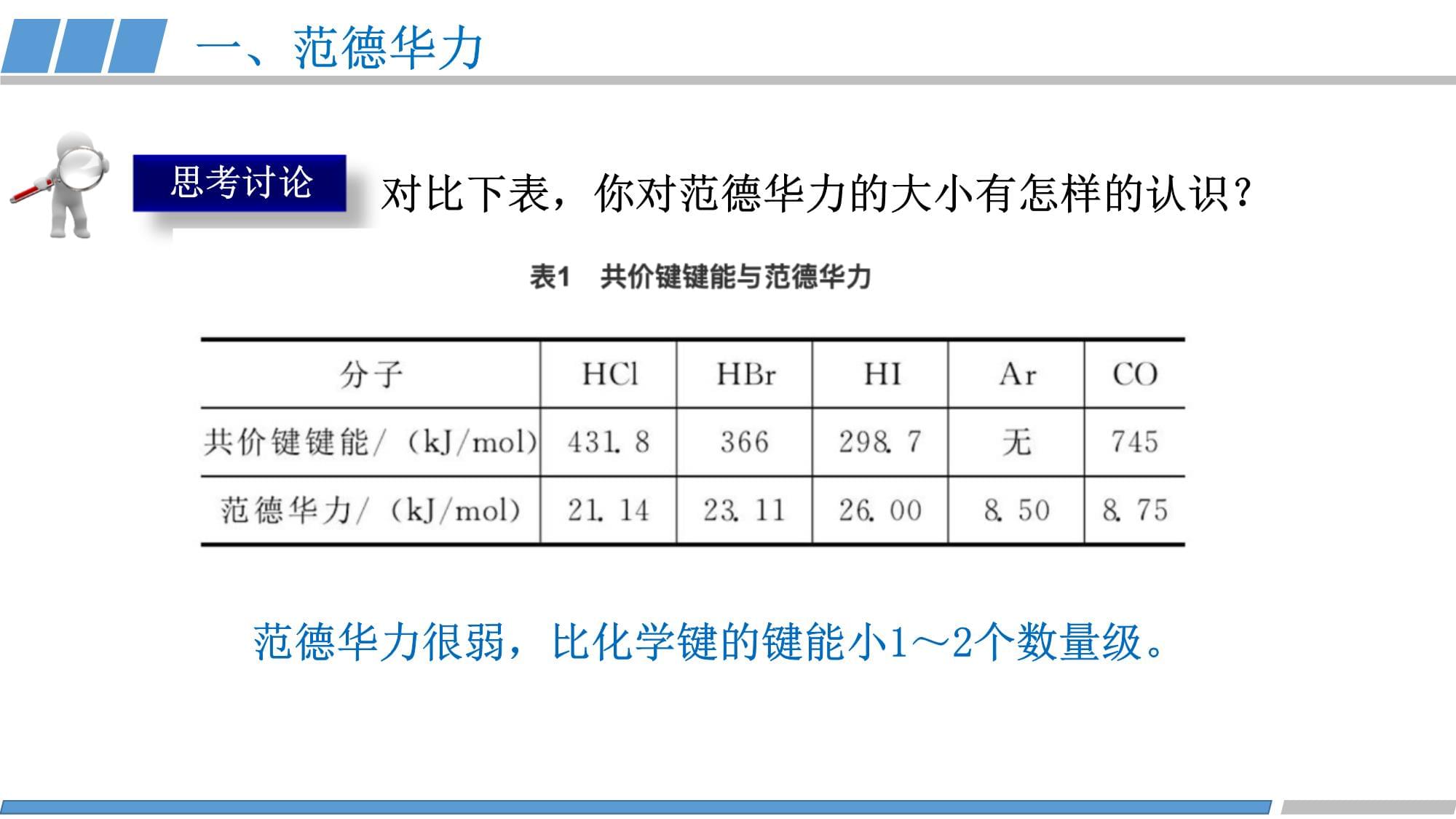
《分子间作用力》人教版选择性必修2第二章第三节第2课时研究表明分子之间普遍存在着相互作用力,而荷兰物理学家范德华是最早研究这种作用力的科学家,因而把这种分子间作用力称为范德华力。J.D.VanderWaals一、范德华力一、范德华力思考讨论对比下表,你对范德华力的大小有怎样的认识?范德华力很弱,比化学键的键能小1~2个数量级。一、范德华力在某些物质如Br2、I2的熔化沸腾过程中,克服了什么作用力?那么这些物质的熔沸点和什么有关?Br2、I2的熔化沸腾过程中,破坏了范德华力;它们的熔沸点取决于范德华力的大小,范德华力越大,熔沸点越高。思考讨论已知卤素单质的相对分子质量、熔点、沸点数据如下表所示单质相对分子质量熔点/℃沸点/℃F238-219.6-188.1Cl271-101.0-34.6Br2160-7.258.78I2254113.5184.4(1)分析上表,总结卤素单质熔点、沸点有什么变化规律?卤素单质的熔点、沸点随着相对分子质量的增大而升高。相对分子质量越大,范德华力越大,熔沸点越高。思考讨论对比下表,范德华力可能还和什么因素有关?一、范德华力物质相对分子质量范德华力Ar408.50CO288.75分子的极性越大,范德华力越大。思考讨论请同学们预测一下卤化氢的熔沸点变化规律。卤化氢相对分子质量HF20HCl36.5HBr81HI128为什么HF的沸点反常呢?可能是什么原因?HF分子之间存在特别强的相互作用,这种作用力叫做氢键。HFHClHBrHI沸点熔点/℃二、氢键水分子间氢键实物模型氢键的形成原理:
当H原子与电负性很大的原子(如N、O、F)形成共价键时,由于N、O、F的电负性很大,将共用电子对强烈地吸引过来,而使H原子带有较高的正电性(δ+)。此时,H原子与另一分子中的N、O、F(δ-)便存在了一种强烈的静电作用。这就是氢键。资料卡片二、氢键表示方法:氢键的通式可用X—H…Y—表示。式中X和Y表示N、O、F,“—”表示共价键,“…”表示氢键。HFHFHFHF*氢键键长一般定义为X—H…Y的长度,而不是H…Y的长度。键长思考讨论根据氢键的形成原理,你认为最强的氢键是什么?
X—H…Y强弱与X和Y的电负性有关。电负性越大,则氢键越强,如F原子电负性最大,因而F-H…F是最强的氢键。氢键类型F-H…FO-H…O氢键键能()28.118.8二、氢键思考讨论已知F-H…F是最强的氢键,为什么H2O的沸点会高于HF?二、氢键氢键具有一定的方向性和饱和性。物质的沸点与氢键的强弱和数目有关。思考讨论对比下表,你对氢键的强度有怎样的认识?二、氢键氢键不是化学键,而是特殊的分子间作用力,其键能比化学键弱,比范德华力强。二、氢键思考讨论实验证实,氢键不仅存在于分子之间,也存在于分子内。观察以下两种氢键,推测这两种物质的熔沸点高低。熔点:2℃沸点:115℃熔点:196.5℃沸点:246.6℃邻羟基苯甲醛对羟基苯甲醛当形成分子内氢键时,物质的熔、沸点将下降。当形成分子间氢键时,物质的熔、沸点将升高。总结:范德华力、氢键、共价键的对比范德华力氢键共价键作用微粒分子H与N、O、F原子特征无方向性和饱和性有方向性和饱和性有方向性和饱和性强度共价键>氢键>范德华力影响因素①相对分子质量②分子的极性X—H…Y强弱与X和Y的电负性有关成键原子半径和共用电子对数目。键长越小,键能越大,共价键越稳定观察思考不溶与溶解现象实验探究1.CCl4与水为什么分层?2.I2为什么从水中转移到CCl4中?在一个小试管里放入一小粒碘晶体,加入约5mL蒸馏水,观察碘在水中的溶解性(若有不溶的碘,可将碘水溶液倾倒在另一个试管里继续下面的实验)。在碘水溶液中加入约1mL四氯化碳(CCl4),振荡试管,观察碘被四氯化碳萃取,形成紫红色的碘的四氯化碳溶液。
再向试管中加入1mL浓碘化钾(KI)水溶液,振荡试管,溶液的紫色变浅。这是由于在水溶液里可发生如下反应:I2+I-
I3-观察思考影响物质溶解性的因素1.分子结构——“相似相溶”规律。非极性分子极性分子碘和四氯化碳都是非极性分子,水是极性分子。非极性溶质(碘)一般能溶于非极性溶剂,而难溶于极性溶剂。观察思考2.氢键——如果溶质与溶剂之间能形成氢键,则溶解度增大。——分子结构相似,“相似相溶”水和甲醇分子结构相似水甲醇戊醇观察思考3.反应——溶质与水发生可逆反应,如SO2与H2O反应生成H2SO3,CO2与H2O反应生成H2CO3等,可增大其溶解度。4.外界条件——温度、压强等。观察思考极易溶易溶可溶或能溶难溶或不溶气体NH3HX、SO2CO2Cl2H2SO2、H2、CH4、CH3Cl、C2H6、C2H4溶解度7004012.262.6\下表为室温、常压下,气体在水中的溶解度:观察思考2.NH3、H2S、H2O分子为极性分子,同为极性分子,为什么溶解度NH3为什么远大于H2S呢?1.为什么NH3的溶解性这么好,而H2,CH4几乎不溶?水是极性溶剂,极性溶质(NH3)比非极性溶质(H2,CH4)在水中的溶解度大。氨分子与水分子之间存在大量氢键,使得氨分子的溶解度远大于硫化氢。观察思考
自然界的生命体中存在许多左右对称的形态思考讨论你的左右手能够完全重叠么?这些互为镜像关系的物质能否完全重叠?镜子里的“自己”和现实中的自己左右相反、完全对称。互为镜像关系,但又不能重叠的现象,称之为“手性现象”。活动·探究活动·探究动手活动根据CH2ClBr、CHFClBr分子模型,制作其镜像分子的模型。并思考以下问题:(1)互为镜像关系的分子能否完全重叠?他们是同种分子吗?(2)什么样的分子具有手性现象呢?思考讨论1.互为镜像的分子可以是同一种分子,也可以是两种不同的分子。2.互为镜像,但不能重叠的两种分子,有什么结构特点?同一个碳原子上连有四个不同的原子或基团思考讨论手性碳原子同一个碳原子上连有四个不同的原子或基团。该碳原子称为手性碳原子(不对称碳原子)。形成简单手性分子需满足的条件(结构特点):思考讨论一对分子,他们的组成和原子的排列方式完全相同,但如同左手和右手一样互为镜像,在三维空间里不能重叠,这对分子互称手性异构体有手性异构体的分子称为手性分子资料卡片资料卡片2001年,诺贝尔化学奖授予三位用手性催化剂生产手性药物的化学家,用他们的方法可以只得到或者主要得到一种手性分子。这种独特的方法称为手性合成。资料卡片资料卡片催化剂催化剂不产生不匹配的手性产物合成匹配的手性产物手性催化剂只催化或者主要催化一种手性分子的合成,可以比喻成握手,手性催化剂像迎宾的主人伸出右手,被催化合成的手性分子像客人,总是伸出右手去握。资料卡片资料卡片
温馨提示
- 1. 本站所有资源如无特殊说明,都需要本地电脑安装OFFICE2007和PDF阅读器。图纸软件为CAD,CAXA,PROE,UG,SolidWorks等.压缩文件请下载最新的WinRAR软件解压。
- 2. 本站的文档不包含任何第三方提供的附件图纸等,如果需要附件,请联系上传者。文件的所有权益归上传用户所有。
- 3. 本站RAR压缩包中若带图纸,网页内容里面会有图纸预览,若没有图纸预览就没有图纸。
- 4. 未经权益所有人同意不得将文件中的内容挪作商业或盈利用途。
- 5. 人人文库网仅提供信息存储空间,仅对用户上传内容的表现方式做保护处理,对用户上传分享的文档内容本身不做任何修改或编辑,并不能对任何下载内容负责。
- 6. 下载文件中如有侵权或不适当内容,请与我们联系,我们立即纠正。
- 7. 本站不保证下载资源的准确性、安全性和完整性, 同时也不承担用户因使用这些下载资源对自己和他人造成任何形式的伤害或损失。
最新文档
- 冠心病合并糖尿病饮食指南
- 税务师考试2018课件
- 逻辑思维模式培训课件
- 县2025年大棚蔬菜基地建设实施方案
- 海水晶项目可行性研究报告
- 2025年中国北京市房地产行业市场供需格局及投资规划建议报告
- 2025年 昭通市焊工操作证理论考试练习题附答案
- 2025年 绵阳市游仙区定向招聘社区专职工作人员考试试题附答案
- 2025-2030年中国猕猴桃果汁饮料行业深度研究分析报告
- 中国泡桐木原木行业市场全景分析及投资策略研究报告
- 2024年机关事业单位工人汽车驾驶员高级技师国家题库练习题答案
- 村级积分制管理
- Nikon尼康D3100中文说明书
- 国家开放大学2024春《1494员工劳动关系管理》期末考试真题及答案-开
- DBJ∕T 13-234-2024 不发火建筑地面应用技术标准
- 2024年新疆中考地理真题卷及答案
- 人教版初三物理总复习电学专题复习教学设计
- 项目风险记录及跟踪表
- 2024年越南氮化铝陶瓷基板行业现状及前景分析2024-2030
- DL∕T 5158-2012 电力工程气象勘测技术规程
- 2024年浙江宁波慈溪市民政局及所属事业单位招聘编外用工6人历年(高频重点提升专题训练)共500题附带答案详解

评论
0/150
提交评论