



版权说明:本文档由用户提供并上传,收益归属内容提供方,若内容存在侵权,请进行举报或认领
文档简介
专题04金属与酸、金属与盐溶液的反应
考点考向
一、金属与酸反应的定量分析
二、金属活动性顺序的判断
三、金属活动性顺序的实验设计与探究
四、应用金属活动性北页序判断金属与酸(盐)反应后溶液(滤杂)成分
助反应的定量分析
本考点一般考查的知识点有:①一定量的金属混合物与足量酸反应,生成一定量H2,根据H2
的量分析金属混合物的组成;②等质量不同金属分别与等质量等浓度的同种(或不同种)酸反
应,分析剩余物的质量大小;③利用坐标图分析同质量(或不同质量)的金属与等量(或不等
量)的酸反应后有关结论的正误判断等。一般在选择题或计算题中呈现。
一、金属不足(横坐标为时间)
题眼
等质量的Mg、Al、Zn、Fe四种金属
Zn
时间
解题思路
1.金属不足,酸就一定过量,化学反应中产物的量永远由量不足的物质决定,虽然题目中所给金属质量相
同,但是因为相对原子质量不同,则生成氢气的质量一定不同。
2.斜率代表:产生氢气的速度(由金属活动性]顺序决定)。
3.产生氢气的总质量由相等价态的金属相对质量决定(铝等价为2价后相对质量为18)。
二、金属不足(横坐标为金属质量)
氢
气
质
量
金属质量
解题思路
1.因为酸足量,所以没有拐点。
2.直线的斜率代表:等质量的金属产生氢气的量。
注意:(1)金属的活动性决定了金属与酸反应的速率,金属越活泼,与酸反应的速率越大,图像中斜线的
倾斜度越大(M的活动性强于N);
(2)金属的相对原子质量与化合价决定了金属与酸反应生成氢气的多少,当两种金属成盐时的化合
价相同时,等质量的两种盐中相对原子质量越小的,生成的氢气越多,图像中的拐点越高(M的相对原子
质量小于N)。
三、足量金属等量酸
横坐标为时间
时间
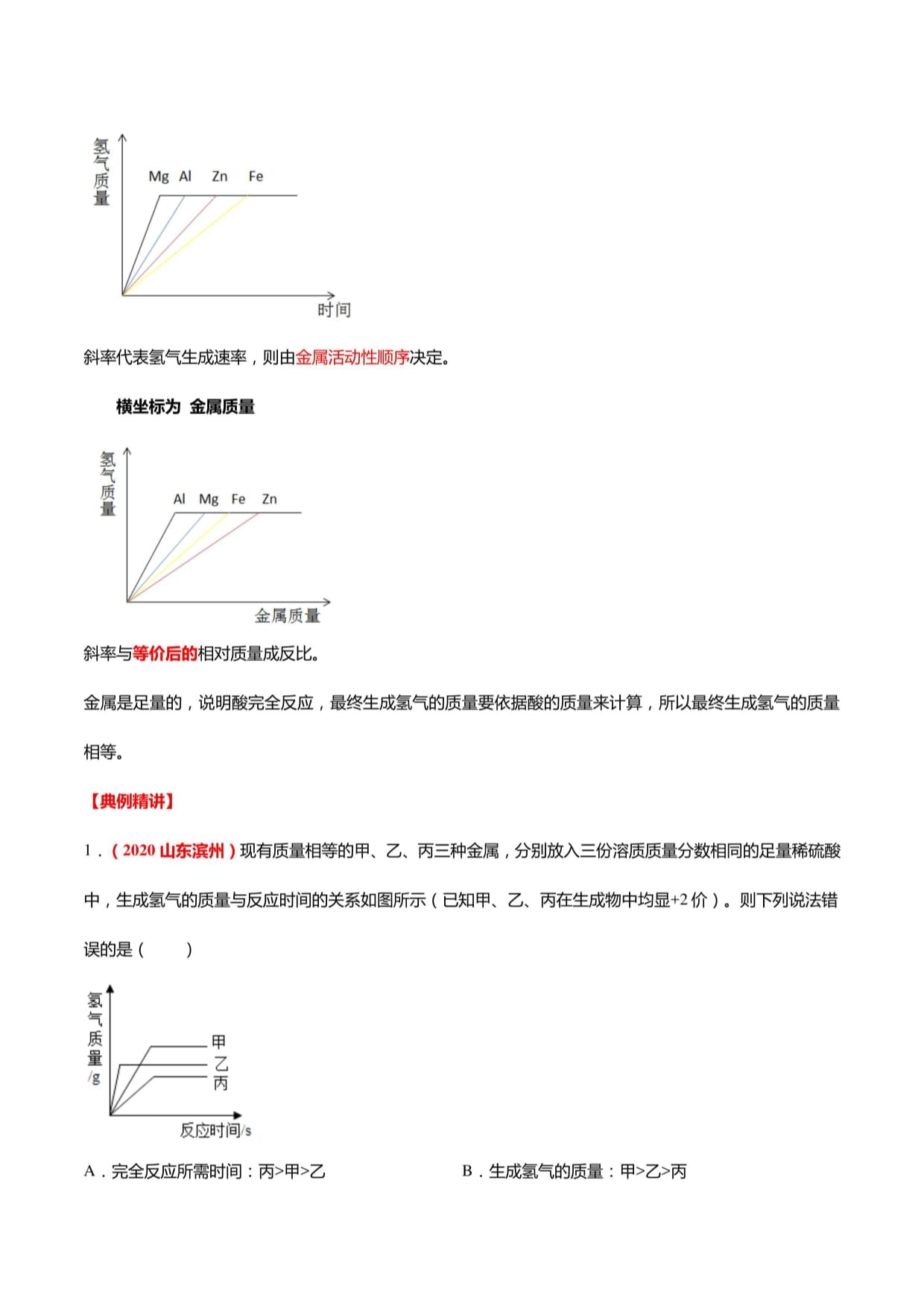
斜率代表氢气生成速率,则由金属活动性顺序决定。
横坐标为金属质量
氢
气
质
Mg
量AlFezn
金属质量
斜率与等价后的相对质量成反比。
金属是足量的,说明酸完全反应,最终生成氢气的质量要依据酸的质量来计算,所以最终生成氢气的质量
相等。
【典例精讲】
1.(2020山东滨州)现有质量相等的甲、乙、丙三种金属,分别放入三份溶质质量分数相同的足量稀硫酸
中,生成氢气的质量与反应时间的关系如图所示(已知甲、乙、丙在生成物中均显+2价)。则下列说法错
反应时间,s
A.完全反应所需时间:丙>甲>乙B.生成氢气的质量:甲>乙>丙
c.相对原子质量:乙〉丙呻D.消耗硫酸的质量:甲>乙>丙
【答案】C
【解析】A.由题意甲、乙、丙三种金属分别与三份溶质质量分数相同的足量稀硫酸反应,金属完全反应,
根据生成氢气的质量与反应时间的关系图可知,金属乙反应的氢气质量最先达到最大值,其次是金属甲,
最后是金属丙,即金属乙最先反应完,其次是金属甲,金属丙最后反应完,因此完全反应所需时间的关系
为丙>甲>乙,A选项说法正确,不符合题意;B.如图所示曲线平行于x轴时,生成的氢气质量达到最大值,
三种金属生成氢气的质量甲最大,其次是乙,最小的是丙,即生成氢气的质量甲>乙>丙,B选项说法正确,
不符合题意;C.由题意已知甲、乙、丙在生成物中均显+2价,若金属元素的符号为M,与稀硫酸反应的
通式为M+H'SOLMSO,+H2T,设金属的相对原子质量为x,金属的质量为m金属,生成氢气的质量为
m氢气,根据方程式可知力二」里,贝U有户——,已知甲、乙、丙三种金属的质量相等,则金属的相
对原子质量x与生成氢气的质量成反比,如图所示生成氢气的质量关系为甲>乙>丙,三种金属的相对原子
质量关系为甲〈乙〈丙,C选项说法错误,符合题意;
D.由题意已知甲、乙、丙在生成物中均显+2价,若金属元素的符号为M,与稀硫酸反应的通式为
M+H2SO4=MSO4+H2T,由方程式可知生成的氢气中的氢元素全部来自于硫酸,根据质量守恒定律元素
守恒,生成的氢气质量越大,消耗的硫酸质量越大,如图所示生成氢气的质量关系为甲>乙>丙,消耗硫酸
的质量关系为甲>乙>丙,D选项说法正确,不符合题意。故选C。
2.(2020湖北孝感)现有某铁样品5.6g,含有的杂质为镁、锌、铜中的两种或三种。向其中逐渐加入溶
质质量分数为9.8%的稀硫酸,产生氢气质量与加入稀硫酸质量的关系如下图所示。则下列结论正确的个数
是()
①恰好完全反应时,一定没有固体剩余
②X的值为0.2
③铁样品中可能含有镁
®M点对应的溶液中含有2种或3种溶质
A.1个B.2个
C.3个D.4个
【答案】A
【解析】100g稀硫酸,恰好完全反应,生成氢气质量,消耗铁镁锌的质量分别为:
HSOFeHSOMgHSOZnHSO
24H2242424
982569824986598
100gx9.8%0.2gx100gx9.8%y100gx9.8%z100gx9.8%
x=5.6gy=2.4gz=6.5g
和100g稀硫酸反应的金属5.6g,可能杂质是镁和铜,可能是镁、锌,可能是镁、锌、铜的混合物。①假
如是镁、锌、铜的混合物,恰好完全反应时,一定有固体剩余,选项说法错误。②由分析可知,生成氢气
质量0.2g,x的值为0.2,选项正确。③由分析可知,样品中含有杂质可能是镁和铜,可能是镁锌,可能
是镁锌铜的混合物,样品中一定有镁,选项说法错误。④M点表示硫酸过量,样品中含有杂质可能是镁和
铜,可能是镁锌,可能是镁锌铜的混合物,对应的溶液中含有的溶质是硫酸,硫酸亚铁,硫酸镁,可能还
含有硫酸锌,选项说法错误。故正确说法一个,故选A。
3.(2020山东济宁)在两只烧杯中分别放入相同质量的镁、锌两种金属,然后向两只烧杯中分别倒入相同
质量、相同质量分数的稀硫酸,反应产生氢气的质量与消耗硫酸的质量关系如图。综合以上信息得到以下
结论,合理的是()
H2的
质
量
g
0消耗H:scu的质量g
A.从图象可以看出,金属镁比金属锌的活动性强
B.若两种金属都有剩余,二者得到的氢气质量相同
C.若硫酸有剩余,二者得到氧气的质量相同
D.若两种金属完全溶解,二者消耗硫酸的质量相同
【答案】B
【解析】A.图像体现的是产生氢气质量与消耗硫酸质量之间的关系,没有体现时间关系,无法比较镁、锌
反应的速率,无法得出镁和锌的活动性强弱,说法错误;B.若两种金属都有剩余,则消耗的硫酸质量相等,
根据氢元素质量守恒,产生的氢气均来自硫酸中的氢元素,故二者得到的氢气质量相同,说法正确;C.若
Mg+H2SO4=MgSO4+H2TZn+H2SO4=ZnSO4+H2T
硫酸有剩余,根据可知,相同质量的镁、锌
242652
Mg+H,SO=MgSO+H,T
产生氢气的质量为:镁〉锌,说法错误;D.若两种金属完全溶解,根据2;9844
Zn+HOSO4=ZnSO4+H,T
6598可知’相同质量的镁、锌与硫酸反应’消耗硫酸的质量为:镁〉锌,说法错
误。故选B。
4.(2019广东省卷)取一定量打磨后的铝片于某容器中,再逐渐加入稀盐酸,加入稀盐酸的质量与有关量
的变化关系图错误的是()
H2的质量/g容器中溶液的质量/g
0^----------------------------►
稀盐酸的质量/g
B
【答案】B
【解析】盐酸和铝片反应生成氢气,但是每消耗54份质量的铝会生成6份质量的氢气,随着盐酸的不断加
入,当铝完全反应时,质量不再变化,B错误。
【典例精讲】
5.(2020北京市)下列不能与稀盐酸反应的金属是()
A.CuB.Zn
C.AlD.Mg
【答案】A
【解析】由于在这四种金属中,只有铜排在氢后,因此它不能和稀盐酸反应;故选A。
6.(2020山东滨州)已知A、B、C、D是四种金属单质,A能从B的硝酸盐溶液中置换出B,但A不能
与稀盐酸反应;相同条件下,C、D能与稀盐酸反应产生H2,且D比C反应剧烈。则四种金属的活动性由
强到弱的顺序是()
A.D>C>A>BB,A>B>C>D
C.B>A>C>DD.D>C>B>A
【答案】A
【解析】】A能置换出B,说明A比B活泼,C、D能与稀盐酸反应产生H?且D比C反应剧烈,而A不
能,说明D比C活泼,C比A活泼,故活动顺序为D>C>A>B,故选A.
7.(2020黑龙江鸡西)将金属镒(Mn)投入稀盐酸中,有气泡产生。将镁条插入硫酸镒溶液中,如果有
镒析出,则Mn、Mg、Cu的金属活泼性由强到弱的顺序是()
A.Mg、Mn、CuB.Mn、Mg、Cu
C.Cu、Mg、MnD.Cu、Mn、Mg
【答案】A
【解析】在金属活动性顺序表中,氢前的金属能置换出酸中的氢。将金属镒(Mn)投入稀盐酸中,有气泡
产生可知Mn>H;将镁条插入硫酸镒溶液中,如果有镒析出可知Mg>Mn;又在金属活动顺序表中Cu<H,
则Mn、Mg、Cu的金属活动性由强到弱的顺序是Mg>Mn>Cu,故选A。
8.(2020湖南邵阳)金属的用途很广,我们应该节约和保护金属资源,请用所学化学知识回答下列问题:
(1)铁制品长期裸露在室外易生锈,铁生锈实际上是铁与空气中的等发生化学反应的过程;
(2)为了预防铁制品生锈,我们常在其表面镀一层抗腐蚀的金属,但在镀金属之前,先要除去铁制品表面
的铁锈。用稀盐酸除去铁锈的化学反应方程式是____O
(3)将X、Z、Y三种金属片分别放入稀硫酸中,Y、Z表面有气泡产生,X没有明显现象,再把Y、Z分
别放入FeSCU溶液中,发现放入Y的FeSCU溶液逐渐变成无色,而放入Z的FeSC)4溶液和Z表面都没有明
显现象。根据上述实验判断,X、Y、Z三种金属的活动性由强到弱的顺序是____。
【答案】(1)氧气和水蒸气;(2)Fe2O3+6HCl=2FeCl3+3H2O;(3)Y>Z>X
【解析】(1)铁生锈实际上是铁与空气中的氧气和水蒸气等发生化学反应的过程,故填:氧气和水蒸气;
(2)铁锈的主要成分是氧化铁,氧化铁与稀盐酸反应生成氯化铁和水,该反应的化学方程式为:
Fe2O3+6HCl=2FeCl3+3H2O;(3)将*、Z、Y三种金属片分别放入稀硫酸中,Y、Z表面有气泡产生,
X没有明显现象,说明Y、Z能与稀硫酸反应,X与稀硫酸不反应,在金属活动性顺序里,Y、Z排在氢前,
X排在氢后,再把Y、Z分别放入FeSCU溶液中,发现放入Y的FeSCU溶液逐渐变成无色,而放入Z的FeSCU
溶液和Z表面都没有明显现象。说明Y能与硫酸亚铁反应,Z与硫酸亚铁不反应,在金属活动性顺序里,Y
排在铁前,Z排在铁后,故X、Y、Z三种金属的活动性由强到弱的顺序是:Y>Z>X。
[方法指导]
判断金属活动性顺序,可以根据金属与酸能否反应以及反应的剧烈程度("氢前能、氢后否、
越靠前、越剧烈")或根据金属能否与另一金属的盐溶液反应(前金换后金)。
图当金属活动性顺序的实验设计与探究
命题趋势
一般考查形式有:①给出几种金属,并设计几套实验方案,要求对设计方案进行正误判断;②
给出几种金属,猜想其金属活动性顺序,设计实验方案,并进行验证探究。一般在选择题、实
验探究题中出现,少量在填空题中呈现。
【典例精讲】
9.(2020湖北恩施)现有Al、Cu、Ag三种金属,限用一种试剂一次性就可以验证它们的金属活动性强弱,
则该试剂是()
A.CuSCU溶液B.稀H2s。4
C.AgNCh溶液D.A1C13溶液
【答案】A
【解析】A.铝能与硫酸铜反应生成硫酸铝和铜,有红色固体析出,说明铝比铜活泼,银与硫酸铜不反应,
无明显现象,说明铜比银活泼,可以验证它们的金属活动性强弱,符合题意;B.铝能与稀硫酸反应生成硫
酸铝和氢气,有气泡产生,说明在金属活动性顺序中,铝在氢前,铜、银都不与稀硫酸反应,无明显现象,
说明在金属活动性顺序里,铜、银排在氢之后,由此可推出在金属活动性顺序里,铝的金属活动性比铜、
银强,但是无法验证铜、银的金属活动性,不符合题意;C.铝能与硝酸银反应生成硝酸铝和银,有银白色
固体析出,说明铝比银活泼,铜能与硝酸银反应生成硝酸铜和银,有银白色固体析出,说明铜比银活泼,
但是无法验证铝、铜的金属活动性强弱,不符合题意;D.铜、银都不与氧化铝反应,无明显现象,说明铝
比铜、银活泼,但是无法验证铜、银的金属活动性顺序,不符合题意。故选Ao
10.(2020四川乐山)某同学参加实验操作考试,为验证镁、锌、铜三种金属的活动性顺序,他设计了以下
四种实验方案,其中能达到目的的是
A.将镁片、锌片分别放入Cu(NO3)2溶液中
B.将锌片、铜片分别放入Mg(NO3)2溶液中
C.将镁片分别放入Zn(NO3)2溶液、Cu(NO3)2溶液中
D.将镁片、锌片、铜片分别放入稀盐酸中
【答案】D
【解析】A.将镁片、锌片分别放入Cu(NO3)2溶液中,观察到镁片、锌片的表面均有红色固体出现,说
明镁、锌的活动性都比铜强,但无法判断镁、锌活动性的强弱,选项错误;B.将锌片、铜片分别放入Mg
(NO3)2溶液中,锌片、铜片上均无明显变化,说明镁的活动性比锌、铜都强,但无法判断锌、铜活动性
的强弱,选项错误;c.将镁片放入Zn(N03)2溶液中,镁片表面有银白色固体出现,将镁片放入
Cu(NO3)2溶液中,镁片表面出现红色固体,说明锌的活动性比锌、铜都强,但无法判断锌、铜活动性的
强弱,选项错误;
D.将镁片、锌片、铜片分别放入稀盐酸中,观察到镁片表面产生气泡的速率最快,锌片表面出现气泡的速
率次之,而铜片表面没有明显变化,证明三种金属的活动性为镁>锌>铜,选项正确,故选D。
11.(2020山东青岛)某同学为验证镁、铁、铜、银的金属活动性顺序,设计了下图所示的四个实验(金
属片均已打磨,且其形状大小相同;实验①②③所用盐酸的溶质质量分数和体积均相同)。下列分析不正
确的是()
铜片
・硝酸银溶液
A.对比实验①②反应的剧烈程度,能判断出镁和铁的金属活动性强弱
B.分析实验②④现象,能判断出铁、铜、银的金属活动性强弱
C.分析实验④的现象,能判断出铜和银的金属活动性强弱
D.分析四个实验的现象,能判断出镁、铁、铜、银的金属活动性顺序
【答案】B
【解析】A.金属与酸反应,反应越剧烈,金属活动性越强,对比实验①②反应的剧烈程度,能判断出镁和
铁的金属活动性强弱,A正确;B.②稀盐酸和铁反应,生成氯化亚铁和氢气,说明金属活动性,铁在氢前,
④铜和硝酸银反应,生成硝酸铜和银,说明金属活动性铜大于银,不能判断出铁、铜的金属活动性强弱,B
错,符合题意;C.活动性强的金属,能和活动性弱的金属盐溶液反应,分析实验④的现象,能判断出铜和
银的金属活动性强弱,C正确;D.对比实验①②反应的剧烈程度,能判断出镁和铁的金属活动性强弱,镁
>铁>氢,实验③铜和稀盐酸不反应,说明活动性氢〉铜,活动性强的金属,能和活动性弱的金属盐溶液
反应,分析实验④的现象,活动性铜>银,故金属活动性,镁〉铁>铜>银,D正确。故选Bo
12.(2020云南昆明)为验证Mg、Cu、Sn的金属活动性顺序,不可选用的一组物质是()
A.MgCL溶液、Cu、SnB.Mg、Cu、SnCb溶液
C.Mg、Sn、Cu、盐酸D.MgCL溶液、Sn、CuCL溶液
【答案】A
【解析】A.MgCb溶液与Cu、Sn均不反应,不能验证Mg、Cu、Sn的金属活动性顺序;B.Mg与SnCh
溶液反应生成略带蓝色的Sn,而Cu与SnCb溶液不反应,能验证Mg、Cu、Sn的金属活动性顺序;C.Mg、
Sn与盐酸均能反应产生氢气,且镁与盐酸反应更加剧烈,Cu与盐酸不反应,能验证Mg、Cu、Sn的金属活
动性顺序;D.MgCb溶液与Sn不反应,可知金属活动性Mg>Sn,Sn、CuCb溶液反应,有红色的铜生成,
可知金属活动性Sn>Cu,能验证Mg、Cu、Sn的金属活动性顺序;故选Ao
13.(21020甘肃平凉)有X、Y、Z三种金属,如果把X和Y分别放入稀硫酸中,X溶解并产生气泡,Y
不反应;如果把丫和Z分别放入硝酸银溶液中,在Y表面有银白色物质析出,而Z没有变化。根据以上实
验事实,判断这三种金属的活动性由强到弱的顺序为()
A.X、Y、ZB.Z、Y、X
C.Y、X、ZD.X、Z、Y
【答案】A
【解析】有X、Y、Z三种金属,如果把X和Y分别放入稀硫酸中,X溶解并产生气泡,说明X的活动性
最强,如果把丫和Z分别放入硝酸银溶液中,在Y表面有银白色物质析出,而Z没有变,说明Y的活动性
大于银,而银的活动性大于Z。故选A。
14.(2020甘肃金昌)某同学为验证铁、铜、银三种金属的活动性顺序,他设计了以下四种实验方案,其中
能达到目的是()
A.将Fe、Cu分别加入AgNO3溶液中
B.将Fe、Cu、Ag分别加入稀盐酸中
C.将Fe分别加入CuS04、AgNCh溶液中
D.将Fe、Ag分别加入CuSO4溶液中
【答案】D
【解析】A.铁、铜都能与AgNCh溶液反应,证明铁、铜的活动性比银强,但不能比较铁、铜的活动性的
强弱,故该方案不能达到目的;B.铁和稀盐酸反应,铜、银和稀盐酸不反应,而则得出:铁〉铜、银,但
不能比较铜、银的活动性的强弱,故该方案不能达到目的;C.铁与CuSCU、AgNCh溶液反应,说明了活动
性铁〉铜、银,但不能比较铜、银的活动性的强弱,故该方案不能达到目的;D.铁与CuS04溶液反应置换
出铜,说明了活动性铁〉铜;银与CuSO4溶液不反应,说明了活动性铜〉银,由此可得的三种金属活动性
铁>铜>银,故该方案能达到目的。故选D。
[方法指导]
金属活动性顺序的实验设计:
(1)两种金属
①把一种金属放入另一种金属的盐溶液中。②把两种金属放入稀盐酸(或稀硫酸)中(至少有
一种金属排在氢前)。
(2)三种金属
①把活动性居中的金属放入两边的金属盐溶液中,简称“中间金属,两边盐”。
②把活动性处于两边的金属放入居中的金属盐溶液中,简称“两边金属,中间盐”。
好为应用金属活动性顺序判断金属与
(盐)反应后溶液(滤杂)成分
本考点的主要考查方式有:以文字叙述(或框图流程)提供一种(或几种)金属与几种盐(或
酸、盐)混合物反应,或几种金属与一种盐(或酸)反应后,对滤液、滤渣中的成分进行判断
等。一般在选择题或填空题中呈现。
两种金属
例:Fe与CuS04反应
铁少量——代表全部消耗并且铜也没有完全置换出
则滤液中:FeSO4CuSO4滤纸上剩余固体:Cu
铁适量一铁全部消耗,铜全部被置换出
则滤液中:CuSO4滤纸上剩余固体:Cu
铁过量一铁不但把铜全部置换出来,且本身有单质剩余
则滤液中:CuSO4滤纸上剩余固体:Fe、Cu(先写剩余的,以防遗漏)
三种金属
例:ZnFeSO4CuCl2
Zn少量分3种情况考虑
1,只置换出部分Cu(金属活动性顺序表中距离远的先反应)
滤液:FeSO4CuCl2ZnCl2(先写剩的,再写生成的)
滤渣:Cu
2.恰好Cu全部被置换出来
滤液:FeSCUZnCl2
滤渣:Cu
3.部分Fe被置换出
滤液:FeSO4ZnCb
滤渣:CuFe
Zn恰好足量
滤液:ZnCh
滤渣:CuFe
Zn过量
滤液:ZnCl2
滤渣:ZnCuFe
【典例精讲】
15.(2020黑龙江牡丹江)有一包固体混合物,其中含有硝酸银、硝酸铜、硝酸镁及铁粉,加入足量的水过
滤,下列描述的情形不可能存在的是()
A.滤纸上有Ag、Cu、Fe,滤液中有Fe2+、C#+、Mg2+
2++
B.滤纸上有Ag、Cu,滤液中有Fe2+、Cu2+、MgXAg
C.滤纸上有Ag,滤液中有Fe2+、Cu2+、Mg2+、Ag+
D.滤纸上有Ag、Cu,滤液中有Fe2+、Cu%、Mg2+
【答案】AB
【解析】硝酸银、硝酸铜、硝酸镁及铁粉的混合溶液中加入一些铁粉,镁>铁>铜>银,铁不会与硝酸镁反应,
故滤液中一定含有硝酸镁,铁与硝酸银反应生成硝酸亚铁和银,铁与硝酸铜反应生成硝酸亚铁和铜,生成
的铜与硝酸银能反应生成硝酸铜和银,铁先消耗硝酸银,硝酸银完全反应后,铁再消耗硝酸铜。A.铁的金
属活动性强于铜,滤渣中有铁,滤液中不可能含有铜离子,A错,符合题意。B.铜的金属活动性强于银,
滤渣中有铜,滤液中不可能含有银离子,B错,符合题意。C.假如铁粉不足,只和部分硝酸银反应,此时
滤纸上有Ag,滤液中有Fe2+、Cu2+、Mg2+、Ag+,C正确。D.铁和硝酸银反应完之后又和部分硝酸铜反
应,此时滤纸上有Ag、Cu,滤液中有Fe2+、Cu2\Mg2+,D正确。故选AB。
16.(2020广西北部湾)金属材料广泛应用于生产、生活中。
(1)用铜作导线,利用了铜的延展性和_______________性。
(2)镁是一种活泼的金属,请写出镁与稀盐酸反应的化学方程式______________________。
(3)将等质量的A、B、C三种金属(生成物中金属元素均为+2价),分别放入质量分数相等且足量的稀
盐酸中,产生H2的质量与反应时间的关系如图所示。A、B、C三种金属中,金属活动性由强到弱的顺序是
,相对原子质量最大的是____________________»
(4)向一定量的硝酸银和硝酸亚铁混合溶液中加入mg锌粉,充分反应后过滤,得到滤液和滤渣。下列分
析正确的是_______________(填字母序号)。
A若滤渣只含一种金属,则滤液中的溶质只有三种
B若滤液中含有两种金属离子,则滤渣中的固体只有两种
C若最终得到的滤渣质量仍为mg,则滤液中溶质最多有两种
D若向滤渣中加入稀盐酸,有气泡产生,则滤液中的溶质最多有两种
【答案】(1)导电;(2)Mg+2HCl=MgCl2+H2T;(3)A>C>B;C;(4)C、D
【解析】(1)用铜作导线,利用了铜的延展性和导电性,故填:导电。(2)镁和稀盐酸反应生成氯化镁
和氢气,化学方程式为Mg+2HC1=MgCl2+H2T,故填:Mg+2HC1=MgCl2+H2T0(3)由图可
知将等质量的A、B、C三种金属(生成物中金属元素均为+2价),分别放入质量分数相等且足量的稀盐酸
中,A先反应完,C再反应完,B最后反应完,故金属活动性A>OB;化合价相等时,等质量金属完全反
应相对原子质量越小,生成氢气越多,相对原子质量最大,生成氢气最少,故C生成氢气最少,相对原子
质量最大,故填:A>OB;CO(4)A.向一定量的硝酸银和硝酸亚铁混合溶液中加入mg锌粉,锌会先
和硝酸银反应生成硝酸锌和银,再和硝酸亚铁反应,生成铁和硝酸锌,若滤渣只含一种金属,一定是银,
可能硝酸银部分反应,滤液溶质硝酸银,硝酸亚铁和硝酸锌,也可能硝酸银完全反应,滤液溶质硝酸亚铁
和硝酸锌,故A错。B.向一定量的硝酸银和硝酸亚铁混合溶液中加入mg锌粉,锌会先和硝酸银反应生成
硝酸锌和银,再和硝酸亚铁反应,生成铁和硝酸锌,若滤液中含有两种金属离子,故溶质为硝酸锌和硝酸
亚铁,离子为锌离子和亚铁离子,硝酸亚铁可能和锌没反应,也可能部分反应,滤渣固体可能为银,也可
Zn+2AgNO3=2Ag+Zn(NO3)2Zn+Fe(NO3)2=Fe+Zn(NO3)2
能为银和铁,B错。C由化学方程
,652166556
式可知65份质量锌生成216份质量银,65份质量锌生成56份质量铁,向一定量的硝酸银和硝酸亚铁混合
溶液中加入mg锌粉,若最终得到的滤渣质量仍为mg,说明锌和硝酸银以及硝酸亚铁都发生了反应,硝酸
亚铁可能有剩余也可能完全反应,硝酸亚铁部分反应溶质为硝酸锌和硝酸亚铁,硝酸亚铁完全反应,溶质
是硝酸锌,则滤液中溶质最多有两种,C正确。D.若向滤渣中加入稀盐酸,有气泡产生,滤渣中一定有铁,
铁和稀盐酸生成气体,此时硝酸亚铁可能完全反应,也可能部分反应,硝酸亚铁部分反应溶质为硝酸锌和
硝酸亚铁,硝酸亚铁完全反应,溶质是硝酸锌,则滤液中溶质最多有两种,D正确。故选CD。
17.(2020辽宁鞍山)将一定质量的铁粉加入到Mg(NO3)2、AgNCh的混合溶液中,充分反应后过滤,
得到滤液和滤渣。向滤液中加入稀盐酸,无明显现象。下列叙述正确的是()
A.滤液中一定含有Mg2+和Fe3+
B.滤液中含有Mg2+和Ag+
C.滤渣中一定含有Ag
D.滤渣中可能含有Mg
【答案】c
【解析】铁的金属活动性比银强,比镁弱,将一定质量的铁粉加入到Mg(NO3)2、AgNC»3的混合溶液中,
铁不能与Mg(NO3)2溶液反应,铁与AgNCh反应生成硝酸亚铁和银,充分反应后过滤,得到滤液和滤渣。
向滤液中加入稀盐酸,无明显现象,说明滤液中不含硝酸银。A.铁与硝酸银反应生成硝酸亚铁和银,铁与
硝酸镁不反应,故滤液中一定含有硝酸亚铁和硝酸镁,故滤液中一定含镁离子和亚铁离子,不含铁离子,
故选项说法错误;B.向滤液中加入稀盐酸,无明显现象,说明滤液中不含硝酸银,滤液中一定含有Mg2+
和Fe2+,一定不含银离子,故选项说法错误。C.铁与AgNCh反应生成硝酸亚铁和银,滤渣中一定含有Ag,
故选项说法正确;D.铁不能与Mg(NO3)2溶液反应,滤渣中一定不含Mg,故选项说法错误。
故选C。
18.(2020辽宁本溪)将一定质量的Zn放入Cu(NO3)2和AgNO3的混合溶液中,充分反应后过滤,得到
滤渣和滤液,下列说法错误的是()
A.滤渣中只含有Ag时,滤液一定呈蓝色
B.滤渣中含有Cu和Ag时,滤液一定呈无色
C.滤渣中含有Zn时,滤液中的溶质只有Zn(NO3)2
D.滤渣中含有Cu时,滤液中的溶质一定没有AgNO3
【答案】B
【解析】A.滤渣中只含有Ag时,说明锌没有和Cu(NO3)2反应,滤液中有
温馨提示
- 1. 本站所有资源如无特殊说明,都需要本地电脑安装OFFICE2007和PDF阅读器。图纸软件为CAD,CAXA,PROE,UG,SolidWorks等.压缩文件请下载最新的WinRAR软件解压。
- 2. 本站的文档不包含任何第三方提供的附件图纸等,如果需要附件,请联系上传者。文件的所有权益归上传用户所有。
- 3. 本站RAR压缩包中若带图纸,网页内容里面会有图纸预览,若没有图纸预览就没有图纸。
- 4. 未经权益所有人同意不得将文件中的内容挪作商业或盈利用途。
- 5. 人人文库网仅提供信息存储空间,仅对用户上传内容的表现方式做保护处理,对用户上传分享的文档内容本身不做任何修改或编辑,并不能对任何下载内容负责。
- 6. 下载文件中如有侵权或不适当内容,请与我们联系,我们立即纠正。
- 7. 本站不保证下载资源的准确性、安全性和完整性, 同时也不承担用户因使用这些下载资源对自己和他人造成任何形式的伤害或损失。
最新文档
- 2026潞安化工集团校招试题及答案
- 2025年金融证券服务流程手册
- 21 声音的产生与传播
- 《小学美术教学创新实践案例库构建:基于教师教学画像的实证分析》教学研究课题报告
- 2026年房地产融资的风险管理策略
- 4一元一次不等式组
- 护理查对制度与信息技术结合
- 2026年区块链供应链管理创新报告及未来五至十年透明化发展报告
- 2026年电气火灾后的环境安全评估
- 2026年创造动态照明效果的设计技巧
- 小学数学低年级学生学情分析
- 水利水电工程建设用地设计标准(征求意见稿)
- 供电一把手讲安全课
- 本科实习男护生职业认同感调查及影响因素分析
- T-GDWCA 0035-2018 HDMI 连接线标准规范
- 合肥机床行业现状分析
- 面板堆石坝面板滑模结构设计
- 无人机装调检修工培训计划及大纲
- 国家开放大学《森林保护》形考任务1-4参考答案
- GB 31604.1-2023食品安全国家标准食品接触材料及制品迁移试验通则
- 殡葬服务心得体会 殡仪馆工作心得体会

评论
0/150
提交评论