



版权说明:本文档由用户提供并上传,收益归属内容提供方,若内容存在侵权,请进行举报或认领
文档简介
专题六科学探究
类型一有关反应后物质成分的探究
1.(2019齐齐哈尔)某班同学为验证碳酸钠的化学性质,向盛有碳
酸钠的试管中加入一定量的稀盐酸,迅速用带导气管的橡胶塞塞紧试管口,并将导管
另一端通入盛有澄清石灰水的试管中(如图所示)。请回答下列问题:
(1)如图试管中澄清石灰水变浑浊,写出该反应的化学方程式土
Ca(OH”=CaCChl+出0。
(2)实验结束后,将两支试管中的所有物质倒入同一个废液缸中,充分反应后得到澄清
溶液。同学们对废液中溶质的成分进行如下探究(忽略二氧化碳的影响):
【提出问题】废液中溶质的成分是什么?
【做出猜想】猜想一:CaCL、NaCl和HC1
猜想二:CaCL、NaCl和Na2cO3
猜想三:CaCl2^»NaCl
【进行讨经过讨论,同学们一致认为猜想—二—是错误的。
【设计实验】请完成实验报告:
实验步骤实验现象实验结论
取少量废液于试管中,加入—立蛆邕产金气泡(灰溶果,由无色变氏或色欢
猜想一成立
匕桐、裱酸遇)_―一―他,■&上一咬时一)
【反思拓展】最终同学们确认了废液中溶质的成分。若将废液直接排入铸铁管道引起
的危害是—体东也下水、力樵管道(,理即可)你认为该废液的处理方法是_他2空堂里
雄/(或碟被轴、11氧化匐)港海凝■理达标后郴数(合理即可)_。
2.(2019滨州)钙元素是一种重要的金属元素,它可组成氯化钙、氢氧化钙等多种物质。
(1)氢化钙(CaHz)固体是登山运动员常用的能源提供剂。某实验探究小组的同学通过查
阅资料得知,氢化钙在常温下能与水反应生成氢氧化钙和氢气,请你写出该反应的化学方
程式CaHh+ZHzO=Ca(OH)2+2H2t。
(2)该实验探究小组将Na2c03溶液滴加到Ca(OH)2溶液中,充分反应后过滤,得到滤
渣和滤液,经检验滤渣的成分是碳酸钙。
【提出问题】滤液中溶质的成分是什么?
【猜想与假设】猜想一:NaOH
猜想二:NaOH和Ca(OH)2
猜想三:NaOH和Na2c:
猜想四:NaOH、Na2cO3和Ca(OH)2
经过讨论,大家认为猜想四不合理,原因是—碟破愈易年11化榜像小攻您(或碟鼠曲•&
氐果化犯不兴喜)
【实验过程】
实验步躲现象结论
步骤I:取滤液,向其中滴入适量
无一一说鑫猜想二不成立
Na2cCh溶液
步骤n:另取滤液,向其中加入足量篁
产生气泡猜想_恐_
,(合理/可)溶液
成立
【拓展延伸】在分析反应后所得物质的成分时,除考虑生成物外,还需考虑一以应电
是塔蛇量_。
3.(2019遂宁)草酸(H2c2O4)存在于自然界的植物中,在170C以上易分解,某校化学兴
趣小组为确定草酸分解产物,做如下探究。
【提出问题】草酸的分解产物是什么?
【猜想与假设】猜想①:COCO2
猜想②:COH2O
猜想③:CO2H2OH2
猜想④:COCO2H2O
经小组同学分析得出上述猜想一①一一定是错误的。
【查阅资料】无水硫酸铜是一种白色固体,遇水会变成蓝色。
【进行实验】该小组同学设计了如下的实验过程(部分固定装置已略去)。
然产,FeA
I无水T澄清t足量a浓T无i水r澄r清
硫酸石灰NaOH硫硫酸石灰
铜水溶液酸铜
ABCDEFG
实验步骤实验现象实验结论
将分解产物从左至右依次通过各装置
A中无水硫酸铜变蓝
B中澄清石灰水变浑浊猜想②错误
F中无水硫酸铜无变化G中澄清石灰
猜想④正确
水变浑浊
(1)装置C的作用_c去?混合气体中
问题解答
一二氧化碟—
(2)写出装置E中发生反应的化学方程
式Fe2()3+3CO_2Fe+
3CO2
【交流反思】为防止污染环境,该实验应增加尾气处理装置。
4.(2019赤峰)某校化学兴趣小组的同学在探究碱的化学性质时,完成了如下图所示的
两个实验。
逐渐加入
稀盐酸至
恰好反应'
0
0氢氧化钠溶液
不,(滴有酚酿)甲
碳酸钠
溶液'
0
0»,饱和
:二隹/石灰水乙
(1)甲实验中观察到的现象是一港俄,由红包变,无虫一。
(2)乙实验中发生反应的化学方程式为Na2cC>3+Ca(OH)2=CaCO3J+2NaOH.。
实验完毕后,小亮同学在整理仪器时,将上述实验后的废液倒入同一个洁净的废液缸
中,发现混合后的废液仍然浑浊并显红色,于是引起了他的质疑和探究兴趣。
【提出问题】混合废液中可能含有的碱性物质有哪些?
【作出猜想】他断定混合废液中一定含有氢氧化钠,理由是一碟破於布JL氧化弼反危
士氏H童化率―;并对是否含有其他碱性物质作出猜想:
猜想I:Na2c。3猜想II:Ca(OH)2
【实验验证】小亮认为只要用反应物(饱和石灰水和碳酸钠溶液)就可以验证猜想。于是
他对混合废液进行过滤,并取少量滤液进行了下列实验:
实验操作实验现象实验结论
适量的
1广
,彳沉能
卜滤液
M曷碳薇钠售版
猜想n不正确
[适量的
[「N溶液
产金的包
手滤液
1帮佬打石垄水
M
沉淀猜想I正确
【反思与交流】
验证完毕,小刚同学受到启发,于是他又设计了一个实验,进一步验证混合废液中含
有的碱性物质。他取一定量的滤液于试管中,然后逐滴滴加稀盐酸至过量,反应过程和产
生的现象如图所示。分析图像数据可以得出混合废液中含有的碱性物质一定是_基1些电
为碟曦钠_。
“生成气体的质量/g
0加入稀盐酸
的质勤g
【拓展应用】为了把以上废液安全排放,你的做法是
一瓢人造黄的黄碱至不嘉广金气体
5.(2019长沙)小华同学通过阅读课外资料得知,潜水艇中常用过氧化钠(Na2(h)作为供
氧剂,有关反应的化学方程式为:2Na2Ch+2CO2=2Na2co3+O2,2Na2O2+2H2O=
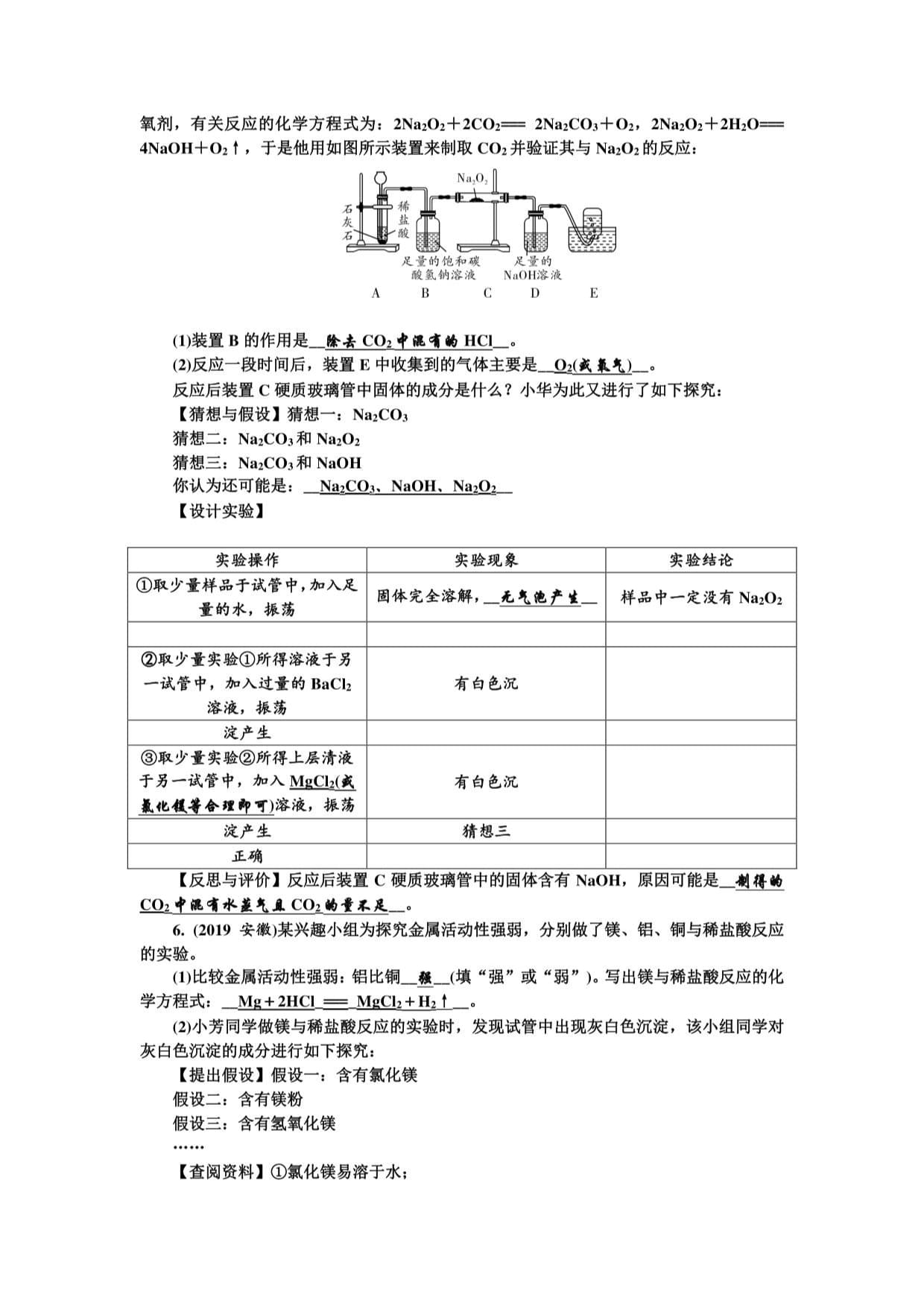
4NaOH+O2t,于是他用如图所示装置来制取CO2并验证其与NazCh的反应:
足量的饱和碳足量的
酸氢钠溶液NaOH溶液
ABCDE
(1)装置B的作用是_片去CO?中偎中的HQ_。
(2)反应一段时间后,装置E中收集到的气体主要是OX年收北
反应后装置C硬质玻璃管中固体的成分是什么?小华为此又进行了如下探究:
【猜想与假设】猜想一:Na2c03
猜想二:Na2cCh和Na2()2
猜想三:Na2cCh和NaOH
你认为还可能是:—83,NaOH、Na?。、
【设计实验】
实验操作实验现象实验结论
①取少量样品于试管中,加入足
固体完全溶解,_九人也产金—样品中一定没有NazOz
量的水,振荡
②取少量实验①所得溶液于另
一试管中,加入过量的BaCL有白色沉
溶液,振荡
淀产生
③取少量实验②所得上层清液
于另一试管中,加入MgCL(我有白色沉
鼠也铁船合理力可)溶液,振荡
淀产生猜想三
正确
【反思与评价】反应后装置C硬质玻璃管中的固体含有NaOH,原因可能是一旦电
CQ2中混守水荽入ACOz的4不足—。
6.(2019安徽)某兴趣小组为探究金属活动性强弱,分别做了镁、铝、铜与稀盐酸反应
的实验。
(1)比较金属活动性强弱:铝比铜_整_(填“强”或“弱”)。写出镁与稀盐酸反应的化
学方程式:Mg+2HCl=MgCL+H2f。
(2)小芳同学做镁与稀盐酸反应的实验时,发现试管中出现灰白色沉淀,该小组同学对
灰白色沉淀的成分进行如下探究:
【提出假设】假设一:含有氯化镁
假设二:含有镁粉
假设三:含有氢氧化镁
【查阅资料】①氯化镁易溶于水;
②在一定条件下,镁可与冷水缓慢反应。
【设计并进行实验】各取少量灰白色沉淀加入2支试管中,进行如下实验:
编号实验操作实验现象
实验1加入适量蒸储水,搅拌沉淀未见减少
实验2加入适量稀盐酸沉淀全部溶解,没有气泡产生
【得出结论】由实验1可知,假设_二_不成立;由实验2可知,沉淀中不含_处
假设三一可像应/_(填“成立”或“可能成立”或“不成立”).
【实验反思】实验后同学们请教老师得知,灰白色沉淀的主要成分是碱式氯化镁,碱
式氯化镁受热易分解产生氯化氢气体。于是小芳再取少量灰白色沉淀于试管中加热,并将
蘸有紫色石蕊溶液的滤纸条悬于试管口,预期的实验现象是—灌抵条或叁
(3)为探究镁与稀盐酸生成碱式氯化镁的条件,该小组同学进行了如下实验:在小烧杯
中加入一定量稀盐酸和去除氧化膜的镁带,观察实验现象,并测量溶液pH的变化。结果见
下表:
时间/
min024812162024
溶液
pH2.05.37.08.69.39.810.010.0
实验
镁带缓慢溶解,
镁带溶解较快,产生气泡速度减
现象—产生大量气泡,慢,溶液变浑浊,
无沉淀生成烧杯底部有灰白
色沉淀
根据表中信息回答下列问题:
①请描述溶液pH变化的规律并解释原因:一氤弄&京的、H,**pH由2.0〜10.0
更断槽4,银鸟用城城山,情奏狡魂能借液.pH/丈,jtK浦靶先后,黑箍候■&水布慢反位
②请对生成碱式氯化镁的条件提出猜想,并设计实验证明猜想:根条的依衣守关,
实般方案:合力取l_cm、2_cm、3_cm、4_fm8衣的去除•量化瓶的极冬于43铁管中,弃
各加入5mL5%的不力麒,苑金宴龄现4(合理用可)
类型二有关物质变质的探究
7.某兴趣小组的同学在老师的指导下,对一瓶没有塞橡皮塞的氢氧化钙溶液进行探究,
请你一起参与。
【提出问题】该氢氧化钙溶液是否全部变质?
【猜想与假设】猜想①:氢氧化钙溶液可能全部变质,变成碳酸钙。
猜想②:氢氧化钙溶液可能部分变质,其成分是_皂星四扑_蔓曳色
【实验探究】
实验步骤实验现象实验结论
取样于试管中,滴加稀盐酸有―一体_生成原溶液中一定有碳酸钙
另取样于试管中,滴加酚酬溶
溶液变成红色原溶液中一定有_基些色丝一
液
【实验结论】综合上述实验,你得出的结论是猜想—②—成立。
【反思拓展】(1)氢氧化钙露置于空气中易变质,原因是CO2+Ca(OH)2=CaCCh
I+H2Q(用化学方程式表示)。
(2)在分析化学反应的物质成分时,除了考虑生成物外,还需考虑的是—功根物是看中
8.(2019营口)化学实验小组的同学在实验室里发现桌上有瓶敞口放置已久的NaOH溶
液,他们对溶质的成分产生了探究的欲望。
【查阅资料】Ca2+和OIF在水溶液中不能大量共存
【提出问题】这瓶NaOH溶液一定变质了,其变质程度如何呢?
【提出猜想】猜想一:NaOH溶质部分变质
猜想二:NaOH溶液完全变质
【实验探究】
⑴氢氧化钠溶液变质的原因为2NaOH+CO?=NazCOL,H2O(用化学方程
式表。
(2)小华设计了如下实验进行探窕,请根据表中内容填写:
实验步骤现象结论
取少量NaOH溶液样品于试管中,向其中滴加过量的CaCL
步骤一产生白
溶液
色沉淀
步骤二过滤,向滤液中滴加酚配溶液酚酬溶
液变红猜想
成立
如果步骤一中白色沉淀由两种物质组成,则两种物质是CaCCh、Ca(OH)2(填化学
式);步骤二中根据酚歆溶液变红这一现象证明样品中含有(填字母)。
A.CaCl2B.Na2cO3
C.NaOHD.Na2cO3和NaOH
【实验反思】
(1)下列物质①BaCL溶液、②Ca(NO3”溶液、③Ca(OH”溶液、④Ba(OH”溶液,不能
替代步骤一中CaCL溶液的是一③④_(填序号)。
(2)步骤二中用另外一种试剂代替酚配溶液也能得出同样的结论,发生反应的化学方程
式为2NaOH+CuSO』=Na2sO4+Cu(OH)2」(或NaOH一扇其他4R4、铁换簿收
反瘗的方程或衲可)―。
9.(2019广安)中国医学著作博大精深,许多化学物质很早就出现在了我国医书中。如
李时珍的《本草纲目》中就有绿帆(FeSO4・7H2O)的相关记载。绿帆又名皂矶、青矶,性酸、
凉、无毒,主要药用功能是除湿、解毒、收敛、止血。
(1)请写出铁与稀硫酸反应的方程式Fe+H2sCh=FeSCh+H2t.
(2)某实验小组欲用久置的硫酸亚铁溶液制备绿研(FeSCh-7H2O)晶体,小明同学提出
该硫酸亚铁溶液可能变质了,于是进行了以下探究活动:
【查阅资料】
①FeSO」易被空气中的氧气氧化成FeMSO4)3而变质。
②Fe2+在溶液中呈浅绿色,Fe3+在溶液中呈黄色。
③Fe3+的检验:向含Fe3+的溶液中滴加无色的KSCN(硫氨化钾)溶液,溶液会变为血红
色。
【猜想与假设】猜想I:该硫酸亚铁溶液没有变质。
猜想II.该硫酸亚铁溶液已经变质。
【设计实验并验证】
实验操作步骤实验现象实验结论
取少量样品于试管中,加入2〜
试管中溶液变成血红色核口酸王铁溶液已经变质
3滴KSCN(魏鼠也钟)溶液
【实验拓展1】下列各组物质在溶液中能大量共存,且形成无色溶液的是D。
A.CuSO4,NH4CkBa(OH)2
B.FeSO4>Na2sB4、KC1
C.FeCb、NaOH、HCI
D.NaCkMgSCh、KNO3
【实验拓展2]该实验小组继续查阅资料得知,单质铁能与硫酸铁溶液反应生成硫酸亚
铁。于是向上述久置的硫酸亚铁溶液中加入过量铁粉,写出其中的化学方程式Fe+
Fe2(SO6=3FeSO』。
类型三标签类成分的探究
10.(2019荆州)现有一瓶无色溶液,溶质可能是KOH、K2cCh中的一种或两种,某兴
趣小组对其成分进行如下实验探究:
【查阅资料】①KOH与NaOH的化学性质相似,K2cCh与Na2cCh的化学性质相似。
②K2cCh溶液呈碱性,BaCL溶液、CaCL溶液、KC1溶液呈中性。
【实验探究】设计并进行实验
实验操作步骤实验现象实验结论
(1)向盛有少量样品溶液的试
彳一色沉除士我肯定含有K2c03
管中加入过量CaCL溶液
(2)将操作⑴后的试管静置,
再向上层清液中加入几滴酚酚肽溶液变红色肯定含有KOH(武OH)
曲■溶液
【评价反思】①甲同学提出操作⑴加入的CaCL溶液必须过量,其目的是证明K2cCh
存在的同时还要K2cOK我c(y-)(合理?可)
②乙同学提出操作(1)在溶液较浓时,没有K2c03也能产生相同现象,其原因是一与避
化/般溶,小布彼(合理期可)建议改加过量的BaCb溶液,BaCL参加反应的化学方程
式为BaCb+K2cO]=BaCChl+2KC1。
【拓展应用】KOH和K2cCh的混合溶液敞口久置后可能变成K2co3溶液,反应的化
学方程式为CO2+2KOH=K2cO3+H2O。
11.(2019永州)在化学实验室,老师为同学们准备了三瓶没有贴标签的试剂(稀硫酸、氢
氧化钠溶液和氯化钢溶液),已知氯化领溶液呈中性。同学们自主进行探究实验。化学课代
表小李同学的实验过程如下:
(1)将三瓶试剂分别标记为A、B、C,然后两两混合,观察和记录实验现象。
实验
编号甲乙丙
实验
4A
操作
皆Bi|-c限
实验
现象产生白
色沉淀无明显现象无明显现象
根据上述实验现象可知:C中溶质的化学式是NaOH:A和B发生了化学反应,
不能肯定C与A,C与B发生了化学反应。
(2)验证C分别与A、B是否发生化学反应。
①实验操作和现象如图
M一
一
X二
」
日溶液变无色
D
一
昌-cLB一
一
一
」
溶液变红色一溶液不变色
日
②实验结论
试剂X的名称是—无色刈K_,C与」发生了化学反应。
(3)实验结束后,将实验甲、乙、丙三支试管中的物质倒入同一个烧杯中,充分搅拌、
静置、过滤,所得滤液中肯定含有的溶质是」M_(填化学式)。
12.(2018青岛)某兴趣小组在实验室里准备常见酸、碱、盐的性质实验时,发现实验台
上摆放的药品中,有一瓶未盖瓶塞且标签破损的溶液(如图),他们决定对这瓶溶液的成分进
行探究。
橡胶塞
小
【提出问题】这瓶溶液的溶质是什么0?
【获得信息】
(1)酸、碱、盐的性质实验中用到含钠元素的物质有氯化钠、氢氧化钠、碳酸钠、碳酸
氢钠。
(2)实验室里盛放碱性溶液的试剂瓶通常使用橡胶塞。
(3)碳酸氢钠溶液与氯化钙I溶液不反应;氯化钢溶液呈中性。
【提出猜想】
猜想一:氢氧化钠;
猜想二:碳酸钠;
猜想三:碳酸氢钠。
【实验探究】
(1)小军取样滴加稀盐酸有_皿__产生,得出结论:该溶液的溶质是碳酸钠或者是一
(2)小军另取样加入过量的氯化领溶液,观察到有—⑨邑范注_产生,进而得出结论:
该溶液的溶质是碳酸钠。
(3)小华认为小军的结论不完全正确,理由是一43L孑空气中的NaOH/英导正气中的
CCh博怠也金氏碟破例小组同学讨论后一致认为还需要进行如下实验:
(4)取小军第二次实验后的上层清液,滴入无色酚酸试液,溶液呈红色。
【实验结论】这瓶溶液的原溶质是一区里维
【探究启示】实验中取用液体药品时,应注意_标筌痛I多花,用后8时;1£檎。__。
类型四有关混合物成分的探究
13.(2019嘉兴、舟山)小明发现某食品包装袋中有一个小袋,上面标有“成分:生石灰、
铁粉;作用:防潮、防氧化”等字样。他想了解袋内粉末是否已失效,取少量粉末在水中
充分溶解,滴入无色酚配发现不变色。通过查阅资料获知,常温下铁在空气中不能反应生
成FejOq和FeO,于是对粉末成分做出如下猜想:
猜想一:可能是CaCCh和Fe;
猜想二:可能是CaCCh和FezCh;
猜想三:可能是CaCCh、Fe、Fe?。.,。
【实验设计】小明设计了如图所示的实验:
【实验与分析】
(1)向A装置中加入稀盐酸,B装置中出现浑浊现象,证明样品中含有CaCCh。
(2)若粉末中含有Fe,装置E中应观察到的现象是一无水就联稠变黄包一。
【评价与反思】上述实验中,如果将E装置去掉,是否还能验证粉末中含有Fe,请说
明理由.徐,,连破也播的您2像也索知崎一。
14.(2019云南省卷)某无色溶液X是碳酸钠、碳酸氢钠、氢氧化钠溶液中的一种或两种
溶液的混合溶液。某兴趣小组的同学为探究无色溶液X的成分,开展了如下的探究活动,
请你一同参与完成:
【查阅资料】获得如下信息:
1.氯化钙溶液呈中性,与碳酸氢钠溶液混合不发生反应。
2.NaHCCh溶液呈碱性,与澄清石灰水反应生成白色沉淀。
【猜想与假设】针对无色溶液X中的溶质成分:
猜想一:含有Na2c。3
猜想二:含有NaHCCh
猜想三:含有_NaOH(我H氟化釉)―
猜想四:是其中两种成分的混合溶液
【实验方案设计】
序号实验步骤预设实
验现象预设实
验结论
取样于烧杯中,滴入
①过量的氯化钙溶液,过产生白色沉淀猜想一
滤
--正端.
取①的滤液于试管中,
②滴入适量的氢氧化钙猜想二不正确
溶液
取①的滤液于试管中,
③溶液变红色猜想三正确
滴入的敏溶液
【综合结论】通过以上实验,得出无色溶液X是一罢K於青灵】也於(仅Na2c。3和
NaOH)的偎,令窿宠_。
【实验反思与拓展】类比资料信息,NaHCCh与NaOH反应生成质量比为53:9的两
种化合物,请写出反应的化学方程式NaHCCh+NaOH=Na2cO3+H2O。
15.某探究小组的同学通过查阅资料得知:在加热条件下,镁不仅能与水反应还能与氯
化核溶液反应。小组同学对此产生兴趣,他们将砂纸打磨过的镁条加入氯化核溶液中并加
热,迅速产生大量气体。为确定生成气体的成分,他们进行如下探究:
【查阅资料】(1)镁与氯化钱溶液反应生成两种气体,每种气体只含有氮、氢两种元素
中的一种或两种。
(2)镁与水在加热条件下反应生成氢氧化镁和氢气。
(3)氨气是一种极易溶于水的气体,能与酸反应。
【提出问题】该气体成分是什么?
【作出猜想】猜想一:出和N2
猜想二:N2和NH3
猜想三:用物NHKLJL大/氐人)_
【进行实验】
步骤一:小组同学闻气体气味,发现该气体有刺激性气味,则猜想_二_不成立。
步骤二:同学们把产生的气体通入盛有水的A装置中除去NHK中氐去,再将剩余
气体依次通过B、C、D装置中,一会儿后,加热试管中的氧化铜,观察到B中溶液不变色,
C中无明显现象,D中黑色粉末变成红色固体,试管口有小水珠。装置C的作用是_干燥
晁七(或除去中的水合)_,装置I)中发生反应的化学方程式为H2+CUO=组=CU
+H2O.
出结论】猜想_三_成立。
【拓展延伸】经过讨论,小华同学认为用点燃木条检验气体的方法代替装置D也能达
到相同的探究目的。你认为是否可行?_可行一(填“可行”或“不可行”)。
类型五有关物质性质的探究
16.(2019广州)已知金属钻(Co)的活动性与铁相似,请预测氯化钻(CoCL)的化学性质,
说明预测的依据,并设计实验验证。经查阅资料,钻的化合物相关性质如下:
物质
CoOCO(OH)2COC12
难溶于水的灰绿色固难溶于水的粉红色固易溶于水形成粉红色
在水中的溶解性
体体溶液
物质
CoSO4CO(NO3)2CoCO3
易溶于水形成粉红色易溶于水形成粉红色难溶于水的粉红色固
在水中的溶解性
溶液溶液体
限选试剂:CoCL溶液、(NH,2CO3溶液、Na2sCh溶液、AgNO.:溶液、NaOH溶液、
稀硫酸、镁条、铜片。
预测预测的依据验证预测的实验操作
与预期现象
取少量CoCL溶液于试管中,
①能够与含Ag+的可溶性盐CoCL溶液中含C「,AgCI_加八夕货AgNO3*》_,
反应难溶于水如果观察到守由色沉淀,广九
则预测成立
取少量CoCb溶液于试管中,
②能够与可游假或(填物质类CoCL4液中叁C()2+,加入寸步NaOH游海,如果
另»反应Co(OH)2《小小水观察到斗日红电电体金氏,则
预测成立
取少量CoCL溶液于试管中,
③能够与含Ctv-的按(我可
CoCL溶波中含Co?+,CoCOj加入夕量(NHQ2CQ3除波,如
♦犍碟致教)(填物质类别)反
唯■一水果观察到守口叁邑国体金氏,
应
则预测成立
17.(2019贵港)某化学兴趣小组在学习金属知识后,对金属钙及其化合物的化学性质非
常感兴趣,并进行了以下实验探究。
(1)对金属钙的化学性质进行探究
【提出问题】金属钙能否与水反应?
【实验探究】取一粒金属钙投入盛有50mL水的烧杯中,钙粒与水剧烈反应,四处游
动,产生气泡,溶液出现浑浊,用手触摸烧杯外壁,感觉发热。反应结束放置一段时间后,
溶液变澄清,往烧杯中滴入无色酚配试液,溶液变红色。
【实验结论】金属钙能与水反应。经进一步检验,产生的气体能燃烧。请写出钙与水
反应的化学方程式Ca+2H2。=H2t+Ca(OH>。
【交流与反思】反应结束放置一段时间后,溶液变澄清的原因是_浸,沸他,力段化
空港解太槽上,不像溶解的氐氟化/小哪窿解
(2)对久置于空气中的“生石灰”干燥剂的组成成分及含量进行探究
【查阅资料】Ca(OH”加热到一定温度时会发生分解反应,生成两种氧化物。
【实验探究】该小组称取10.0g干燥剂样品于控温电加热器中,按下图所示装置进行
实验(装置气密性良好,装置A、B、C中药品足量,实验操作正确)。
【实验数据记录】充分反应后,产物被完全吸收,A装置增重0.9g,B装置增重2.2g。
【分析与结论】该包干燥剂的成分有CaO、Ca(OHRCaCCh-(填化学式),其中
Ca(OH)2的质量为32_g。
【反思与拓展】
①停止加热后,需要通入N2一段时间的目的是—使女正士风的水、二/也碟全部较浓
砒减,、气兼化噌除恢,唳收__。
②若没有C装置,会导致含量测定结果偏小的成分是_星色鱼
类型六有关条件、影响因素的探究
18.(2018福建节选)某研究小组对过氧化氢溶液制取氧气进行如下探究。
实验二探究H2O2质量分数、溶液pH、温度对反应速率的影响
(2)设计如下表实验方案:
实验序号出。2质
量分数/%pH温度/℃每分钟气
泡数
130520
230620
3301120
4151130
5aHb
①实验[〜3的实验目的是—探究修波pH对反怠速■阜的图响(箕其他合理答案)_。
②.二」5(或30)_;%=_20(或30,■&上一1财
实验三探究制取氧气的适宜催化剂
(3)实验方案如下
I.用Mnth、CuO、Fe2O3,CnCh四种催化剂分别与海藻
温馨提示
- 1. 本站所有资源如无特殊说明,都需要本地电脑安装OFFICE2007和PDF阅读器。图纸软件为CAD,CAXA,PROE,UG,SolidWorks等.压缩文件请下载最新的WinRAR软件解压。
- 2. 本站的文档不包含任何第三方提供的附件图纸等,如果需要附件,请联系上传者。文件的所有权益归上传用户所有。
- 3. 本站RAR压缩包中若带图纸,网页内容里面会有图纸预览,若没有图纸预览就没有图纸。
- 4. 未经权益所有人同意不得将文件中的内容挪作商业或盈利用途。
- 5. 人人文库网仅提供信息存储空间,仅对用户上传内容的表现方式做保护处理,对用户上传分享的文档内容本身不做任何修改或编辑,并不能对任何下载内容负责。
- 6. 下载文件中如有侵权或不适当内容,请与我们联系,我们立即纠正。
- 7. 本站不保证下载资源的准确性、安全性和完整性, 同时也不承担用户因使用这些下载资源对自己和他人造成任何形式的伤害或损失。
最新文档
- 2025年透视企业项目合同管理现状与优化策略
- 2025车库转让合同范本
- 江西省赣州市大余县部分学校联考2024-2025学年高二下学期3月月考英语试题(含答案)
- 2025个人借款合同模板规范
- 2025年:探讨合同法在企业人力资源管理中的关键作用
- 2025资产买卖合同模板
- 2025YY年地区寄宿制学校学生公寓床采购合同
- 汽车安全性检查流程及重点试题及答案
- 浙江理工大学《交通数据处理与分析》2023-2024学年第二学期期末试卷
- 武汉城市学院《设计与开发课程设计》2023-2024学年第二学期期末试卷
- 期中检测卷2023-2024学年人教版数学八年级下册
- 包头铸胶滚筒工艺
- 2024年山东春季高考数学试题word版(含答案解析)
- (完整版)东南大学工程项目管理陆惠民第二章工程项目策划和决策(课后习题答案)
- 盐的销售与市场拓展
- ST语言编程手册
- 医院HIS信息管理系统故障应急预案
- 司法案例研究方法与技巧
- 足球运球课件
- (7)-2.3 理想信念是精神之钙
- MSA-测量系统分析模板

评论
0/150
提交评论