



版权说明:本文档由用户提供并上传,收益归属内容提供方,若内容存在侵权,请进行举报或认领
文档简介
第三章水溶液中的离子反应与平衡
4.1难溶电解质的沉淀溶解平衡【新课引入】电子感光材料珠宝饰品医用金属银有关的用途【新课引入】1mL
0.012mol/L
NaCl溶液1mL
0.010mol/L
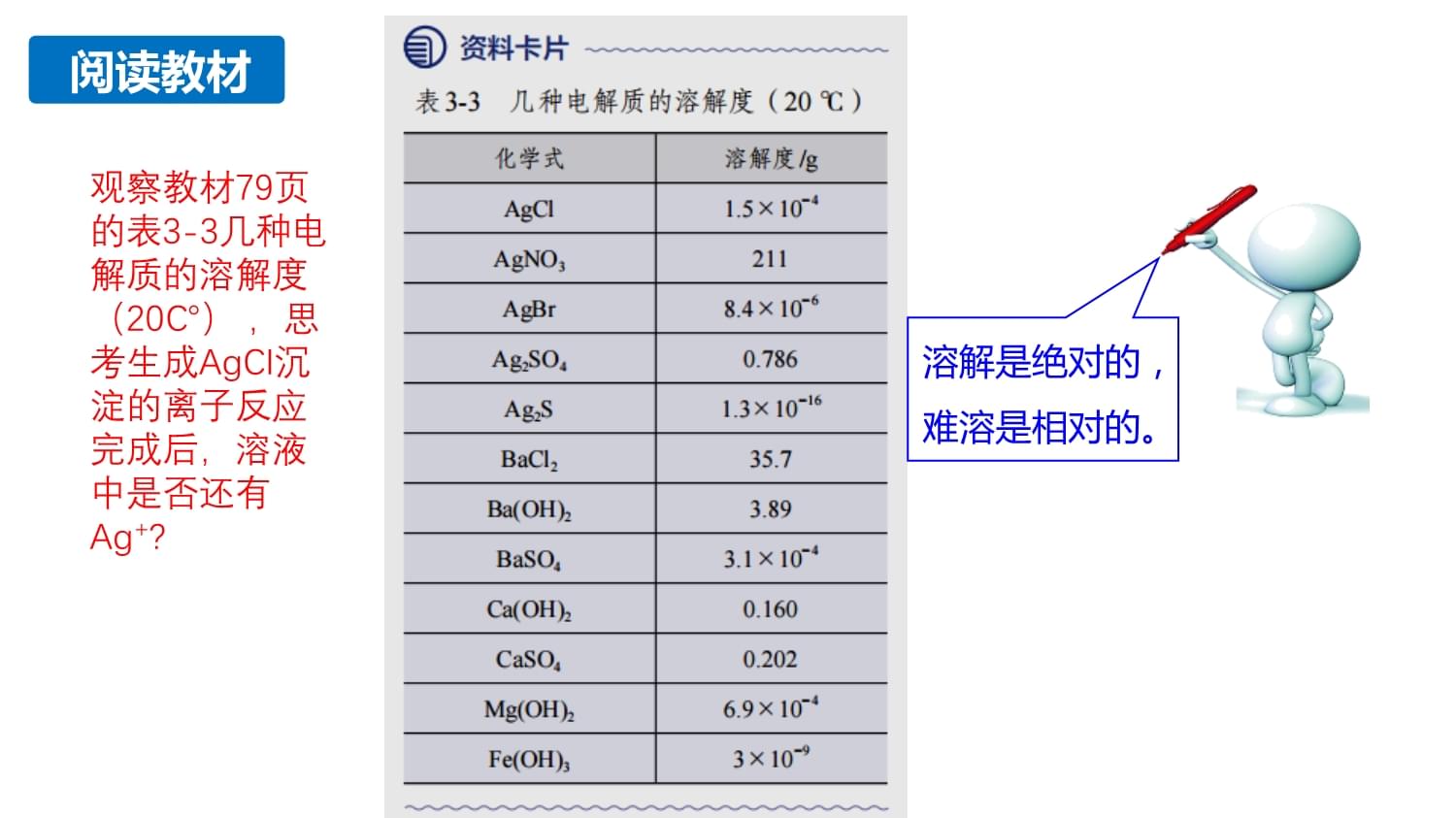
AgNO3溶液Ag+已经除尽了吗?【思考与讨论1】Ag++Cl-=AgCl↓现用1mL0.010mol/LAgNO3溶液模拟工业废水,某同学提出可以加入1mL0.012mol/L的NaCl溶液,充分反应,除去其中的Ag+。溶液中还有Ag+吗?阅读教材溶解是绝对的,难溶是相对的。观察教材79页的表3-3几种电解质的溶解度(20℃),思考生成AgCI沉淀的离子反应完成后,溶液中是否还有Ag+?【分析】10g1g0.01g易溶可溶微溶难溶AgNO3BaCl2Ba(OH)2Ag2SO4Ca(OH)2CaSO4AgClAgBrAg2SBaSO4Mg(OH)2Fe(OH)3习惯上将溶解度小于0.01g的电解质称为难溶电解质。尽管难溶电解质的溶解度很小,但在水中并不是绝对不溶。生成AgCI沉淀后,有三种粒子在反应体系中共存:AgCl(s)、Ag+(aq)、Cl-(aq)Ag+(aq)+Cl-(aq)
AgCl(s)
【分析】一、沉淀溶解平衡的概念以AgCl为例,分析沉淀溶解平衡的建立两个过程:一方面,在水分子作用下,少量Ag+和Cl-脱离AgCl的表面进入水中,这一过程就是溶解另一方面,溶液中的Ag+和Cl-受AgCl表面阴、阳离子的吸引,回到AgCl的表面析出,这一过程就是沉淀υ(沉淀)=
υ(溶解)沉淀不再增多,达到沉淀溶解平衡一定时间后:AgCl(s)Ag+(aq)+Cl-(aq)
溶解AgCl(s)Ag+(aq)+Cl-(aq)
溶解沉淀(1)概念:在一定温度下,当难溶电解质溶解和沉淀的速率相等时,形成
电解质的饱和溶液,达到平衡状态,溶液中各离子的浓度保持
不变,这种平衡称为沉淀溶解平衡。(2)特征:逆、等、动、定、变(3)沉淀溶解平衡方程式:AgCl(s)Ag+(aq)+Cl-(aq)
溶解沉淀书写时注意表明各物质的状态和可逆符号特别提醒:一、沉淀溶解平衡的概念Fe(OH)3(s)Fe3+(aq)+3OH-(aq)
(沉淀溶解平衡)Fe(OH)3Fe3++3OH-
(电离平衡)沉淀溶解平衡和弱电解质的电离平衡的区别一、沉淀溶解平衡的概念【练习】请写出BaSO4、Ag2S、Fe(OH)3的沉淀溶解平衡方程式。
BaSO4(s)⇌Ba2+(aq)+SO42-(aq)
Fe(OH)3(s)⇌Fe3+(aq)+3OH-(aq)
Ag2S(s)⇌2Ag+(aq)+S2-(aq)
一、沉淀溶解平衡的概念【思考与讨论2】AgNO3溶液与NaCl溶液沉淀反应完成后,要使溶液中的Ag+浓度尽量小?你能想出哪些办法?二、沉淀溶解平衡的影响因素【思考】哪些因素会影响沉淀溶解平衡?(1)内因:难溶电解质本身的结构和性质。决定因素(2)外因:——符合“勒夏特列原理”①温度:升高温度,多数平衡向沉淀溶解方向移动;Ca(OH)2除外②浓度:向平衡体系中加水稀释,平衡向沉淀溶解方向移动;
增大离子浓度,平衡向生成沉淀方向移动【讨论】对于平衡AgCl(s)⇌Ag+(aq)+Cl-(aq),改变下列条件,对其有何影响?改变条件平衡移动方向c(Ag+)c(Cl-)升温
加水(有固体剩余)
加AgCl(s)
加NaCl(s)
加AgNO3(s)
正向增大增大正向不变不变不移动不变不变逆向减小增大逆向增大减小二、沉淀溶解平衡的影响因素上述1mL0.012mol/L的NaCI溶液与1mL0.010mol/LAgNO3溶液充分反应后,溶液中剩余Ag+的浓度是多少?【思考与讨论3】涉及化学平衡的计算常需要什么数据?三、溶度积常数Ksp=c(Ag+)·c(Cl-)
难溶电解质的沉淀溶解平衡常数,称为溶度积常数,简称溶度积,符号为Ksp。思考:AgCl溶解平衡的平衡常数如何表示?AgCl(s)Ag+(aq)+Cl—(aq)固体纯物质不列入平衡常数【练习】写出下列难溶物的沉淀溶解平衡方程式和溶度积表达式。BaSO4Fe(OH)3Ag2SKsp=c(Ba2+)·c(SO42-)BaSO4(s)⇌Ba2+(aq)+SO42-(aq)
Fe(OH)3(s)⇌Fe3+(aq)+3OH-(aq)
Ag2S(s)⇌2Ag+(aq)+S2-(aq)
Ksp=c(Fe3+)·c3(OH-)Ksp=c2(Ag+)·c(S2-)三、溶度积常数【思考与讨论3】上述1mL0.012mol/L的NaCI溶液与1mL0.010mol/LAgNO3溶液充分反应后,溶液中剩余Ag+的浓度是多少?一般情况,当溶液中剩余离子的浓度小于1×10-5mol/L时,化学上通常认为生成沉淀的反应就进行完全了。国家各行业污染物排放标准中,规定了不同的Ag+排放标准,例如有些行业规定不能超过约1×10-7mol/L。教材126页Ksp的意义:反映了难溶电解质在水中的溶解能力化学式AgClAgBrAgIAg2SKsp1.8×10-105.4×10-138.1×10-176.3×10-50溶解度(S)1.5×10-48.4×10-62.1×10-71.3×10-16(1)对于同类型(阴、阳离子个数比相同)的难溶电解质来说,
Ksp越小,其溶解度越小。溶度积:Ksp(AgCl)>Ksp(AgBr)>Ksp(AgI)溶解度:S(AgCl)>S(AgBr)>S(AgI)三、溶度积常数(2)判断沉淀是否生成达到平衡状态时:溶度积
Ksp=c2(Ag+)·c(S2-)任意某一时刻:离子积Q
=c2(Ag+)·c(S2-)若Q
>
Ksp,溶液过饱和,有沉淀析出;若Q=Ksp,溶液饱和,沉淀与溶解处于平衡状态;若Q<Ksp,溶液不饱和,无沉淀析出;【例】将4×10-3mol·L-1的AgNO3溶液与4×10-3mol·L-1的Na2S溶液等体积混合能否有沉淀析出?[Ksp(
温馨提示
- 1. 本站所有资源如无特殊说明,都需要本地电脑安装OFFICE2007和PDF阅读器。图纸软件为CAD,CAXA,PROE,UG,SolidWorks等.压缩文件请下载最新的WinRAR软件解压。
- 2. 本站的文档不包含任何第三方提供的附件图纸等,如果需要附件,请联系上传者。文件的所有权益归上传用户所有。
- 3. 本站RAR压缩包中若带图纸,网页内容里面会有图纸预览,若没有图纸预览就没有图纸。
- 4. 未经权益所有人同意不得将文件中的内容挪作商业或盈利用途。
- 5. 人人文库网仅提供信息存储空间,仅对用户上传内容的表现方式做保护处理,对用户上传分享的文档内容本身不做任何修改或编辑,并不能对任何下载内容负责。
- 6. 下载文件中如有侵权或不适当内容,请与我们联系,我们立即纠正。
- 7. 本站不保证下载资源的准确性、安全性和完整性, 同时也不承担用户因使用这些下载资源对自己和他人造成任何形式的伤害或损失。
最新文档
- 2025-2030中国煤制乙烯行业发展趋势及发展前景研究报告
- 2025-2030中国热成像红外摄像机行业市场现状供需分析及投资评估规划分析研究报告
- 2025-2030中国火炮系统行业市场发展趋势与前景展望战略研究报告
- 2025-2030中国激光焊接服务行业市场发展趋势与前景展望战略研究报告
- 2025-2030中国激光全息防伪行业市场现状分析及竞争格局与投资发展研究报告
- 2025-2030中国滤网行业供需趋势及未来投资可行性研究报告
- 2025-2030中国滑板卡车行业市场现状供需分析及投资评估规划分析研究报告
- 2025-2030中国游泳池盖行业市场现状供需分析及投资评估规划分析研究报告
- 2025-2030中国港口建设行业发展分析及发展趋势预测与投资风险研究报告
- 2025-2030中国渗滤液处理行业发展潜力评估及市场前景预判研究报告
- 拘留所教育课件02
- 中国音乐史课件
- 11471劳动争议处理(第4章)
- 小学语文人教三年级下册 赵州桥-
- 基因治疗课件最新版
- 幼儿园社会领域自我意识活动教案(3篇)
- 识别和获取法律法规管理制度
- 2022“博学杯”全国幼儿识字与阅读大赛选拔试卷
- 2022年老年人健康管理工作总结
- 《碳纤维片材加固混凝土结构技术规程》(2022年版)
- 青岛城园林绿化技术规范

评论
0/150
提交评论