



付费下载
下载本文档
版权说明:本文档由用户提供并上传,收益归属内容提供方,若内容存在侵权,请进行举报或认领
文档简介
1、2.3 氧化还原反应(第一课时)本节教材是化学1(人教版)第二章化学物质及其变化的第三节,在这一章的第一节物质的分类中,学生已学习了简单的分类法及其应用。在第一节的“思考与交流”教学活动,学生曾对化学物质和化学反应进行了简单的分类。学生在初三已学习过化学反应从得失氧的角度分类可分为氧化反应和还原反应,按反应物和生成物的类别以及反应前后物质的种类的多少把化学反应可分为四种基本反应类型,即化合反应、分解反应、置换反应、复分解反应。学生在初三已经学习了化合价,初步认识了化合价的变化跟电子的转移有一定的关系。教学目标知识与技能:1通过方程式的对比,使学生认识到化学反应可以从有无电子转移进行分类,建立氧
2、化还原反应的概念。2学会用化合价升降及电子转移的观点来理解氧化还原反应。3通过学生尝试画出四种基本反应类型与氧化还原的交叉分类示意图,进一步理解四种基本反应与氧化还原的关系,认识到用有无电子转移对反应分类更为本质。4认识到氧化还原反应与我们生活密切相关。过程与方法:1通过设计问题情境,由表及里培养思维的深刻性,由此及彼培养思维的逻辑性。2运用对比、类推的方法,形成科学的探究精神,学会分析反应过程中电子转移的方向和数目。3通过提出问题、讨论交流、分组合作,揭示氧化还原反应的本质和特征,培养学生从微观角度准确理解概念的能力。情感态度与价值观:1通过交流、讨论,形成合作学习的意识及自我表达的能力2在
3、理解电子得失、氧化和还原的相互依存和相互对立的关系上对学生进行对立统一等辩证唯物主义观点的教育。3 通过对氧化还原反应概念认识的过程,培养学生用发展的观点、科学的态度,体会科学探究的基本方法,提高科学探究能力,使学生体验到知识的发展是有局限性的,是要不断推陈出新的。4 了解氧化还原反应在工农业生产、日常生活中的应用,认识并理解化学这门学科对提高人类生活质量、促进社会发展的重要作用。重点、难点教学重点:引导学生用相关知识从化合价升降和电子转移观点认识氧化、还原、氧化还原反应等概念,从而归纳出氧化还原反应的特征与本质。教学难点:从电子转移的观点来分析理解氧化还原反应的本质。因为观察事物的外部特征比
4、较容易,但透过现象揭示本质时学生往往觉得较难。教学过程:教师活动学生活动设计意图谜语引入:前世生在海中,炼得一 身晶莹,三餐离它不行,遇水无影 无踪。展示:氯化钠样品提问:实验室中可通过哪些/、同的 反应原理(交型)得到氯化钠呢?激发兴趣相互讨论学生能举出:通过复分解、 化合等反应实现学生通过身边的 氯化钠入手,复 习初中学过的几 类反应投影:(1)盐酸与氢氧化钠的反应 (2)金属钠与氯气的反应 演示实验:钠在氯气中燃烧初步观察两个方程式观察反应现象,迅速得到氯 化钠增加学生对钠和 氯气反应的感性 认识,为钠原子 和氯原子得失电 子的分析作铺 垫。布置任务:宏观上看,上述两种方 法都能得到氯化
5、钠,但从微观角度 看,两个反应还是有很大差别的, 你能找出这两个反应的本质区别 吗?教师及时引导学生从反应前后无 素是否变化,原子重新组合时是否 变化的微观角度去对比两个反应进一步分析这两个方程式 学生分组讨论联系前面学习的离子反应, 能够得出反应前后都是离 子,微粒没有变化;联系初 二离子化合物的形成,可分 析出反应前微粒为原子,而 反应后微粒为离子0设置先行组织 者,从前圜的知 识认识化学反应 前后,微粒可能 发生改变培养学生用不同 视角观察反应, 从宏观上、微观 上认识两个反应 的/、同点投影:初中金属钠与氯气反应卡通 图提问:钠原子为什么要把电子给氯 原子呢?观看从原子核外电子排布和8
6、电子稳定结构上分析使学生了解为什 么要转移电子分析:金属钠与氯气反应生成氯化钠的微观过程动画演示:氯化钠的形成使学生明白,完成这个反应的同时 化合价也发生了变化初步认识到某些 化学反应中启电 子的转移。教师演示双线桥表示电子转移的 方法观察、了解表示方法布置任务:化合价的升降与电子的 转移具体关系如何呢? 投影:化合价数轴-4 -3 -2 -1 0 +1 +2 +3 +4 +5 +6学生讨论,完成学案思考讨论得出定性关系:化合价升 高,元素失去电子从定性定量角度 进一步将化合价 的变化与电子的 得失联系在T+7演示实验:锌粒和硫酸铜反应时电 流检验,观察现象讲解:铜的产生,说明后新物质生 成,
7、这说明发生了一个化学反应, 在此反应过程中我们观察到了有 电流通过,充分说明反应过程中肩 电子的转移。观察,好奇验证自己的判断,产生成就感同时感觉到理论可以由实验来验证通过实验验证, 使学生体会到电 子转移的真实存 在激发学生进一步 学习的兴趣结论:从宏观上看,化学反应的本 质是有新物质生成;从微观上看, 化学反应前后兀素种类不变,但反 应前的微粒在重新结合成新物质 时,会出现网种情况:一种是无电 子的转移,一种是有电子的转移。 由此,我们依据是否启电子转移的 标准把化学反应分为两大类倾听、记忆学习另一种给反应分类的 方法r有电子转移化学反应,1无电子转移初步认识到化学 反应中可能有电 子的转
8、移使学生从微观角 度去认识反应, 去给反应分类讲解:电子的转移是个微观过程, 我们/、可能把所有的反应都用这 套装置来检验是否后电子的转移, 这就需要我们从反应前后物质的 化合价是否启改变角度去判断。学会用理论判断找到理论判断依 据布置任务:判断卜列反应过程中启无化合价的改变?CaO + CO = CaCQ2HgO = 2Hg+ QTH2 + CuO = Cu + H 2OCuCb+2NaOH=Cu(OH) +2NaCl运用初三所学常见化合价, 能止确进行判断认识到化学反应 中启的有化合价 改变,有的没有 为氧化还原概念 的引出作铺垫提问:我们看到,有的化学反应反 应前后化合价无变化,有的反应
9、化 合价后发化,你能给化行份后发化 的反应起个名字吗?思考,给反应起名字 学生进一步理解这类反应 的特征和本质引起学生学习新 概念的兴趣引出:其实科学家们早已起好了, 我们把有化合价改变的化学反应 叫做氧化还原反应,把无化合价改 变的化学反应叫做非氧化还原反 应。倾听、记忆可能有的学生会与初中的 氧化、还原反应挂钩,产生 认识的矛盾给出氧化还原反 应的概念使学生明确化合 价的改变是判断 氧化还原反应的 标准讲解:氧化还原反应定义、特征、本质及氧化还原反应的组成(氧化反应 和还原反应)给出氧化反应和还原反应的定义, 讲解二者对立统一关系学生接受新知识了解氧化还原中的对立统一关系建立较完整的氧 化
10、还原理论揭示氧化还原反 应的本质和特 征,培养学生从 微观角度准确理 解概念的能力布置任务:请同学们指出下取化学 反应的类型?4Na + O2 = 2Na2OCaO + CO = CaCO3Cu(OH» = CuO + H2O 2KC1Q = 2KC1+ 3O 2 T H2 + CuO = Cu + H 2O Zn + CuSO4 = ZnSO4 + Cu CuCb+2NaOH=Cu(OH) +2NaCl FeQ + 3CO = 2Fe + 3CO 2讨论分析,可分为化合、分 解、复分解、置换反应;可 能有同学分析得出有的属 于氧化反应、有的属于还原 反应;也可能有的同学直接 分为两
11、类,氧化还原和非氧 化还原反应从/、同视角给反 应分类试着从氧化还原 视角看反应使学生对化学反 应的分类肩了新 的认识,即化学 反应可分为氧化 还原反应和非氧 化还原反应。布置任务:四类基本反应和氧化还 原反应的关系从集合角度分析氧还反应 和四类基本反应的关系 置换反应全部属于氧化还 原反应有单质参加的化合反应和 有单质生成的分解反应全 部属于氧化还原反应 复分解反应全部属于非氧 化还原反应让学生尝试画出 四种基本反应类 型与氧化还原的 交叉分类示意 图,进一步理解 四种基本反应与 氧化还原的关系 从氧化还原角度 认识反应更为本 质同学们在初中接触过氧化还原反 应吗?你能举几个例子吗?从化合价
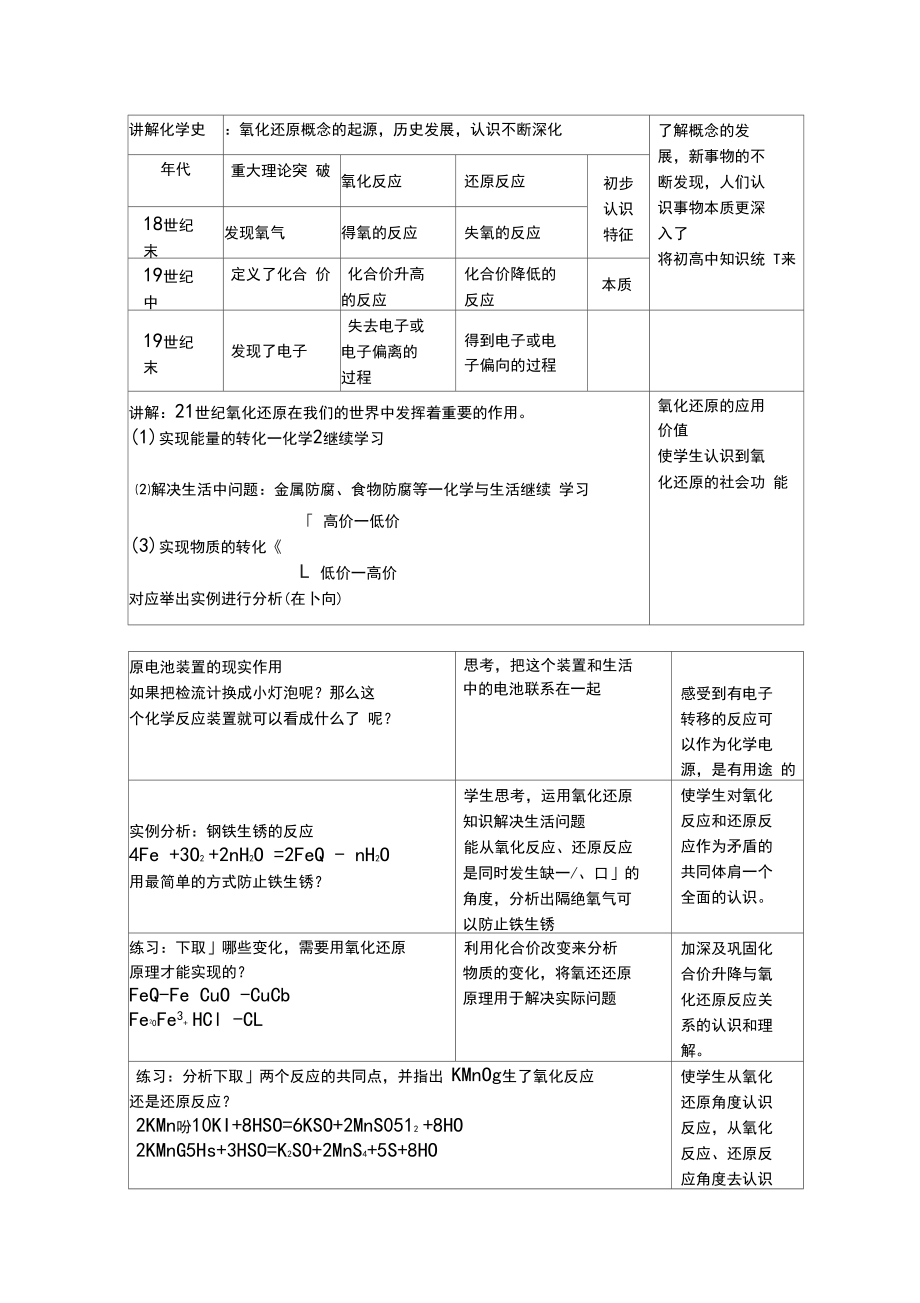
12、升降角度看,他们是氧化 还原反应吗?以 H2 + CuO = Cu + H 2O 为例,进 行分析,同一个反应随着历史的发 展,认识/、断深化将初中学的氧化反应、还原 反应与今天讲的氧化还原 反应联系起来举出几个氧化反应和还原反应的例子判断出这些例子都是氧化 还原反应初机口高一的知 识不矛盾,局中 电子转移认识氧 化还原的层次更 高,原有理论并 不是完全抛弃, 是认识发展的体 现讲解化学史:氧化还原概念的起源,历史发展,认识不断深化了解概念的发 展,新事物的不 断发现,人们认 识事物本质更深 入了将初高中知识统 T来年代重大理论突 破氧化反应还原反应初步 认识 特征18世纪末发现氧气得氧的反应
13、失氧的反应19世纪中定义了化合 价化合价升高 的反应化合价降低的 反应本质19世纪末发现了电子失去电子或 电子偏离的 过程得到电子或电 子偏向的过程讲解:21世纪氧化还原在我们的世界中发挥着重要的作用。(1)实现能量的转化一化学2继续学习解决生活中问题:金属防腐、食物防腐等一化学与生活继续 学习 高价一低价(3)实现物质的转化L 低价一高价对应举出实例进行分析(在卜向)氧化还原的应用 价值使学生认识到氧 化还原的社会功 能原电池装置的现实作用如果把检流计换成小灯泡呢?那么这 个化学反应装置就可以看成什么了 呢?思考,把这个装置和生活 中的电池联系在一起感受到有电子 转移的反应可 以作为化学电
14、源,是有用途 的实例分析:钢铁生锈的反应4Fe +3O2 +2nH2O =2FeQ - nH2O 用最简单的方式防止铁生锈?学生思考,运用氧化还原 知识解决生活问题能从氧化反应、还原反应 是同时发生缺一/、口的 角度,分析出隔绝氧气可 以防止铁生锈使学生对氧化 反应和还原反 应作为矛盾的 共同体肩一个 全面的认识。练习:下取哪些变化,需要用氧化还原 原理才能实现的?FeQ-Fe CuO -CuCbFe20Fe3+ HCl -CL利用化合价改变来分析 物质的变化,将氧还还原 原理用于解决实际问题加深及巩固化 合价升降与氧 化还原反应关 系的认识和理 解。练习:分析下取两个反应的共同点,并指出 KMnOg生了氧
温馨提示
- 1. 本站所有资源如无特殊说明,都需要本地电脑安装OFFICE2007和PDF阅读器。图纸软件为CAD,CAXA,PROE,UG,SolidWorks等.压缩文件请下载最新的WinRAR软件解压。
- 2. 本站的文档不包含任何第三方提供的附件图纸等,如果需要附件,请联系上传者。文件的所有权益归上传用户所有。
- 3. 本站RAR压缩包中若带图纸,网页内容里面会有图纸预览,若没有图纸预览就没有图纸。
- 4. 未经权益所有人同意不得将文件中的内容挪作商业或盈利用途。
- 5. 人人文库网仅提供信息存储空间,仅对用户上传内容的表现方式做保护处理,对用户上传分享的文档内容本身不做任何修改或编辑,并不能对任何下载内容负责。
- 6. 下载文件中如有侵权或不适当内容,请与我们联系,我们立即纠正。
- 7. 本站不保证下载资源的准确性、安全性和完整性, 同时也不承担用户因使用这些下载资源对自己和他人造成任何形式的伤害或损失。
最新文档
- 长春电子科技学院《安全管理工程》2025-2026学年期末试卷
- 武夷学院《病理学》2025-2026学年期末试卷
- 闽南师范大学《新闻编辑学》2025-2026学年期末试卷
- 闽南科技学院《口腔内科学》2025-2026学年期末试卷
- 煤制烯烃生产工持续改进评优考核试卷含答案
- 整经工岗前实操评估考核试卷含答案
- 固体树脂版印刷员复测模拟考核试卷含答案
- 电机车修配工安全防护测试考核试卷含答案
- 中高频炉工岗前班组考核考核试卷含答案
- 压榨机工创新应用评优考核试卷含答案
- (2025年)电工三级安全教育试题及答案
- 2026年设备状态监测的标准与规范
- 2026广东东莞市常平镇编外聘用人员招聘5人备考题库附答案详解(完整版)
- 广东省广州市黄埔区第八十六中学2024-2025学年八年级下学期4月期中物理试题(含答案)
- 2026年广东食品药品职业学院单招职业技能测试题库附参考答案详解(a卷)
- 深海采矿生态修复技术的可行性研究
- 企业价值成长中耐心资本的驱动作用研究
- 兰铁局防护员考核制度
- 2026届安徽省江南十校高三上学期10月联考数学试题(解析版)
- 廊道、洞室及有限空间作业安全注意事项
- 2026届新高考语文三轮冲刺复习:散文阅读

评论
0/150
提交评论