



版权说明:本文档由用户提供并上传,收益归属内容提供方,若内容存在侵权,请进行举报或认领
文档简介
1、 第三章第三章 水溶液中的离子平衡水溶液中的离子平衡第二节第二节 水的电离和溶液的酸碱性水的电离和溶液的酸碱性 ( (第第1 1课时课时) ) 知知 识识 回回 顾顾分析分析HCl在水中的电离过程,写出电离方程式。在水中的电离过程,写出电离方程式。HCl = H+ + Cl-Cl-Cl-Cl-Cl-Cl-HCl是是 电解质电解质 在水溶液中在水溶液中 电离电离强强完全完全 知知 识识 回回 顾顾分析分析CH3COOH在水中的电离过程,写出电离方程式。在水中的电离过程,写出电离方程式。CH3COOH是是 电解质电解质 在水溶液中在水溶液中 电离电离弱弱部分部分CH3COOH H+CH3COO-
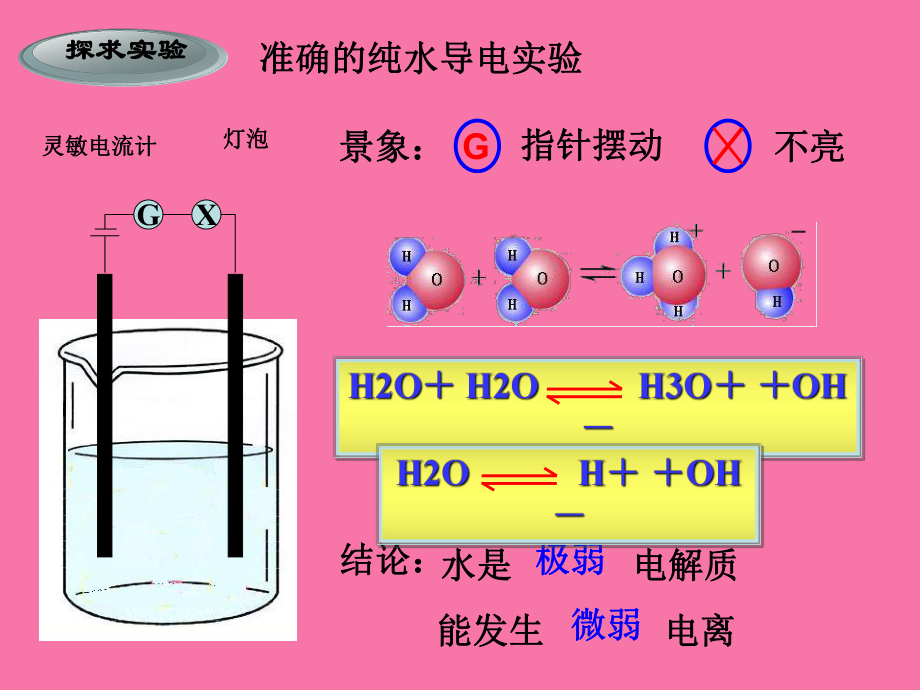
2、CH3COOH H+CH3COO- 以下那幅电离表示图可以表示水的电离过程。以下那幅电离表示图可以表示水的电离过程。以分子方式存在以分子方式存在部分电离部分电离完全电离完全电离如何用实验探求水的电离过程?如何用实验探求水的电离过程?OH-OH-OH-OH-OH-OH-探求实验探求实验准确的纯水导电实验准确的纯水导电实验G指针摆动指针摆动不亮不亮结论:结论:水是水是 电解质电解质 极弱极弱能发生能发生 电离电离 微弱微弱灵敏电流计灵敏电流计灯泡灯泡景象:景象:GX一、水的电离一、水的电离K电离电离 =c(H+) c(OH-) c(H2O)c(H+) c(OH-) c(H2O) K电离电离 =室温
3、下室温下55.6mol H2O中中有有110-7mol H2O电离,电离,因此因此c(H2O)可视为常数。可视为常数。 Kw 水的离子积水的离子积Kw =室温下室温下110-14注:注:c(H2O)=1 L1000 g18 gmol-1分析表格中的数据,有何规律,并解释之。分析表格中的数据,有何规律,并解释之。t/0102025405090100Kw/10-140.1340.2920.6811.012.925.4738.055.0结论结论温度越高,温度越高,Kw越大。越大。 Kw在一定温度下是个常数。在一定温度下是个常数。升高温度,促进水的电离。升高温度,促进水的电离。水的电离是一个吸热过程。
4、水的电离是一个吸热过程。影响水的电离平衡的要素影响水的电离平衡的要素(阅读阅读P46)思索与交流思索与交流:根据室温时水的电离平衡根据室温时水的电离平衡,分分析影响水的电离平衡的要素析影响水的电离平衡的要素比较以下情况下比较以下情况下, c(H+)和和c(OH-)的值或变化趋势的值或变化趋势(添加或减少添加或减少)纯水纯水加少量盐酸加少量盐酸加少量氢氧化钠加少量氢氧化钠c(H+)c(OH-)c(H+) 和和 c(OH-)大小比较大小比较10-710-7c(H+) =c(OH-)c(H+) c(OH-)c(H+) C(OH-) ;C(H+)C(H+)C(OH-) ;C(H+)越大酸性越强越大酸性
5、越强碱性溶液:碱性溶液:C(H+)C(OH-) ;C(OH-)C(H+)C(OH-) C(H+)1C(H+)C(OH-) C(H+)110-7mol/L10-7mol/LC(H+)C(OH-) C(H+)1C(H+)C(OH-) C(H+)110-7mol/L10-7mol/LpH的测定:的测定:pH计酸度计计酸度计2pH试纸试纸留意:不能用水润湿留意:不能用水润湿要放在玻璃片或外表皿上要放在玻璃片或外表皿上不是将试纸伸到溶液中不是将试纸伸到溶液中广泛广泛pH试纸只能读出整数试纸只能读出整数粗略测定:粗略测定: 1酸碱指示剂酸碱指示剂甲基橙甲基橙石蕊石蕊酚酞酚酞酸色酸色 碱色碱色 红红 黄黄
6、红红 蓝蓝 无无 红红准确测定:准确测定:变色范围变色范围(pH) 3.14.4 5.08.0 8.210.0了解了解用法:用玻璃棒蘸用法:用玻璃棒蘸溶液,点在溶液,点在pH试纸试纸中央,半分钟后与中央,半分钟后与比色卡比色比色卡比色 2007年高考广东卷以下可用于测定溶液年高考广东卷以下可用于测定溶液pH且准且准确度最高的是确度最高的是( ) (A)酸碱指示剂酸碱指示剂 (B)pH计计 (C)精细精细pH试纸试纸 (D)广泛广泛pH试纸试纸高考链接高考链接B3.3.溶液中溶液中C(H+)C(H+)、C(OH-)C(OH-)的计算的计算例例1 1:计算以下溶液中:计算以下溶液中C(H+)C(H
7、+)与与C(OH-)C(OH-)(1)1(1)110-3mol/LHCl10-3mol/LHCl溶液溶液(2)0.05mol/LBa(OH)2(2)0.05mol/LBa(OH)2溶液溶液例例2 2:10mL10-4mol/LHCl,10mL10-4mol/LHCl,加水至加水至100mL,100mL,此时溶液中此时溶液中C(H+)= mol/LC(H+)= mol/L;假设加水至;假设加水至105mL,105mL,此时溶液中此时溶液中C(H+)C(H+)又是又是 阐明阐明 2 2常温下,浓度为常温下,浓度为1 110-5mol/l10-5mol/l的的NaOHNaOH溶液溶液中,由水电离产生的中,由水电离产生的C(OH-)C(OH-)是多少?是多少? 练习练习1.1.1 1常温下,浓常温下,浓度为度为1 110-5mol/l10-5mol/l的盐酸溶的盐酸溶液中,由水电离产生的液中,由水电离产生的C CH+H+是多少?是多少?(1)(1)解:解:C C水水H+H+=C=C水水OH-OH-(2)(2)解:解:C C水水OH-OH-= C= C水水H+H+ 思索题:在常温下,由水电离产生的思索题:在常温下,由水电离产生的C CH+H+=1=110-9 mol/L10-9 mol/L的溶液,那么该溶液的酸碱性如何?的溶液,那么该溶
温馨提示
- 1. 本站所有资源如无特殊说明,都需要本地电脑安装OFFICE2007和PDF阅读器。图纸软件为CAD,CAXA,PROE,UG,SolidWorks等.压缩文件请下载最新的WinRAR软件解压。
- 2. 本站的文档不包含任何第三方提供的附件图纸等,如果需要附件,请联系上传者。文件的所有权益归上传用户所有。
- 3. 本站RAR压缩包中若带图纸,网页内容里面会有图纸预览,若没有图纸预览就没有图纸。
- 4. 未经权益所有人同意不得将文件中的内容挪作商业或盈利用途。
- 5. 人人文库网仅提供信息存储空间,仅对用户上传内容的表现方式做保护处理,对用户上传分享的文档内容本身不做任何修改或编辑,并不能对任何下载内容负责。
- 6. 下载文件中如有侵权或不适当内容,请与我们联系,我们立即纠正。
- 7. 本站不保证下载资源的准确性、安全性和完整性, 同时也不承担用户因使用这些下载资源对自己和他人造成任何形式的伤害或损失。
最新文档
- 城市公共交通信息化建设与应用考核试卷
- 管道工程标准化战略实施展望与挑战应对考核试卷
- 港口及航运设施工程合同管理考核试卷
- 租赁市场客户关系维护与管理考核试卷
- 深海打捞装备的作业安全标准制定与实施考核试卷
- 涤纶纤维在高端运动品牌的技术创新与市场应用趋势考核试卷
- 海洋石油钻探的钻井工程优化考核试卷
- 生物质能源项目风险评估与管理考核试卷
- 江汉艺术职业学院《数码图形处理》2023-2024学年第二学期期末试卷
- 江西旅游商贸职业学院《运动解剖学》2023-2024学年第二学期期末试卷
- 美国加征关税从多个角度全方位解读关税课件
- 期中(试题)-2024-2025学年人教精通版(2024)英语三年级下册
- 2025中考英语热点话题阅读《哪吒2魔童闹海》
- 定额〔2025〕1号文-关于发布2018版电力建设工程概预算定额2024年度价格水平调整的通知
- 《思想政治教育方法论》考研(第3版)郑永廷配套考试题库及答案【含名校真题、典型题】
- UL9540A标准中文版-2019储能系统UL中文版标准
- 一种基于STM32的智能门锁系统的设计-毕业论文
- 极域电子教室解决方案
- JA系列电子天平使用说明书
- 《质量管理体系文件》GB-T-19001-2016-质量管理体系-要求最新
- 山岭重丘区二级公路综合设计

评论
0/150
提交评论