



版权说明:本文档由用户提供并上传,收益归属内容提供方,若内容存在侵权,请进行举报或认领
文档简介
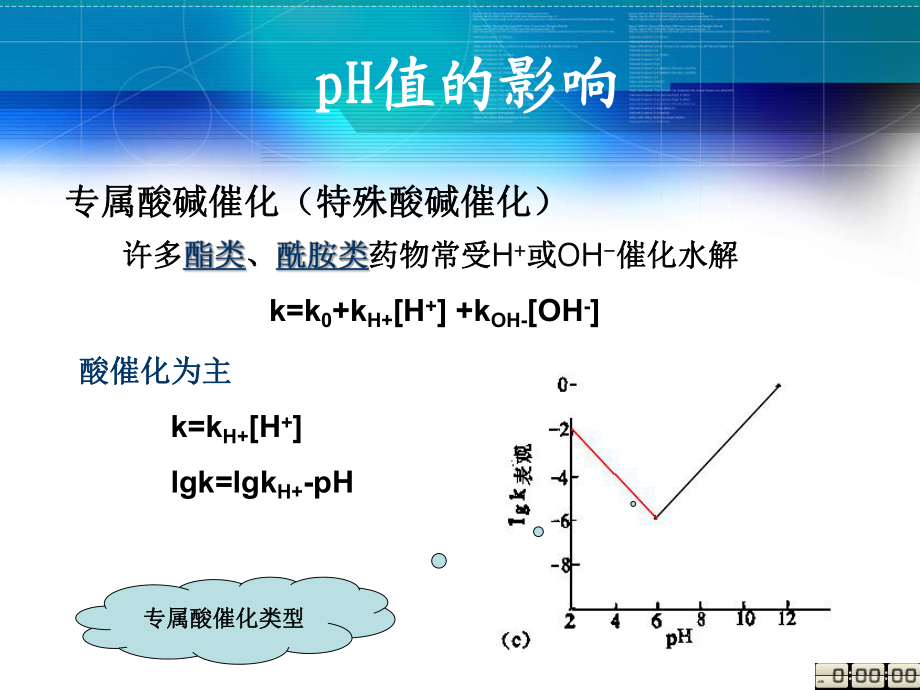
1、 药物制剂稳定性影响因素药物制剂稳定性影响因素的研究的研究影响药物制剂稳定性的因素影响药物制剂稳定性的因素处处 方方 因因 素素外外 界界 因因 素素影响药物制剂稳定性的因素影响药物制剂稳定性的因素表面活性剂表面活性剂离子强度(离子强度()溶剂溶剂pH(广义酸碱催化)(广义酸碱催化)pH(专属酸碱催化专属酸碱催化)处方处方因素因素处方中的基质与辅料处方中的基质与辅料外界外界因素因素pHpH值的影响值的影响专属酸碱催化(特殊酸碱催化)专属酸碱催化(特殊酸碱催化)许多许多、药物常受药物常受H H+ +或或OHOH- -催化水解催化水解k=k0+kH+H+ +kOH-OH-酸催化为主酸催化为主k=k
2、H+H+lgk=lgkH+-pH专属酸催化类型专属酸催化类型pHpH值的影响值的影响k=k0+kH+H+ +kOH-OH-碱催化为主碱催化为主k=kOH-OH-lgk=lgkOH-+lgkW +pH专属碱催化类型专属碱催化类型pHpHmm最最稳稳定定pHpH值值pHpHmm= pk= pkw w- log- log1 12 21 12 2k kOH-OH-k kH+H+pHpH值的影响值的影响药液的药液的pHpH值不仅影响药物的值不仅影响药物的, ,而且影响药物的而且影响药物的 如:吗啡如:吗啡 pH 4 pH 4 稳定稳定pH 5.5pH 5.57.07.0氧化速率迅速增大氧化速率迅速增大
3、肾上腺素肾上腺素pHpH氧化速率氧化速率 维生素维生素C CpH2.5pH2.5氧化速率氧化速率pHpH值的调节值的调节注意事项:注意事项:一、利于制剂的稳定性一、利于制剂的稳定性二、不影响药物的溶解性能二、不影响药物的溶解性能三、注意到药效及用药安全性三、注意到药效及用药安全性尽量采用与药物本身具有相同离子的酸或碱进行调节尽量采用与药物本身具有相同离子的酸或碱进行调节pHpH值的影响值的影响广义酸碱催化(一般酸碱催化)广义酸碱催化(一般酸碱催化)按照按照Bronsted-LowryBronsted-Lowry酸碱理论酸碱理论广义的广义的酸酸:给出给出质子的物质质子的物质广义的广义的碱碱:接受
4、接受质子的物质质子的物质有些药物也可被广义的酸碱催化水解。有些药物也可被广义的酸碱催化水解。这种催化作用叫广义的酸碱催化或一般酸碱催化。这种催化作用叫广义的酸碱催化或一般酸碱催化。常用的缓冲剂:常用的缓冲剂:醋酸盐、磷酸盐、枸橼酸盐、硼酸盐醋酸盐、磷酸盐、枸橼酸盐、硼酸盐pHpH恒定法试验恒定法试验判断是否据广义酸碱催化作用判断是否据广义酸碱催化作用溶剂的影响溶剂的影响( (一一) )介电常数介电常数 溶剂对制剂稳定性的影响复杂,无普遍规律,通过实验来确定。溶剂对制剂稳定性的影响复杂,无普遍规律,通过实验来确定。大多数降解反应大多数降解反应-属于离子反应属于离子反应-介电常数显著影响制剂的稳定
5、性。介电常数显著影响制剂的稳定性。 介电常数的大小能影响离子与离子间的引力介电常数的大小能影响离子与离子间的引力-影响降解速度。影响降解速度。lg k=lg k- kZAZB 若若进攻离子与药物离子的电荷符号相同采用介电常数低的溶剂进攻离子与药物离子的电荷符号相同采用介电常数低的溶剂如:甘油如:甘油、乙醇、丙二醇等,能够降低药物的水解速度、乙醇、丙二醇等,能够降低药物的水解速度。 1/1/ lgklgk k k 如:巴比妥钠注射液常用如:巴比妥钠注射液常用60%60%丙二醇作溶剂丙二醇作溶剂 若进攻离子与药物离子的电荷符号相反(异号反应),采用介电常若进攻离子与药物离子的电荷符号相反(异号反应
6、),采用介电常数低的溶剂不能达到提高稳定性的目的数低的溶剂不能达到提高稳定性的目的 1/1/ lgklgk k k ( (二二) ) 极极性性 lgK=lgK0+V/2.303RT(SA+ SB- +)当生成物的极性小于反应物的极性时,不易溶于溶剂,当生成物的极性小于反应物的极性时,不易溶于溶剂,需要较大的活化能达到活化态,使分解速度减慢。需要较大的活化能达到活化态,使分解速度减慢。相反当生成物的极性大于反应物的极性时,相反当生成物的极性大于反应物的极性时,则极性溶剂会加速反应。则极性溶剂会加速反应。离子强度离子强度 反应中,一些中性介质组份反应中,一些中性介质组份如:如:NaClNaCl存在
7、的浓度不同而存在的浓度不同而使降解速度改变,使降解速度改变,该现象属于该现象属于离子强度离子强度的影响的影响又称又称一级盐效应一级盐效应,原盐效应原盐效应Brsted-Bjerrum方程方程对药物降解速度影响关系式对药物降解速度影响关系式lgK=lgK0+1.02ZAZB 一些易水解的药物,加入表面活性剂可使稳定性的增加一些易水解的药物,加入表面活性剂可使稳定性的增加如如: :苯佐卡因易受碱催化水解,苯佐卡因易受碱催化水解, 在在5%5%的十二烷基硫酸钠溶液中,的十二烷基硫酸钠溶液中,3030 C C时的时的t t1/21/2增加到增加到11501150分钟分钟 不加十二烷基硫酸钠时则为不加十
8、二烷基硫酸钠时则为6464分钟分钟这是因为表面活性剂在溶液中形成胶束(胶团),这是因为表面活性剂在溶液中形成胶束(胶团),“屏障屏障”一些药物,加入表面活性剂会加快降解一些药物,加入表面活性剂会加快降解如:如:聚山梨酯聚山梨酯8080可使维生素可使维生素D D3 3的稳定性降低的稳定性降低表面活性剂的影响表面活性剂的影响表面活性剂对制剂稳定性的影响建立在实验基础上表面活性剂对制剂稳定性的影响建立在实验基础上一些半固体剂型如软膏、霜剂,药物的稳定性与制剂处一些半固体剂型如软膏、霜剂,药物的稳定性与制剂处方的基质有关。方的基质有关。如:如:聚乙二醇促进软膏剂中氢化可的松的分解聚乙二醇促进软膏剂中氢
9、化可的松的分解 促进阿司匹林栓剂中阿司匹林的水解促进阿司匹林栓剂中阿司匹林的水解维生素维生素U U片采用糖粉和淀粉为赋形剂,则产品变色,若片采用糖粉和淀粉为赋形剂,则产品变色,若应用磷酸氢钠,再辅以其它措施,产品质量则有所提高。应用磷酸氢钠,再辅以其它措施,产品质量则有所提高。硬脂酸镁会加乙酰水杨酸的水解硬脂酸镁会加乙酰水杨酸的水解 处方中基质或赋形剂的影响处方中基质或赋形剂的影响微生物微生物影响药物制剂稳定性的因素影响药物制剂稳定性的因素金属离子金属离子空气空气湿度与水分湿度与水分光线光线温度温度外界外界因素因素包装材料包装材料温度的影响温度的影响VanVan t Hofft Hoff规则规
10、则温度每升高温度每升高1010,反应速度增加,反应速度增加2 2-4-4倍倍 k=Ae-E/RTlgk=lgA-Ea/2.303R 1/TArrheniusArrhenius指数定律指数定律 lgk1/T的图形中可以看出,的图形中可以看出,Ea越大,越大,则直线斜率越大,说明在温度升高时,则直线斜率越大,说明在温度升高时,对降解速度的影响也较大。对降解速度的影响也较大。斜率斜率=-Ea=-Ea2.303R2.303R截距截距=lgA=lgA斜率斜率 活化能活化能截距截距 频率因子频率因子A A低温低温( (如室温如室温) )和其他指定温度下的和其他指定温度下的k k在在2525时降解时降解10
11、10所需时间所需时间t t0.90.9lgk2/k1=Ea/2.303R (T2-T1)/T2T1a a值越大,温度变化,值越大,温度变化,kk值变化越明显值变化越明显制剂中药物的降解反应,制剂中药物的降解反应,Ea一般为一般为10-30kcalmoI扩散过程或光解反应,扩散过程或光解反应,E E在在2 2-3kcaI.mol-3kcaI.mol-1-1热解反应,其热解反应,其E E为为50-70 50-70 kcaI.molkcaI.mol-1-1不适合用升温进行加速试验不适合用升温进行加速试验lgk=lgA-Ea/2.303R1/T(3)某些制剂,如乳膏剂、软膏、乳剂等在升温后可能改变物理
12、状态,影响反应机理某些制剂,如乳膏剂、软膏、乳剂等在升温后可能改变物理状态,影响反应机理下列情况下不能应用下列情况下不能应用Arrhenius方程方程(1)在高温时,制剂或容器中的水分蒸发或重新分配在高温时,制剂或容器中的水分蒸发或重新分配-制剂中水分的量与温度有关;制剂中水分的量与温度有关;(2)在降解过程中,参加反应的组分与温度有关;在降解过程中,参加反应的组分与温度有关;制备、储存过程制备、储存过程:加热温度、加热时间加热温度、加热时间(如:溶解、提取、灭菌)(如:溶解、提取、灭菌)剂型设计剂型设计(如:固体制剂)(如:固体制剂)工艺选择工艺选择(如:冷冻干燥)(如:冷冻干燥)低温贮存低
13、温贮存光线的影响光线的影响 光子的能量与波长成反比,光线波长越短,能量越大光子的能量与波长成反比,光线波长越短,能量越大因而,紫外线更易激发化学反应,加速药物的分解。因而,紫外线更易激发化学反应,加速药物的分解。 光化降解:光化降解:有些药物分子受辐射(光线)作用使分子活化而产有些药物分子受辐射(光线)作用使分子活化而产生分解的反应生分解的反应,其速度与系统的温度无关其速度与系统的温度无关这种易被光降解的物质叫光敏感物质。这种易被光降解的物质叫光敏感物质。如:如:喹诺酮类、维生素喹诺酮类、维生素B2B2、吗啡、可待因、肾上腺素、吗啡、可待因、肾上腺素 制备、储存过程制备、储存过程:避光操作、避
14、光包装避光操作、避光包装湿度和水分的影响湿度和水分的影响青霉素盐类粉针剂青霉素盐类粉针剂维生素维生素C C片片乙酰水杨酸片等乙酰水杨酸片等固体制剂固体制剂固体表面吸附了一层液膜固体表面吸附了一层液膜固体药物产生降解反应固体药物产生降解反应例如:例如:药物是否容易吸湿药物是否容易吸湿取决其取决其(CRH%CRH%)的大小的大小如:如:氨苄青霉素极易吸湿,其临界相对湿度仅为氨苄青霉素极易吸湿,其临界相对湿度仅为47%47%,如果在,如果在相对湿度(相对湿度(RH%RH%)75%75%的条件下,放置的条件下,放置2424小时,可吸收水分约小时,可吸收水分约2 20%0%,同时粉末溶化。,同时粉末溶化
15、。这些原料药物的水分含量,一般水分控制在这些原料药物的水分含量,一般水分控制在1%1%左左右,水分含量越高分解越快。右,水分含量越高分解越快。 湿度和水分的影响湿度和水分的影响氧气氧气引起药物制剂氧化引起药物制剂氧化1.1.氧在水中有一定的溶解度氧在水中有一定的溶解度2.2.在药物容器空间的空气中,存在着一定量的氧在药物容器空间的空气中,存在着一定量的氧生产上一般在溶液中和容器空间通入惰性气体如二生产上一般在溶液中和容器空间通入惰性气体如二氧化碳或氮气,置换其中的氧。氧化碳或氮气,置换其中的氧。固体制剂真空包装固体制剂真空包装加入抗氧剂(强还原剂;链反应阻化剂;协同剂)加入抗氧剂(强还原剂;链
16、反应阻化剂;协同剂)空气的影响空气的影响原辅料、溶剂、容器以及操作过程中使用的工具等。原辅料、溶剂、容器以及操作过程中使用的工具等。微量金属离子对自动氧化反应有显著的催化作用微量金属离子对自动氧化反应有显著的催化作用如:如:0.00020.0002mol/Lmol/L的铜能使维生素的铜能使维生素C C氧化速度增大氧化速度增大10 00010 000倍。倍。 铜、铁、钴、镍、锌、铅等离子都有促进氧化作用。铜、铁、钴、镍、锌、铅等离子都有促进氧化作用。 选用纯度高的原辅料选用纯度高的原辅料操作过程不要使用金属器具操作过程不要使用金属器具加入螯合剂加入螯合剂金属离子的影响金属离子的影响1.1.要排除
17、外界因素的干扰,要排除外界因素的干扰,2.2.要考虑包装材料与药物制剂的相互作用要考虑包装材料与药物制剂的相互作用通常使用的有玻璃、塑料、橡胶及一些金属通常使用的有玻璃、塑料、橡胶及一些金属装样试验装样试验包装材料的影响包装材料的影响增加药物制剂稳定性的方法增加药物制剂稳定性的方法制剂中药物的化学降解途径制剂中药物的化学降解途径酯类、酰胺类、甙类酯类、酰胺类、甙类酚类、烯醇类、芳胺类、其酚类、烯醇类、芳胺类、其他类药物他类药物异构化反应、光学异构化异构化反应、光学异构化几何异构化几何异构化水解降解水解降解(一)酯类药物的水解(一)酯类药物的水解 含酯键药物的水溶液在酸碱条件下生成醇和酸含酯键药
18、物的水溶液在酸碱条件下生成醇和酸 内酯在碱性条件下易水解开环内酯在碱性条件下易水解开环(二)酰胺类药物的水解(二)酰胺类药物的水解 酰胺类药物水解以后生成酸与胺酰胺类药物水解以后生成酸与胺(三)其它药物的水解(三)其它药物的水解 苷类、嘧啶类等苷类、嘧啶类等例如:阿糖胞苷在酸性溶液中,脱氨水解为阿糖脲苷。例如:阿糖胞苷在酸性溶液中,脱氨水解为阿糖脲苷。 在碱性溶液中,嘧啶环破裂,水解速度加快。在碱性溶液中,嘧啶环破裂,水解速度加快。一、延缓水解的方法一、延缓水解的方法 调节调节pHpH1 控制温度控制温度2 改变溶剂改变溶剂3 改变剂型改变剂型4调整调整pHpH值值 考虑稳定性、溶解性、疗效考
19、虑稳定性、溶解性、疗效调整至最稳定调整至最稳定pHpH值范围值范围根据药物的溶解性调整根据药物的溶解性调整减小药品的刺激性减小药品的刺激性 调节剂调节剂常用:盐酸、氢氧化钠常用:盐酸、氢氧化钠与药物本身相同的酸碱与药物本身相同的酸碱尽可能低浓度或无催化作用的缓冲系统尽可能低浓度或无催化作用的缓冲系统控制温度控制温度 操作温度操作温度 操作时间操作时间 操作工艺操作工艺改变溶剂改变溶剂 非水溶剂非水溶剂 混合溶剂混合溶剂改变剂型改变剂型 固体制剂固体制剂粉针剂粉针剂干糖浆剂干糖浆剂颗粒剂颗粒剂氧化降解氧化降解 氧化过程有时与光化分解、水解等过程共存氧化过程有时与光化分解、水解等过程共存 药物的氧化作用与化学结构有关药物的氧化作用与化学结构有关如:如:酚类、烯醇类、芳胺类、吡唑酮类、噻嗪类药物酚类、烯醇类、芳胺类、吡唑酮类、噻嗪类药物 药物氧化后,不仅效价损失,而且可能产生颜药物氧化后,不仅效价损失,而且可能产生颜色或沉淀。有些药物即使被氧化极少量,亦会色或沉淀。有些药物即使被氧化极少量,亦会色泽变深或产生不良气味,严重影响药品的质色泽变深或产生不良气味,严重影响药品的质量,甚至成为废品。量,甚至成为废品。 二、防止氧化的方法二、防止氧化的方法 充惰性气体充惰性气体1 调节调节pHpH值值1 添加抗氧剂和协同抗氧剂添
温馨提示
- 1. 本站所有资源如无特殊说明,都需要本地电脑安装OFFICE2007和PDF阅读器。图纸软件为CAD,CAXA,PROE,UG,SolidWorks等.压缩文件请下载最新的WinRAR软件解压。
- 2. 本站的文档不包含任何第三方提供的附件图纸等,如果需要附件,请联系上传者。文件的所有权益归上传用户所有。
- 3. 本站RAR压缩包中若带图纸,网页内容里面会有图纸预览,若没有图纸预览就没有图纸。
- 4. 未经权益所有人同意不得将文件中的内容挪作商业或盈利用途。
- 5. 人人文库网仅提供信息存储空间,仅对用户上传内容的表现方式做保护处理,对用户上传分享的文档内容本身不做任何修改或编辑,并不能对任何下载内容负责。
- 6. 下载文件中如有侵权或不适当内容,请与我们联系,我们立即纠正。
- 7. 本站不保证下载资源的准确性、安全性和完整性, 同时也不承担用户因使用这些下载资源对自己和他人造成任何形式的伤害或损失。
最新文档
- 2025国家电投集团数字科技有限公司招聘10人备考题库(第三批)有完整答案详解
- 2025科技日报社招聘事业单位人员2人备考题库及参考答案详解1套
- 2026四川成都市青羊区妇幼保健院招聘2人备考题库及参考答案详解1套
- 2026江西赣州市第二十中学春季学期顶岗教师招聘备考题库完整参考答案详解
- 2026河南省统一考试录用公务员10429人备考题库及一套答案详解
- 企业员工绩效评估与激励制度手册
- 2025浙江省律师协会秘书处招聘工作人员4人备考题库及参考答案详解1套
- 2025下半年贵州遵义市市直事业单位选调56人备考题库及参考答案详解
- 2026江苏南京大学图书馆安全保卫和消防人员备考题库及参考答案详解
- 2026中铁十一局集团有限公司专业人才招聘1人备考题库及答案详解一套
- 电力工程有限公司管理制度制度范本
- 科研伦理与学术规范-课后作业答案
- 《混凝土结构工程施工规范》
- 安全防范系统安装维护员题库
- mbd技术体系在航空制造中的应用
- 苗木育苗方式
- 通信原理-脉冲编码调制(PCM)
- 省直单位公费医疗管理办法实施细则
- 附录 阿特拉斯空压机操作手册
- JJG 693-2011可燃气体检测报警器
- GB/T 39557-2020家用电冰箱换热器

评论
0/150
提交评论