



版权说明:本文档由用户提供并上传,收益归属内容提供方,若内容存在侵权,请进行举报或认领
文档简介
第四章第一节无机非金属材料
主角——硅
4.1.1人教版必修一
第四章非金属及其化合物(SiClSN)1/43
经过以下图片你能总结归纳出硅元素在自然界中存在吗?观察与思考2/431.自然界硅元素主要存在于:岩石、沙子和土壤2.地壳中含量:排在第二位,氧后面.3.自然界硅存在形态:硅无游离态单质状态
只有化合态:经常有硅氧化物和硅酸盐(一)硅元素在自然界中存在和含量3/43
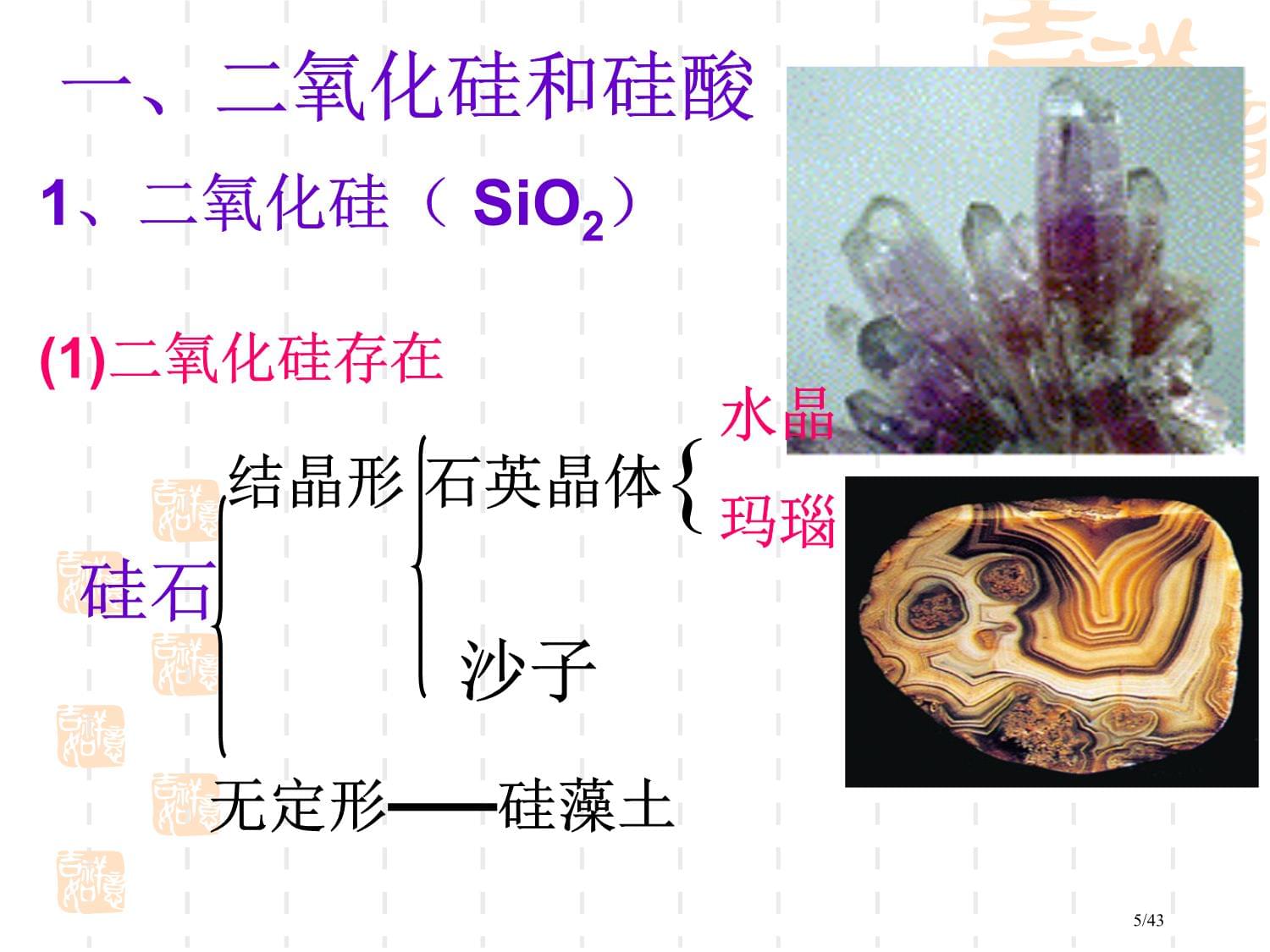
你能画出碳和硅原子结构示意图,并归纳出硅与碳在元素周期表中位置与结构吗?(二)硅位置与结构CSi碳和硅在自然界中存在形式有所不同的原因是什么?思考:4/43一、二氧化硅和硅酸1、二氧化硅(SiO2)(1)二氧化硅存在结晶形石英晶体无定形——硅藻土{水晶玛瑙硅石沙子5/43每1个Si原子周围结合4个O原子,Si在中心,O在四个顶角.
同时每1个O原子周围结合2个Si原子相结合。
硅原子——[SiO2]四面体二氧化硅中硅原子与氧原子个数比为1:2,用SiO2来表示二氧化硅组成,表示Si与O原子个数比,不是分子式是化学式科学视野(2)二氧化硅结构6/433、从下列图你能知道二氧化硅有什么用途吗?SiO2主要用作装饰、石英坩埚、光纤7/43当代通信用光缆光学纤维胃镜用光导纤维做无开刀手术光导纤维手术头灯8/43二氧化碳
二氧化硅
状态物理性质化学性质与水反应与碱反应与碱性氧化物反应与酸反应用途CO2+H2O=H2CO3CO2+2NaOH=Na2CO3+H2OCO2+Na2O=Na2CO3不反应SiO2
+2NaOH=Na2SiO3
+H2OSiO2+CaO=CaSiO3固态熔点低气态熔点高、硬度大——
SiO2
+4HF=SiF4↑+2H2O
人工降雨,灭火等
装饰、石英坩埚、光纤(3)二氧化硅物理和化学性质和用途9/431、试验室盛装NaOH溶液试剂瓶为何用橡胶塞而不用玻璃塞?
SiO2
+2NaOH=Na2SiO3
+H2ONaOH溶液能与玻璃中SiO2反应生成Na2SiO3,使瓶塞部分粘结而无法打开。所以盛装NaOH溶液试剂瓶不能用玻璃塞而要用橡胶塞。
图4-6试验室盛放NaOH溶液试剂瓶动动脑筋10/433、某同学依据SiO2既可与碱反应,也能与氢氟酸反应,推断SiO2为两性氧化物.是否正确?动动脑筋2、试验室为何不用玻璃瓶盛装氢氟酸?
HF能腐蚀玻璃,所以,盛装氢氟酸不能用玻璃试剂瓶而要用塑料瓶。SiO2
+4HF=SiF4↑+2H2O
此反应惯用于雕刻玻璃
不正确。因为二氧化硅只跟氢氟酸反应,不跟其它酸反应,而是属于酸性氧化物。11/43想一想:怎样设计试验制取H2SiO3呢?
2、硅酸(H2SiO3)
温馨提醒:CO2+H2O=H2CO3
,不过SiO2不能与水直接化合成H2SiO3。Na2CO3+2HCl=2NaCl+H2O+CO2↑原理:强酸制弱酸(1)制备:12/43
制取原理:强酸制弱酸现象结论化学方程式离子方程式滴入酚酞后溶液变为红色,再滴入稀盐酸,溶液红色变浅至无色,同时有白色胶状沉淀产生a、Na2SiO3溶液呈碱性,b、可溶性硅酸盐与盐酸反应生成不溶于水硅酸,阅读书本P65并探究试验4-1Na2SiO3+2HCl==2NaCl+H2SiO3↓SiO32-+2H+==H2SiO3↓13/43生成硅酸逐步聚合而形成硅酸溶胶,经干燥脱水就形成硅酸干胶,称为“硅胶”。常惯用做干燥剂。(3)用途(2)物理性质:硅酸是一个白色固体,溶解度很小,而且是一个弱酸,酸性比H2CO3还弱。14/43离子方程式为:SiO32-+H2O+CO2==CO32-+H2SiO3↓Na2SiO3+H2O+CO2==Na2CO3+H2SiO3↓
想一想用什么试验事实能够证实硅酸酸性比碳酸弱?向可溶性硅酸盐溶液中通入二氧化碳气体,出现白色浑浊,即用H2CO3可制得H2SiO3
,可证实H2SiO3
酸性比H2CO3弱。(强酸制弱酸)15/43小结(二)硅酸
H2SiO3(一)二氧化硅SiO2
(2)硅胶用途:干燥剂,吸附剂,催化剂载体。(1)试验室制取方法(强酸制弱酸):
Na2SiO3+2HCl=H2SiO3(胶体)+2NaCl
(2)酸性氧化物Ⅰ、与碱反应SiO2+2NaOH=Na2SiO3+H2O
Ⅱ、与碱性氧化物反应SiO2+CaO=CaSiO3(1)特征
SiO2+4HF=SiF4↑+2H2O16/43课堂练习1.地壳中含量第一和第二两种元素所形成化合物不含有性质是()
A.熔点很高B.与水反应生成对应酸
C.可与烧碱反应生成盐D.坚硬2、以下试剂能贮存在磨口玻璃塞试剂瓶里是()A.HF溶液 B.KOH溶液C.盐酸D.水玻璃BC17/434.以下物质改变,不能经过一步化学反应完成是()A.CO2→H2CO3B.SiO2→Na2SiO3C.Na2O→Na2CO3D.SiO2→H2SiO3
3.能证实硅酸酸性弱于碳酸酸性试验事实是()A.CO2溶于水形成碳酸,SiO2难溶于水B.CO2通入可溶性硅酸盐中析出硅酸C.高温下SiO2与碳酸盐反应生成CO2D.氯化氢通入可溶性碳酸盐溶液中放出气体,通入可溶性硅酸盐溶液中生成硅酸沉淀BD18/43【作业】书本P814、5、6、7、8、9、10同时导学19/43第四章第一节无机非金属材料
主角——硅
4.1.2
人教版必修一
第四章非金属及其化合物(SiClSN)20/43二、硅酸盐1、定义:硅酸盐是由硅、氧、金属元素组成化合物总称2、性质:硅酸盐种类很多,大多数难溶于水,最常见可溶性硅酸盐是Na2SiO3,K2SiO33、表示方法:(1)化学式法:适合用于简单硅酸盐如:Na2SiO3,K2SiO3、CaSiO3等。21/43(2)氧化物法:要领:两边原子个数守恒格式:金属氧化物.二氧化硅.水次序:金属氧化物书写次序按金属活动次序表22/43实例Na2SiO3Na2O•SiO223/43高岭石Al2(Si2O5)(OH)4Al2O3·2SiO2·2H2O24/43
K2O·2Al2O3·6SiO2·2H2OK(Al2Si3O10)(OH)225/434、硅酸钠(Na2SiO3)白色固体,易溶于水;Na2SiO3水溶液俗称水玻璃,又称泡花碱,是一个无色粘稠液体,是一个矿物胶,黏性很强,能够作黏胶剂和木材防火剂。阅读书本P65并探究试验4-2放入蒸馏水放入硅酸钠饱和溶液现象结论
水分蒸发后燃烧水分蒸干后不燃烧硅酸钠能防火水不能防火(1)、硅酸钠物理性质26/43问一问硅酸钠水溶液久置在空气中会出现什么现象?为何?硅酸钠水溶液久置在空气中会出现白色浑浊。因为发生以下反应:(2)、硅酸钠化学性质化学性质相对稳定,不能燃烧,不易被腐蚀,热稳定性好。Na2SiO3+CO2+H2O=Na2CO3+H2SiO3↓27/43(3)、用途作肥皂填料;用做建筑、纸张黏合剂;木材、织物防腐剂及防火剂。②与盐反应①与酸反应(强酸制弱酸)Na2SiO3+2HCl=2NaCl+H2SiO3↓CaCl2+Na2SiO3=CaSiO3↓
+2NaCl5、硅酸盐工业产品传统硅酸盐工业三大产品有:玻璃、陶瓷、水泥。28/43[练习]1.以下说法正确是()A.陶瓷、玻璃、水泥都是硅酸盐产品B.水晶、玛瑙、光纤、硅胶主要成份都是SiO2C.SiO2很稳定,与全部酸都不反应D.将石棉(CaMg3Si4O12)化学式改写成氧化物形式:3(MgO·CaO)·4SiO2A29/43三、硅单质(Si)2、物理性质:3、化学性质有金属光泽灰黑色固体,熔点高,硬度大。1、存在形式{晶体硅无定形硅你能依据硅原子结构推测硅单质可能含有化学性质么?30/43②在高温条件下,单质硅能与O2和Cl2等非金属单质反应。3、Si化学性质①常温下化学性质不活泼,只能跟F2、HF和NaOH溶液反应。Si+2F2=SiF4Si+4HF=SiF4↑+2H2↑
Si+2NaOH+H2O=Na2SiO3+2H2↑Si+O2SiO231/43工业上,用焦炭在高温下还原石英砂可制得粗硅SiO2+2C=Si(粗)+2CO↑
①
,又能跟氯气反应经提纯得到SiCl4后再用氢气还原制得纯硅:Si(粗)+2Cl2=SiCl4
②
,SiCl4+2H2=Si(纯)+4HCl③。依据以上反应回答以下问题:(1)反应①中焦炭做()A.还原剂B.氧化剂C.二者都不是(2)反应②属于(),反应③属于()A.化合反应B.分解反应C.氧化还原反应D.非氧化还原反应E.置换反应4、硅工业制备AACCE32/435、用途:太阳能电池、计算机芯片半导体材料信息技术等材料人造卫星、登月车、火星探测器等动力设备新能源。硅太阳能电池硅芯片是各种计算机、微电子产品关键观看下列图片总结单质硅的用途33/43【作业】书本P801、2、3、11、12同时导学34/43看一看你能指出常见硅酸盐产品有哪些吗
35/43科学视野新型陶瓷人造关节36/43高压钠灯高温结构陶瓷1.氧化铝陶瓷37/43陶瓷机械零件38/43三、新型无机非金属材料特征1.能承受高温、强度高。比如:氮化硅陶瓷在1200℃左右高温下,仍含有很高强度,可用来制造汽轮机叶片、轴承、永久性模具等。39/432.含有电学特征,一些新型无机非金属材料能够作
温馨提示
- 1. 本站所有资源如无特殊说明,都需要本地电脑安装OFFICE2007和PDF阅读器。图纸软件为CAD,CAXA,PROE,UG,SolidWorks等.压缩文件请下载最新的WinRAR软件解压。
- 2. 本站的文档不包含任何第三方提供的附件图纸等,如果需要附件,请联系上传者。文件的所有权益归上传用户所有。
- 3. 本站RAR压缩包中若带图纸,网页内容里面会有图纸预览,若没有图纸预览就没有图纸。
- 4. 未经权益所有人同意不得将文件中的内容挪作商业或盈利用途。
- 5. 人人文库网仅提供信息存储空间,仅对用户上传内容的表现方式做保护处理,对用户上传分享的文档内容本身不做任何修改或编辑,并不能对任何下载内容负责。
- 6. 下载文件中如有侵权或不适当内容,请与我们联系,我们立即纠正。
- 7. 本站不保证下载资源的准确性、安全性和完整性, 同时也不承担用户因使用这些下载资源对自己和他人造成任何形式的伤害或损失。
最新文档
- 自主创业档案模板
- 2024年特许金融分析师考试回顾试题及答案
- 2024年特许金融分析师考试考试心得试题及答案
- 高速收费站现场安全培训
- 2024年特许金融分析师学习心得试题及答案
- 湖北省武汉市江夏区、蔡甸、黄陂、新洲四区2024-2025学年九年级(上)期末历史试卷
- 教导主任个人工作总结11
- 金融理论与CFA考试的融合试题及答案
- 泌尿系感染的预防和护理
- 食管癌放疗病人的护理查房
- 2025年中国票据融资行业发展现状、市场运行态势及发展前景预测报告
- 生物-九师联盟2025届高三2月质量检测巩固卷(G)(九师一模)试题和答案
- 2025年仲裁法考试试题及答案
- 2024年成都市新津区卫健系统招聘笔试真题
- 2025年电梯修理作业证理论考试练习题(100题)含答案
- 2025年公务车辆租赁合同范本
- 2025年生物制药市场分析:生物制药行业规模以上企业数量超过1148家
- 2025年包头钢铁职业技术学院单招综合素质考试题库带答案
- T-ZJWL 001-2024 大宗商品供应链金融动产质押监管仓储服务规范
- 2025年河南对外经济贸易职业学院单招职业技能测试题库附答案
- 非遗文化之漆扇介绍课件

评论
0/150
提交评论