



版权说明:本文档由用户提供并上传,收益归属内容提供方,若内容存在侵权,请进行举报或认领
文档简介
1、中学高一化学备课组中学高一化学备课组化学反应的应用化学方程式化学方程式氧化剂:氧化剂:MnO2 还原剂:还原剂:HCl离子方程式离子方程式MnO2 4H 2Cl Mn2 Cl2 2H2OMnO2 + 4HCl(浓)(浓)= MnCl2 Cl2 2H2O失2e得2eMnO2 + 4HCl(浓)= MnCl2 Cl2 2H2O一套完整的氯气制取装置应该包括一套完整的氯气制取装置应该包括哪几步?哪几步?气体收集装置气体收集装置尾气处理装置尾气处理装置气体净化装置气体净化装置气体发生装置气体发生装置根据反应物根据反应物的状态和反的状态和反应条件选用应条件选用根据气体的根据气体的水溶性和对水溶性和对空气
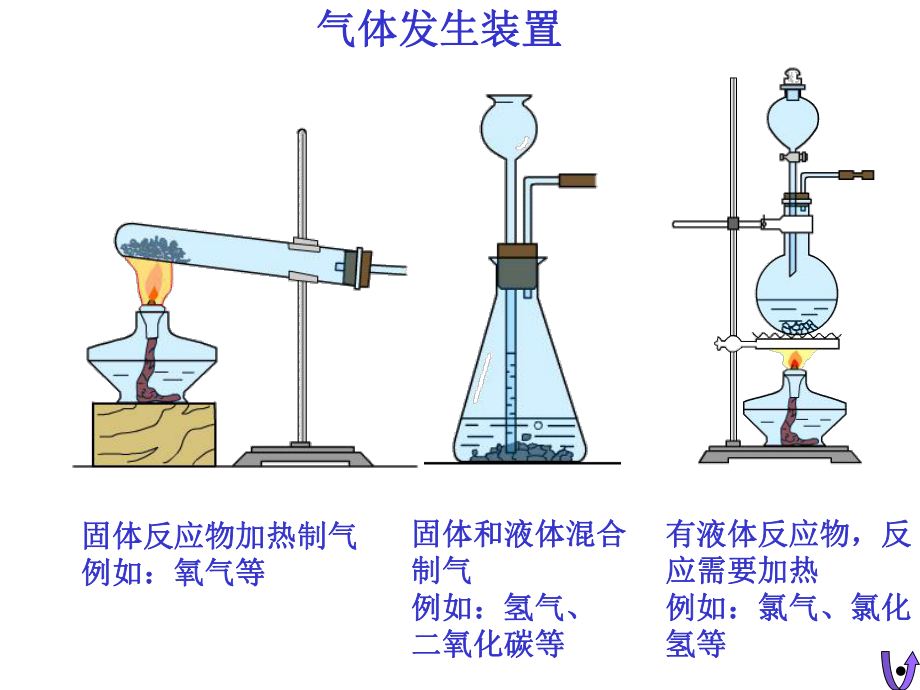
2、的相对空气的相对密度选用密度选用尾气有毒或尾气有毒或污染空气,污染空气,不能直接排不能直接排空空向上排空气法向上排空气法向下排空气法向下排空气法排水法排水法点燃点燃用试剂吸收用试剂吸收固体固体固体固体固体液体固体液体固体固体(液体液体)液体液体根据气体的根据气体的性质和制取性质和制取要求选择要求选择除杂、除杂、干燥干燥发生装置发生装置 净化装置净化装置收集装置收集装置尾气处理尾气处理装置装置固体反应物加热制气固体反应物加热制气例如:氧气等例如:氧气等固体和液体混合固体和液体混合制气制气例如:氢气、例如:氢气、二氧化碳等二氧化碳等有液体反应物,反有液体反应物,反应需要加热应需要加热例如:氯气、氯
3、化例如:氯气、氯化氢等氢等气体发生装置气体发生装置 净净 化化 装装 置置固态试剂液态试剂收集比空气重收集比空气重的气体的气体例如:氧气、例如:氧气、 氯气氯气收集难溶或微溶收集难溶或微溶于水的气体于水的气体例如:氧气、氢气例如:氧气、氢气 一氧化碳一氧化碳收集比空气轻的收集比空气轻的气体气体例如:氢气、氨气例如:氢气、氨气气体收集装置气体收集装置尾气的处理尾气的处理难以吸收的可以点燃处理,选用难以吸收的可以点燃处理,选用D。练习:请选出练习:请选出Cl2 、HCl 、CO尾气处理的装置尾气处理的装置ABCD说明:吸收溶解速度不很快,溶解度也不很大的气体用装置说明:吸收溶解速度不很快,溶解度也
4、不很大的气体用装置A;若气体在吸收剂中溶速快且溶解度极大,易倒吸,选用若气体在吸收剂中溶速快且溶解度极大,易倒吸,选用B;少量尾气可以集于气球中,选用少量尾气可以集于气球中,选用C;讨论:讨论:制取氯气的过程中可能产生哪些杂质气体,制取氯气的过程中可能产生哪些杂质气体,如何除去,如何除去,A瓶中是什么试剂,用于除去哪种杂质?瓶中是什么试剂,用于除去哪种杂质?那那B瓶呢?瓶呢?A B C D发生装置-除杂装置干燥装置-收集装置-吸收装置气气体体发发生生装装置置分液漏斗圆底烧瓶酒精灯铁架台(带铁圈铁夹)石棉网导管双孔塞【合作探究【合作探究2】1、根据氯气实验室制备的原理,应选择什么类型的发生装、根
5、据氯气实验室制备的原理,应选择什么类型的发生装置?置? 用到的仪器有哪些?用到的仪器有哪些?问题讨论问题讨论1.为什么不能加强热?为什么不能加强热?2.还能选用其他试剂反应制取氯气吗?还能选用其他试剂反应制取氯气吗?3.工业上制取氯气的方法?工业上制取氯气的方法?防止氯化氢挥发防止氯化氢挥发用用KMnO4或者或者KClO3代替代替MnO2或者用浓硫酸和氯化钠代替或者用浓硫酸和氯化钠代替HCl电解食盐水电解食盐水问题讨论问题讨论1.为什么不能加强热?为什么不能加强热?答:浓盐酸有较强的挥发性,若加强热会使氯气中有大量的答:浓盐酸有较强的挥发性,若加强热会使氯气中有大量的氯化氢杂质,另外也降低了氯
6、化氢杂质,另外也降低了HCl的利用率。的利用率。2.还能选用其他试剂反应制取氯气吗?还能选用其他试剂反应制取氯气吗?3.工业上制取氯气的方法?工业上制取氯气的方法?答:电解饱和食盐水可以得到氯气、氢气和氢氧化钠答:电解饱和食盐水可以得到氯气、氢气和氢氧化钠答:可以用高锰酸钾答:可以用高锰酸钾(氯酸钾氯酸钾)和浓盐酸反应和浓盐酸反应2KMnO4 16HCl 2KCl 2MnCl2 5Cl2 8H2O也可以氯化钠、浓硫酸和也可以氯化钠、浓硫酸和MnO2混合制取氯气混合制取氯气2NaCl 3H2SO4 MnO2 2NaHSO4 MnSO4 Cl2 2H2O请思考图示的装置都有哪些用途?请思考图示的装
7、置都有哪些用途?洗气和收集作用洗气和收集作用1.从从A口进气,从口进气,从B口排出瓶内的空气,口排出瓶内的空气,可收集可收集O2、Cl2等比空气重的气体等比空气重的气体2.从从B口进气,从口进气,从A口排出瓶内的空气,可收集口排出瓶内的空气,可收集H2、NH3等比空气轻的气体。等比空气轻的气体。5.在瓶内充满水,从在瓶内充满水,从B口进气,将瓶内水从口进气,将瓶内水从A口压出,可作为口压出,可作为排水取气装置。排水取气装置。3. 在瓶内加入适量液态净化剂,从在瓶内加入适量液态净化剂,从A口进气,口进气,B口出气,可作口出气,可作为气体净化装置。为气体净化装置。4.瓶内加入适量浓硫酸,从瓶内加入
8、适量浓硫酸,从A口进气,口进气,B口出气,可作为气体口出气,可作为气体干燥装置。干燥装置。! 可以用排饱和食盐水饱和食盐水的方法收集Cl2氢气制取的简易装置图氢气制取的简易装置图实验步骤实验步骤 现象现象结论或解释结论或解释 锌片上有气泡锌片上有气泡锌与稀硫酸反应锌与稀硫酸反应铜片上无气泡铜片上无气泡铜与硫酸不反应铜与硫酸不反应铜片上有气泡铜片上有气泡? ?Cu2、原电池工作原理、原电池工作原理较活泼的金属较活泼的金属失去电子发生氧化反应,失去电子发生氧化反应,电子从较活泼金属(电子从较活泼金属(负极负极)通过外电)通过外电路流向路流向较不活泼的金属(正极)较不活泼的金属(正极) 。实验探究形
9、成原电池的条件实验探究形成原电池的条件(可以)(可以)(可以)(可以)(可以)(可以)(不可以)(不可以)形成条件一:形成条件一:活泼性不同的两个电极活泼性不同的两个电极负极:较活泼的金属负极:较活泼的金属正极:较不活泼的金属、石墨等正极:较不活泼的金属、石墨等第一组实验第一组实验(可以)(可以)(不可以)(不可以)形成条件二:电极需插进电解质溶液中;形成条件二:电极需插进电解质溶液中;第二组实验第二组实验实验探究形成原电池的条件实验探究形成原电池的条件第三组实验第三组实验实验探究形成原电池的条件实验探究形成原电池的条件形成条件三:必须形成闭合回路形成条件三:必须形成闭合回路(不可以)(不可以
10、)原电池的工作原理原电池的工作原理较活泼的金属发生较活泼的金属发生氧化反应氧化反应,电子从较电子从较活泼的金属活泼的金属(负极负极)通过外电路流向较通过外电路流向较不活泼的金属不活泼的金属(正极正极)。 电子流向:负极 正极导线导线两极相连形成闭合电路两极相连形成闭合电路组成原电池的条件组成原电池的条件有两种活动性不同的金属(或有两种活动性不同的金属(或一种是非金属导体)作电极一种是非金属导体)作电极电极材料均插入电解质溶液中电极材料均插入电解质溶液中1.1.铜片上的气体是什么?铜片上的气体是什么? 2.2.氢元素原来以什么形式存在?氢元素原来以什么形式存在?3. 从电子得失的角度分析,从电子
11、得失的角度分析,H H+ +如何如何 转变成氢气?转变成氢气?思考:思考: 1. 1. 电子从何而来?电子从何而来?2. 2. H为何不直接在锌片上为何不直接在锌片上得电子而在铜片上得电子?得电子而在铜片上得电子?讨论:讨论:实验步骤实验步骤现象现象结论或解释结论或解释 电流计指针偏转电流计指针偏转导线中有导线中有电流通过电流通过测干电池时,电流计指测干电池时,电流计指针偏向针偏向 极方向极方向测铜锌原电池时,电流测铜锌原电池时,电流计指针偏向计指针偏向 片方向片方向锌片为负极锌片为负极 铜片为正极铜片为正极 正正铜铜ZnCuZnCuABCDEF下列哪些装置能构成原电池?自己动手做一做。下列哪
12、些装置能构成原电池?自己动手做一做。G水果水果未构成闭合回路未构成闭合回路负极(锌片):负极(锌片): Zn 2e - = Zn 2+负极(锌片):负极(锌片): Zn 2e - = Zn 2+正极(石墨):正极(石墨): 2H+2e - = H2 正极(铜片):正极(铜片): Cu2+ + 2e - = Cu 请将氧化还原反应:请将氧化还原反应:Fe + Cu2+ = Cu + Fe2+Fe比比Fe不活泼的金属或石墨不活泼的金属或石墨 CuSO4 、CuCl2等等设计成一个原电池。设计成一个原电池。负极:负极:正极:正极:电解质溶液:电解质溶液:X X、Y Y、Z Z都是金属,把都是金属,把X X浸入浸入Z Z的硝酸的硝酸盐溶液中,盐溶液中,X X的表面有的表面有Z Z析出,析出,X X与与Y Y组成原电池时,组成原电池时,Y Y为电池的负极。为电池的负极。X X、
温馨提示
- 1. 本站所有资源如无特殊说明,都需要本地电脑安装OFFICE2007和PDF阅读器。图纸软件为CAD,CAXA,PROE,UG,SolidWorks等.压缩文件请下载最新的WinRAR软件解压。
- 2. 本站的文档不包含任何第三方提供的附件图纸等,如果需要附件,请联系上传者。文件的所有权益归上传用户所有。
- 3. 本站RAR压缩包中若带图纸,网页内容里面会有图纸预览,若没有图纸预览就没有图纸。
- 4. 未经权益所有人同意不得将文件中的内容挪作商业或盈利用途。
- 5. 人人文库网仅提供信息存储空间,仅对用户上传内容的表现方式做保护处理,对用户上传分享的文档内容本身不做任何修改或编辑,并不能对任何下载内容负责。
- 6. 下载文件中如有侵权或不适当内容,请与我们联系,我们立即纠正。
- 7. 本站不保证下载资源的准确性、安全性和完整性, 同时也不承担用户因使用这些下载资源对自己和他人造成任何形式的伤害或损失。
最新文档
- 大班儿童游戏活动方案
- 大厂员工活动方案
- 壁画创意美术活动方案
- 地产公寓活动方案
- 垂钓大赛布置活动方案
- 地产保价活动方案
- 场景应用活动方案
- 天猫满减活动方案
- 外卖小吃店开业活动方案
- 业务提升培训季活动方案
- 幼儿教师沟通技巧培训课件
- 2025年安全知识竞赛题库及答案(共150题)
- GB 45673-2025危险化学品企业安全生产标准化通用规范
- 医院培训课件:《新生儿早期基本保健专家共识(2020)解读》
- 南开强基计划试题及答案
- 区块链与慈善公益商业模式的创新与探索
- 2025年湖南中考英命题分析及复习备考策略指导课件
- 近岸海域生态环境问题分析
- 2025重庆水务环境集团招聘8人笔试参考题库附带答案详解
- 2025至2030中国大型啤酒厂产业运行态势与竞争格局研究报告
- 陕投(赣州)信丰能源发展集团有限公司招聘笔试题库2025

评论
0/150
提交评论