



版权说明:本文档由用户提供并上传,收益归属内容提供方,若内容存在侵权,请进行举报或认领
文档简介
任课教师:王锦程AOffice:友谊校区创新大厦B-1318Telmail:jchwang@
上节回顾Helmholtz自由能
等温=可逆<自发等温等容
=可逆>不可逆Helmholtz自由能判据
=可逆>不可逆Gibbs自由能
等温等压
Gibbs自由能判据
=可逆>不可逆=可逆<自发
2/28上节回顾Gibbs自由能变化计算
简单物理变化
等温过程
液体和固体
理想气体
简单变温过程
一般不设计变温步骤直接套公式或设计路径
相变过程可逆相变
不可逆相变
设计路径混合过程
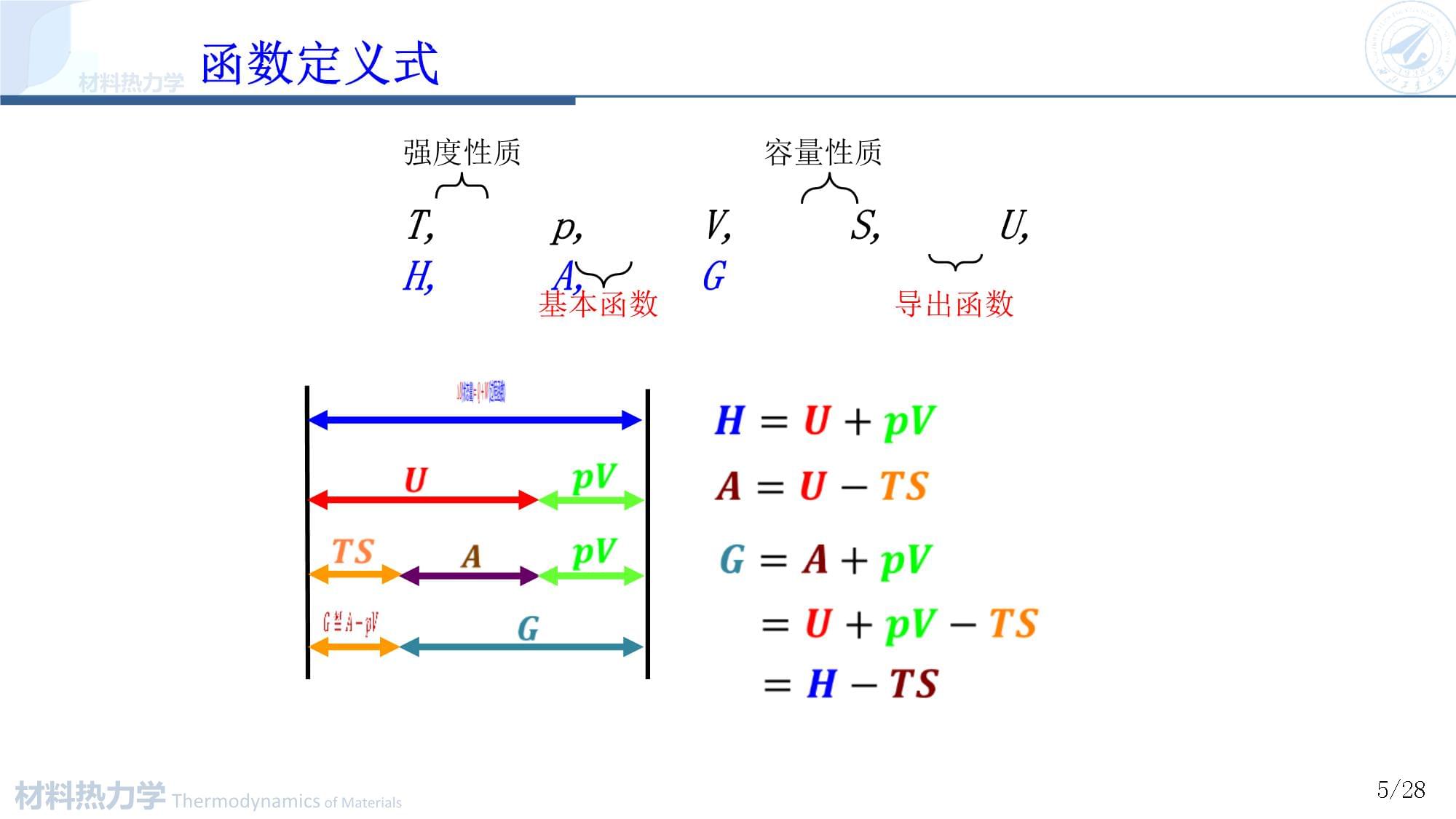
3/28第四章热力学函数及基本关系式4.1亥姆霍兹自由能和吉布斯自由能4.2热力学基本关系式4.3麦克斯韦关系式4.4热力学基本关系式的应用4.5自由能的计算4/28函数定义式T,p,V,S,U,H,A,G强度性质容量性质基本函数导出函数
5/28热力学基本方程
第一定律第二定律第一、第二定律联用得
6/28热力学基本方程
7/28关于热力学基本方程dU=TdS-pdV,下面的说法中准确的是TdS是过程热pdV是体积功TdS是可逆热在可逆过程中,-pdV等于体积功,TdS即为过程热ABCD提交8/28单选题1分热力学基本方程
封闭系统的热力学基本方程(Gibbs公式)
对复杂物理变化和化学变化:必须可逆(3)用途:计算双变量系统的状态函数变,得出其他结论(2)对双变量系统(组成不变的均相封闭系统):不可逆也可用9/28关于热力学基本方程dU=TdS-pdV的适用条件,下列说法错误的是适用于组成不变的均相封闭系统,不作非体积功的一切过程适用于可逆不做非体积功的过程过程可逆不是必须的,但无非体积功是必须的。可适用于单组分理想气体的任何过程ABCD提交10/28单选题1分特性函数A
在均相前提下,对任意一个特性函数,通过求偏导数等数学手段,可得到任何状态函数。
11/28对应系数关系式
得:
令则
与其余三个基本关系式做类似处理可得相应关系式对比12/28
(1)证明推演(2)分析问题
用途:对应系数关系式对应系数关系式基本关系式13/28Maxwell关系式以易测量代替难测量
(1)
(2)
(3)
(4)
全微分的性质
Euler倒易关系导出其他具有普遍意义的公式、结论14/28下列四个关系式中,哪一个不是麦克斯韦关系式?
ABCD提交15/28单选题1分根据热力学第一、二定律推导4个热力学基本关系式、8个对应关系式及4个麦克斯韦关系式(双变量系统)。课堂练习16/28
课堂练习17/28第四章热力学函数及基本关系式4.1亥姆霍兹自由能和吉布斯自由能4.2热力学基本关系式4.3热力学基本关系式的应用4.4自由能的计算18/28热力学证明题的常用数学方法恒等式两边同时微分或同时求导在一定条件下,将微分式两端同除以某个量的微分比较系数法。利用不同方法分别写出同一函数的全微分,在自变量相同的情况下,可以分别比较各项的系数
利用二阶偏导数与求导次序无关
不可测量
可测量
等压膨胀系数等容压力系数等温压缩系数19/28两个重要热力学性质
等温对V求偏微分
根据Maxwell关系式不易测定
20/28已知基本公式
等温对p求偏微分
两个重要热力学性质21/28
热力学性质变化的推导
22/28
麦克斯韦关系式
当体积不变时,熵随温度的变化值为:
该式适用于一般凝聚态体系的熵变计算。用于熵随温度、体积变化计算热力学性质变化的推导23/28
用于熵随温度、压力变化的计算
当压力不变时,熵温度的的变化值为:
适用于一般凝聚态体系的熵随温度变化计算
热力学性质变化的推导24/28热力学性质变化的推导
25/28
热力学性质变化的推导
26/28
4.100℃的恒温槽中有一带活塞的导热圆筒,筒中为2molN2(g)及装于小玻璃瓶中的3molH2O(l)。环境压力及系统压力维持120kPa不变。今将小玻璃瓶打碎,液态水蒸发至平衡态。求过程的Q,W,ΔU,ΔH,ΔS,ΔA及ΔG
温馨提示
- 1. 本站所有资源如无特殊说明,都需要本地电脑安装OFFICE2007和PDF阅读器。图纸软件为CAD,CAXA,PROE,UG,SolidWorks等.压缩文件请下载最新的WinRAR软件解压。
- 2. 本站的文档不包含任何第三方提供的附件图纸等,如果需要附件,请联系上传者。文件的所有权益归上传用户所有。
- 3. 本站RAR压缩包中若带图纸,网页内容里面会有图纸预览,若没有图纸预览就没有图纸。
- 4. 未经权益所有人同意不得将文件中的内容挪作商业或盈利用途。
- 5. 人人文库网仅提供信息存储空间,仅对用户上传内容的表现方式做保护处理,对用户上传分享的文档内容本身不做任何修改或编辑,并不能对任何下载内容负责。
- 6. 下载文件中如有侵权或不适当内容,请与我们联系,我们立即纠正。
- 7. 本站不保证下载资源的准确性、安全性和完整性, 同时也不承担用户因使用这些下载资源对自己和他人造成任何形式的伤害或损失。
最新文档
- 制造业供应链协同与效率提升制度
- 2025年水质采样试题及答案
- 2025-2030针织家纺产业政府战略管理与区域发展战略研究咨询报告
- 2025年事业单位招聘考试艺术设计类综合专业能力测试试卷及答案
- 2025年事业单位教师招聘考试生物学科专业知识模拟试题试卷及答案
- 2025新企业人力资源管理师核心考点题库及答案
- 2026冷链物流温控技术升级投资回报率分析
- 2026冬季低温环境下药用饲料保存稳定性改良技术专题
- 2025年出租车行业政府购买服务报告
- 2026农产品冷链物流行业市场供需整合及投资评估规划分析研究报告
- 村镇建设科培训课件
- 药物作用机制-洞察及研究
- 室内概念方案汇报
- 物业营销溢价方案(3篇)
- 2025年浙江省中考科学试题卷(含答案解析)
- 太原市城市供热收费管理办法
- 白癜风诊疗共识(2025版)解读
- T/CHES 89-2022河湖生态流量保障实施方案编制技术导则
- 青岛2025年自主招生考试物理试卷试题及答案详解
- 四川省旅游景区精细化管理服务质量提升规范 DB51 -T 2878-2022
- 2025年河南工业贸易职业学院单招职业技能考试题库及答案1套

评论
0/150
提交评论