



版权说明:本文档由用户提供并上传,收益归属内容提供方,若内容存在侵权,请进行举报或认领
文档简介
江苏省扬州市三年(2019-2021)中考化学真题分类汇编-非选择题
影响化学反应速率的因素探究(共2小题)
1.(2021•扬州)氧气支持生命活动,也是一种重要的化工原料。
(1)实验室用如图所示的装置制取少量氧气。
②锥形瓶内发生反应的化学方程式是。
(2)工业上有多种制取氧气的方法,如:
方法一:在低温、加压条件下,将空气液化。然后将温度升高至-196℃〜-183℃之间,使液态氮气先蒸
发,剩余液态氧气储存于钢瓶里。
方法二:利用电解水的方法制取氧气,将得到的氧气干燥。在低温,加压条件下,使之转化为液态,储存
于钢瓶里。
①从构成物质的微粒视角分析,在方法一空气液化过程中,主要改变的是。
②某工厂用方法二制取氧气,发现氧气的产量略小于理论值,且所得氧气中有淡淡的鱼腥气味。从元素守
恒角度分析,该鱼腥气味的气体是(填化学式或名称)。
(3)氢气和氧气在Pd基催化剂表面可反应生成H#2,其微观示意图如图:
吸附解离结合脱离
OH•。,///,////,///,,,Pd基催化剂
“解离”时,结构被破坏的分子是(填化学式)。
(4)为探究双氧水的分解,进行以下两个实验:
①氯化物对双氧水分解的影响。
反应条件:6.0mL3(»双氧水,0.1g氯化物,室温;实验时间:1.5h。
实验数据如表所示:
氯化物NaCl
MgCl2CuC12
第1页共36页
放出氧气的体积/mL2.04.0420.0
双氧水的分解率/%0.300.6063.18
由上表可知,双氧水保存时应绝对避免引入的离子是(写离子符号)。
②pH对双氧水分解的影响。
反应条件:6.0mL30%双氧水,反,C;
用NaOH溶液调pH;实验时间:L5h。
实验结果如图所示:
双100
氧
水80
的60
分
解40
率20
/%0
567891011
pH
由图可知,pH为(填数字)时,双氧水的分解率最高。
(5)用双氧水可制得“鱼浮灵”“钙多宝”。
①“鱼浮灵”主要成分是2Na£03・3H2()2,可迅速增加水体含氧量,其原因是
②“钙多宝”主要成分是Ca02,常温下能与水反应生成氢氧化钙和氧气。长时间存放的过氧化钙中含有主
要杂质是(填化学式)、Ca(Oil)2
2.(2020•扬州)实验室可利用Zn与稀硫酸的反应制取上。
(1)用浓硫酸配制稀硫酸的操作为(填字母),用玻璃棒引流,并不断搅拌。
A.将浓硫酸缓缓注入盛有水的烧杯中
B.将水缓缓注入盛有浓硫酸的烧杯中
(2)Zn与稀硫酸反应的化学方程式为o
⑶图1所示的仪器B、D的名称为、,组装制取H2的发生装置应选用的仪器为(填
字母)。
图1图2
(4)为收集并准确测量他的体积,在装入药品前,需检查装置的
第2页共36页
(5)相同条件下%密度比空气小,利用该性质可以通过法收集112,若用图2所示装置测量生成
%的体积,%应从(填“甲”或“乙”)管通入。
(6)为探究影响Zn与稀硫酸反应快慢的因素,进行以下三组实验,室温下,取颗粒大小相同的锌粒与足
量的稀硫酸反应,测量产生10矶112(通常状况)所需的时间,下表为实验数据:
实验编号硫酸的质量分数/%硫酸的体积/mL锌粒的质量/g时间/s
11010178
21010257
3401019
①比较实验1、2的数据,可以得出的结论是o
②由实验数据可知,该实验中对Zn与稀硫酸反应快慢影响较大的因素是0
③比较不同条件下锌粒与稀硫酸反应的快慢有不同的方法,除测量产生相同体积的%所需的时间,还可采
用的测量方法是(写出一种)。
二氧化碳的化学性质(共1小题)
3.(2020•扬州)CO?的捕集与资源化利用是化学研究的热点。
(1)控制CO2的排放,是为了减缓效应,加压水洗法可捕集CO?,是因为压强增大时CO?在水中的
溶解度(填“增大”“不变”或“减小”)。
(2)石灰石循环法可用于捕集烟气中的CO?,该方法以CaO捕集CO?,将所得产物在高温下煨烧可重新获
得CaO,高温煨烧时反应的化学方程式为,生成的CaO疏松多孔,结构与活性炭相似,其在捕集
过程中对(%具有良好的性。
(3)对CO2气体加压、降温,可获得干冰。从构成物质的微粒视角分析,该过程主要改变的是。
干冰能用于人工降雨,是因为。
(4)CO?可用于食品保鲜,实验测得气体中CO?的体积分数与溶液pH的关系如图1所示。
①气体中CO?体积分数增大时,造成图示变化的主要原因是溶液中浓度增大(填化学式)。
②智能化食品包装通过颜色变化显示包装内CO2气体含量的变化,举出一种可通过颜色变化用于该智能化
第3页共36页
包装的物质o
(5)已知一定条件下CO?与L以质量比11:2反应可生成CH】.与该反应类似,不同条件下,CO?与也反
m(C0o)
应也能生成甲醇(CH.Q)。生成甲醉时参加反应的CO?与%的质量比—一「=。
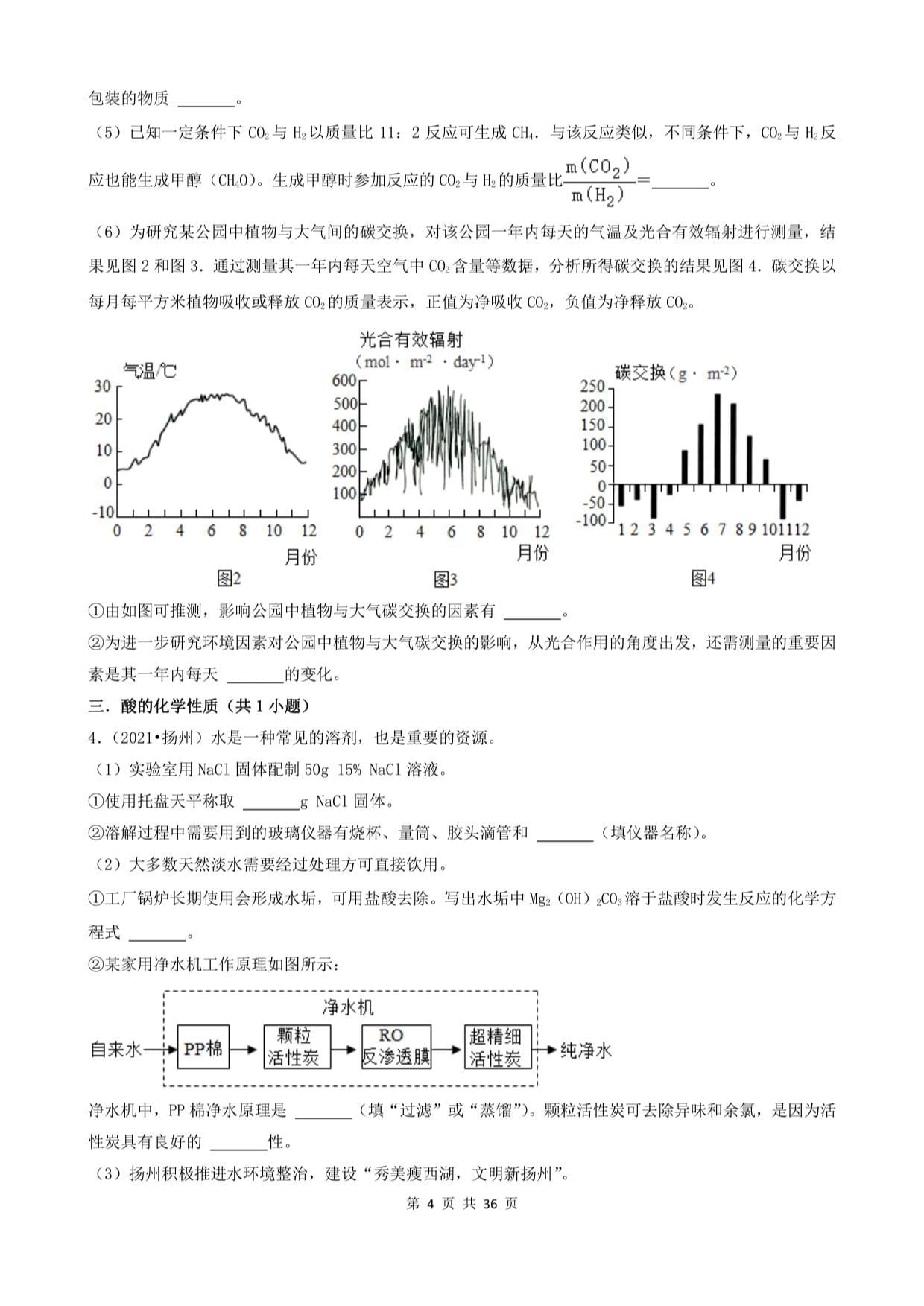
(6)为研究某公园中植物与大气间的碳交换,对该公园一年内每天的气温及光合有效辐射进行测量,结
果见图2和图3.通过测量其一年内每天空气中CO?含量等数据,分析所得碳交换的结果见图4.碳交换以
每月每平方米植物吸收或释放C02的质量表示,正值为净吸收CO?,负值为净释放C02o
光合有效辐射
碳交换m")
图2图3
①由如图可推测,影响公园中植物与大气碳交换的因素有
②为进一步研究环境因素对公园中植物与大气碳交换的影响,从光合作用的角度出发,还需测量的重要因
素是其一年内每天的变化。
三.酸的化学性质(共1小题)
4.(2021•扬州)水是一种常见的溶剂,也是重要的资源。
(1)实验室用NaCl固体配制50g15%NaCl溶液。
①使用托盘天平称取gNaCl固体。
②溶解过程中需要用到的玻璃仪器有烧杯、量筒、胶头滴管和(填仪器名称)。
(2)大多数天然淡水需要经过处理方可直接饮用。
①工厂锅炉长期使用会形成水垢,可用盐酸去除。写出水垢中Mg?(Oil)£0:;溶于盐酸时发生反应的化学方
程式o
②某家用净水机工作原理如图所示:
净水机中,PP棉净水原理是(填“过滤”或“蒸储”)。颗粒活性炭可去除异味和余氯,是因为活
性炭具有良好的性。
(3)扬州积极推进水环境整治,建设“秀美瘦西湖,文明新扬州”。
第4页共36页
①环保部门对水质进行长期监测,将水质从“优”到“劣”分为I〜V类。由如图可知,近年来扬州市II〜
in类优良水质百分比明显呈(填“上升”或“下降”)趋势。由此推断,扬州市主要水域的水质
在(填“变好”或“变差”)。
(
来
)
五
会
皿
茶
林
眼
性
2018-2021年4月扬州全程水质类别百分比变化趋势
②产生这种变化趋势的原因可能是(填字母)。
A.夜间排放工业污水
B.清理污染河道的淤泥
C.关停或整改存在污染隐患的企业
(4)污水未经处理直接排入河流,会使水面上藻类物质大量繁殖,水质恶化。某藻类含化学式为
G。6H263(UN酒的物质,则污水中导致藻类生长过快的营养元素是(填元素名称)。
四.盐的化学性质(共1小题)
5.(2019•扬州)悔0在医药建筑等行业应用广泛。硫酸镁和木炭高温馔烧的产物为帼0(固体)、S02,C02>
CO、硫蒸气。
(1)工业上,S0?的任意排放会引起的环境问题是。化石燃料燃烧是产生SO?的主要原因,下列做
法能减少S0?排放的是(填字母)。
a.开发新能源替代化石燃料b.向高空排放SO?
(2)在高温、催化剂条件下,C0和H2可化合成燃料甲醇(CH30H),该反应中CO和H2的分子个数比为。
若C0和庆中混有H2s气体,H?S会与催化剂中的Cu在高温下发生置换反应,其中一种产物为CuS,该反应
的化学方程式为。
(3)利用如图装置对硫酸镁和木炭进行高温煨烧,并对产生的四种气体进行分步吸收或收集。
已知:常温下,硫为固体;SO?、CO2均能与NaOH溶液反应。
第5页共36页
\1gS04和c
a.NaOH溶液
b.KMM溶液
②装置B、C的作用分别是、。
③装置D的作用是o
④若将装置A中的固体隔绝空气加热至500C,就会变成蒸气,其中有一种相对分子质量为128的气体。
该气体的化学式为。
五.物质的相互转化和制备(共5小题)
6.(2021•扬州)天然气(主要成分为CH』)作为清洁能源,正逐步走进城乡居民生活。
(1)“西气东输”工程利于国家能源和产业结构调整,极大改善了沿线居民生活质量。
①为防止传输天然气的钢管被腐蚀,可采取的措施有(写出一种)。
②CH」完全燃烧的化学方程式是,该过程(填“释放”或“吸收”)能量。
③天然气的使用可有效减少酸雨形成。下列现象与酸雨有关的是。
A.石刻文物被腐蚀
B.全球海平面上升
(2)工业上以CH”为原料生产H”制取原理如图所示:
HOH:OTHzO
洗涤塔
洗涤液
已知变换塔、洗涤塔发生的主要反应依次是:CO+HC一定条件CO”+H“C02+H20=H2C0:io
①“转化炉”中有为产生,参加反应的CH”与的质量比_______。
m(H20)------
②“洗涤塔”中气体从塔底通入,水从塔顶喷淋。这样操作的优点是。
③若有32gCH,参与反应(假设各步反应都完全转化),理论上可制得gH2»
(3)我国是世界上首个成功试采海域可燃冰的国家。可燃冰是CH“被H?0分子形成的笼包裹,在海底低温
第6页共36页
和高压作用下形成的结晶物质。
①可燃冰样品常存放于液氮储存罐中,其原因是。
②可燃冰有多种结构,某H型可燃冰的化学式为。1广9上0,分析其结构发现:平均34个HzO分子构成6个
笼,每个笼只容纳一个CH,或分子。这6个笼内容纳的CH,与HR分子个数比是(填最小整数
比)。
HO―►
由2、
7.(2021•扬州)以某菱镁矿石(主要成分是MgCOs,含少量M11CO3、Si02)制取MgSOjTIW,流程如图:
(1)“酸浸”时,为了提高浸取率,除了搅拌、提高硫酸浓度外,还可采取的措施有(写出一种).
此时,MnW发生反应的化学方程式是。
(2)“转化”时主要反应是NaC10+MnS0,+H20=Mn021+NaCl+H2S0,1,氯元素反应前后化合价变化情况是
(填“升高”或“降低叽
(3)硫酸镁溶液在不同温度下进行浓缩结晶,可得到不同的晶体:
温度/℃-3.9-1.81.8—48.148.1—67.567.5—200
析出晶体
MgS04-12H20MgS04-7H20MgS04-6H20MgSOjHzO等
①“操作1”的具体操作是:蒸发浓缩滤液至表面有晶膜出现(此时MgSO,溶液已饱和)、、过滤、
洗涤、低温干燥。
②“操作1”所得滤液中能分离出一种可循环使用的物质,该物质是(填化学式)。循环使用的目
的是。
(4)已知:《尼50「7乩0中镁元素质量分数为9.76%。采用热分析法测定所得MgSOqVHzO样品中镁元素质量
分数:
①未加热前,测得样品中镁元素质量分数略大于9.76%,可能的原因是。
②高于900℃后,测得剩余固体中镁元素质量分数大于20%,可能的原因是o
(5)若用100t菱镁矿石可制得246tMgSO.j7H2O产品,忽略反应过程中镁元素损失,求该菱镁矿石中MgC03
的质量分数。(写出计算过程)
8.(2019•扬州)由氯化钢废液(杂质为FeCb及微量NaCl)制备产品BaCLVIbO的流程如图。
第7页共36页
熟石灰滤液循环95%乙醇
|废液卜》|j铁卜除钙►艮发浓缩、冷却藕卜压回f钠」产品
(1)氯化铁废液属于_______(填“纯净物”或“混合物”)。FeCL;中铁元素的化合价是。
(2)煨烧石灰石制取生石灰的化学方程式为,生石灰变成熟石灰的过程是过程(填“吸
热”或“放热”),石灰水能使紫色石蕊试液变色。石灰石和熟石灰中常用于改良酸性土壤的
是o
(3)用95%乙醇(C2H6。)洗涤滤渣可除微量NaCl.C2Hfi0由种元素组成,是化合物(填“有
机”或“无机”)。C21I6O在02中完全燃烧生成CO?和o2个CO2分子可用化学符号表示为o
煤、氢气、乙醇三种燃料中,最清洁的是。
(4)结合流程和表回答:工业上选择25℃而不选择5℃进行冷却结晶的主要原因是①滤液多次循环后,
25c与5℃结晶产品的总产率基本相同;②。
表:每次结晶时,温度对产品纯度和产率的影响
冷却结晶的温度/℃产品的纯度/%产品的产率/%
59972
259960
9.(2019•扬州)实验室以某石灰石(含少量Fe20:J为原料制备高纯CaCO:;的步骤如下。
溶解向石灰石样品中加入适量盐酸,至反应完全。
除铁加入氨水调节pH,然后加入适量Ca(0H)2,充分反应后过滤。
沉淀向滤液中补充氨水,通入C02,反应一段时间。
分离过滤、洗涤、干燥得高纯Cat%。
(1)溶解时,CaC()3、Fez()3分别与盐酸反应的化学方程式为、。判断样品已完全反应的实
验现象是。
(2)除铁时,选用Ca(0H)2而不选用NaOH,其主要原因是Ca(0H)2价格低且来源广、、;
过滤所得滤渣的主要成分为。
(3)沉淀时,其他条件相同,反应温度对CaC()3产率的影响如图。高于350c时,CaCOs产率下降的主要原
产品的实际质量
因是_______(已知:X100%)
产品的理论质量
(4)分离时,若向过滤所得滤液中加入(填化学式)并加热,则可回收加3。
(5)该实验中可以循环利用的物质有压0和o
(6)石灰厂煨烧石灰石生产CaO,若要得到28tCaO,则至少需要含CaC()390%的石灰石多少吨?(写出
计算过程,保留一位小数。)
第8页共36页
10.(2019•扬州)以MnOz为原料制备MnSOjHzO的工业流程如图。
NfnSCU溶液
滤'液
已知:①沉淀时的化学方程式为7MnS0*+7Na2co3+llH20=MnOV6Mn(0H)2・5a01+7Na2s04+6C02t
②MnSQjHzO和MnS0,«5H20易溶于水,难溶于乙醇。
③MnSO,的溶解度曲线如图1所示。
(1)溶解时,为控制80'C,在实验室可用水浴加热如图2.水浴加热需要的玻璃仪器有酒精
灯、o水浴加热的优点有。能加快溶解的方法有(写一种)。
溶
解
度
g
(3)过滤I所得滤液的溶质主要是Na2sol和。过滤时,玻璃棒的作用是。
(4)酸溶时,MnC(V6Mn(OH)z畤HQ与足量稀硫酸反应的化学方程式为。
(5)请补充完整由流程中“酸溶”所得MnSO,溶液制备MnSO^H2O的实验方案:将MnSO”溶液转移至蒸发
皿中,,在高于40℃时趁热过滤,,100℃烘干得MnSOjIbO。
六.根据化学反应方程式的计算(共1小题)
第9页共36页
11.(2020•扬州)以FeS(V7H2。为原料制备铁红(Fe2O3)的一种方法如图:
H:O芋
FeSCU-7H:O—溶解冗淀回最卜",燃烧『Fe。
IJ
物质Z滤液
已知“沉淀”时的主要反应为:2FeSOi+H2O2+2&O=2FeO(OH)I+2H2soi
(1)FeO(OH)中铁元素的化合价为。FeO(0H)可表示为mFezC^nFe(OH)3,旦=。
n
(2)“沉淀”时需控制溶液的pH与反应的温度。
①“沉淀”时调节溶液的初始pH约为4,过程中应始终保持溶液的pH为3.0~4.5,需不断加入物质Z调
节溶液的pH,Z应具备的性质有(填字母)。
A.能与酸反应
B.能与碱反应
C.不与FeO(0H)反应
②“沉淀”时反应温度不宜过高,其原因是«
(3)“过滤”后需对固体进行洗涤与干燥。洗涤时被除去的沾于固体表面的阴离子为(填离子符
号)。
(4)“煨烧”时反应的化学方程式为。
(5)如图为其他条件相同时不同煨烧温度对产品中Fez。:,质量分数的影响。煨烧温度较低时,产品中Fez。,
质量分数较低,其原因是。当煨烧温度达800℃时,继续升高温度,产品中Fe?03质量分数降低,
且铁元素质量分数升高,所得产品发黑,其可能原因是。
,FeK)3质量分数,%
99.
700750800850900
燧烧温度七
(6)用该方法制备FeQ,计算理论上13.9tFeS04«7H20(相对分子质量为278)可制得FezOs的质量(写
出计算过程)。
七.完全燃烧与不完全燃烧(共1小题)
12.(2020•扬州)空气质量意味着生活质量。
(1)下表为某同学测量的呼吸前后气体组成的实验数据(通常状况)。
物质吸入空7(体积分数/%)呼出身体(体积分数/%广
第10页共36页
氮气7875
氧气2116
二氧化碳0.034
水蒸气ab
①氮气的化学性质比较(填“稳定”或“活泼”),在呼吸前后没有发生变化,实验中呼出气体的
总体积吸入空气的总体积(填“>”“=”或
②呼吸时消耗产生C02,该过程能量(填“吸收”或“释放
(2)汽车多以汽油为燃料,辛烷(cslll8)是汽油中的一种成分。
①每114gC8H完全燃烧,需要消耗400g02,生成mgCO?和162gH20,则m=go
②与完全燃烧相比,等质量的GHIB不完全燃烧时会产生C0,消耗Oz的质量_______(填“偏大”“相等”
或“偏小”),除污染环境外,燃料不完全燃烧还会产生的问题是(写出一种)。
(3)“远在高空是地球卫士,近在身边是健康杀手。”臭氧(03)对环境的作用需辩证地认识。
①高空中臭氧层能吸收紫外线。有学者认为,致冷剂氟利昂进入高空大气后会产生氯原子(C19,引发以
下反应:Cl.+03—C10*+02I
2C10•=2C1«+O2II
Cl•加快了上述转化过程总反应的速率,但自身的质量和化学性质在总反应前后没有发生变化,其作用
是,该转化过程总反应的化学方程式为。
②地面附近的臭氧是一种空气污染物,臭氧属于(填“单质”或“化合物”),03可表示一个(填
“原子”“分子”或“离子”)。
(4)有人提出:你吸入的空气中的某个氧原子可能自于若干年前恐龙的身体。该说法表达的观点是
(填字母)。
A.分子聚集形成物质,分子在不停地运动
B.在化学变化中原子既不会产生,也不会消失
C.原子内部结构复杂,原子不是构成物质的最小微粒
八.复合材料、纳米材料(共2小题)
13.(2021•扬州)扬州被称为运河之都、文化之都和美食之都,自古人文荟萃。
(1)故人西辞黄鹤楼,烟花三月下扬州。--唐•李白
①孟浩然“下扬州”的交通工具是木船。现代游船常用玻璃钢制造船体,玻璃钢属于(填“复合
材料”或“金属材料”)。
②现代人远行可乘坐飞机。铝锂合金材料大量运用于国产C919大飞机的制造,下列不属于铝锂合金性质
的是(填字母)。
A.密度大
B.硬度大
第11页共36页
C.抗腐蚀
③汽车是重要的陆路交通工具。燃油车辆须加装尾气催化净化装置,该装置将尾气中的CO和NO转化成C02
和一种无污染的气体,发生反应的化学方程式是o
(2)天下三分明月夜,二分无赖是扬州。--唐•徐凝
①空气质量影响人们观赏明月。空气属于(填“混合物”或“纯净物”)。
②下列做法不利于改善空气质量的是(填字母)。
A.风力发电
B.徒步出行
C.垃圾露天焚烧
③煤的气化和液化可实现能源清洁化,改善空气质量。水煤气中CO和出在高温、高压和催化剂条件下合
成甲醉(CH.,0),该反应的化学方程式是。
(3)前日扬州去,酒熟美蟹蝌。--宋•梅尧臣
①蟹肉鲜美,富含蛋白质。蛋白质水溶液在加热时会生成沉淀,此沉淀(填“能”或“不能”)
重新溶解于水中。
②各种酒中都含有乙醇(C2H60)。在酿酒过程中,粮食中的(填糖类名称)先转化为葡萄糖,再
经发酵生成乙醇。
③下列食品中富含维生素C的是(填字母)。
A.盐水鹅
B.西红柿
C.大虾
14.(2019•扬州)日常生活、社会发展都与化学密切相关。
(1)3D打印机根据不同需求,使用不同材料,如铝合金、聚乙烯、碳纤维增强复合材料。其中属于无机
材料的是,属于合成材料的是,属于复合材料的是。
(2)《本草纲目》记载,杨桃具有去风热、生津止渴等功效。
①杨桃的主要成分是水,还含有糖类和蛋白质等。葡萄糖和蛋白质中属于有机高分子化合物的是,
能在人体内分解生成氨基酸的是。葡萄糖由三种元素组成•
②经测定酸杨桃的pH为1.35,甜杨桃的pH为1.81,其中酸性较强的是。(填“酸杨桃”或“甜
杨桃”)
③酸杨桃中矿质元素含量如表2.人体缺少元素易得佝偻病,缺少元素易得贫血症。如表
所列元素中,属于微量元素的是、。
表:每克酸杨桃中矿质元素的含量
矿质元素KCaZnFe
含量/mg0.3890.5870.0490.070
第12页共36页
九.生命活动与六大营养素(共1小题)
15.(2020•扬州)扬州既是世界美食之都,更是一座拥有两千多年历史的文化旅游名城。
(1)扬州早点是一张靓丽的城市名片。
①扬州包子面皮如雪。面皮的主要成分为淀粉,淀粉属于(填字母)。
A.糖类
B.油脂
C.蛋白质
②大煮干丝富含蛋白质。蛋白质在人体内转化为能被吸收的小分子化合物,这类化合物称为。
③翡翠烧卖色泽翠润,所用天然色素来自新鲜绿色蔬菜。获取天然色素时,将菜渣与菜汁分离开可采用
的方法。
(2)青砖黛瓦诉说着扬州的历史。
①《天工开物》中介绍了烧制青砖的方法,其中载有“灌水其上”“水火既济”。相关反应为水蒸气与灼热
的碳生成C0和一种气体单质,其化学方程式为。
②古代建筑工匠常用糯米灰浆粘合墙砖,糯米灰浆由糯米汁、熟石灰和砂土等混合制成。糯米灰浆属于
(填“复合材料”或“金属材料”)。熟石灰的化学式为,在空气中熟石灰最终转化为(填
化学式)。
③''帘外芭蕉惹骤雨,门环惹铜绿。”铜绿是铜发生一系列复杂反应的产物,空气中参与该反应过程的物
质有(填化学式)。
第13页共36页
江苏省扬州市三年(2019-2021)中考化学真题分类汇编-非选择题
参考答案与试题解析
影响化学反应速率的因素探究(共2小题)
1.(2021•扬州)氧气支持生命活动,也是一种重要的化工原料。
(1)实验室用如图所示的装置制取少量氧气。
(2)工业上有多种制取氧气的方法,如:
方法一:在低温、加压条件下,将空气液化。然后将温度升高至-196C〜-183C之间,使液态氮气先蒸
发,剩余液态氧气储存于钢瓶里。
方法二:利用电解水的方法制取氧气,将得到的氧气干燥。在低温,加压条件下,使之转化为液态,储存
于钢瓶里。
①从构成物质的微粒视角分析,在方法一空气液化过程中,主要改变的是微粒间的距离。
②某工厂用方法二制取氧气,发现氧气的产量略小于理论值,且所得氧气中有淡淡的鱼腥气味。从元素守
恒角度分析,该鱼腥气味的气体是6(填化学式或名称)。
(3)氢气和氧气在Pd基催化剂表面可反应生成上。2,其微观示意图如图:
“解离”时,结构被破坏的分子是H?(填化学式)。
(4)为探究双氧水的分解,进行以下两个实验:
①氯化物对双氧水分解的影响。
反应条件:6.0mL30%双氧水,0.1g氯化物,室温;实验时间:1.5h。
第14页共36页
实验数据如表所示:
氯化物NaCl
MgCl2CuCl2
放出氧气的体积/mL2.04.0420.0
双氧水的分解率/%0.300.6063.18
由上表可知,双氧水保存时应绝对避免引入的离子是CJ(写离子符号)。
②pH对双氧水分解的影响。
反应条件:6.0mL30%双氧水,60℃;
用NaOH溶液调pH;实验时间:1.5h。
实验结果如图所示:
双100
氧
水80
的60
分
解40
率20
/%0
567891011
pH
由图可知,pH为9(填数字)时,双氧水的分解率最高.
(5)用双氧水可制得"鱼浮灵"''钙多宝"。
①“鱼浮灵”主要成分是2Na2cQJ3H2O2,可迅速增加水体含氧量,其原因是碳酸钠溶液显碱性,可以促
进过氧化氢的分解。
②“钙多宝”主要成分是CaO2,常温下能与水反应生成氢氧化钙和氧气。长时间存放的过氧化钙中含有主
要杂质是CaW(填化学式)、Ca(0H)2。
【解答】解:(1)①a为固定仪器的铁架台,b为收集气体的集气瓶;
故答案为:铁架台;集气瓶。
②过氧化氢在二氧化镒催化作用下反应生成水和氧气,书写化学方程式注意配平及气体符号,所以化学方
MnOn
程式为2HO,-----=2H20+021;
MnOn
故答案为:211。/2H2O+O2t。
(2)①气态变为液态,物质本身没有变化,只是间距变小;
故答案为:微粒间的距离。
②电解水产生氧气,气体只含有氧元素,而此时有鱼腥味,与臭氧性质相似,因此此时产生了臭氧,化学
式为。3;
第15页共36页
故答案为:。3。
(3)根据题目中图像信息可以看出,氢气分子分裂为氢原子,所以发生变化的氢气;
故答案为:4。
(4)①三者阴离子相同,只有含有铜离子时,反应速率最快,所以保存时避免引入铜离子;
故答案为:Cu2\
②根据图像数据,可以看到pH=9时,此时分解率最高;
故答案为:9。
(5)①根据(4)中信息可知,碱性环境可以提高过氧化氢的分解速率,碳酸钠溶于水,形成碱性溶液,
此时含有过氧化氢,碱性环境加速过氧化氢分解,增加氧含量;
故答案为:碳酸钠溶液显碱性,可以促进过氧化氢的分解。
②过氧化钙与水反应生成了氢氧化钙,氢氧化钙吸收二氧化碳变为碳酸钙,因此杂质含有氢氧化钙和碳酸
钙;
故答案为:CaCQ”
2.(2020•扬州)实验室可利用Zn与稀硫酸的反应制取均。
(1)用浓硫酸配制稀硫酸的操作为A(填字母),用玻璃棒引流,并不断搅拌。
A.将浓硫酸缓缓注入盛有水的烧杯中
B.将水缓缓注入盛有浓硫酸的烧杯中
(2)Zn与稀硫酸反应的化学方程式为Zn+H2so尸ZnSOi+&t。
(3)图1所示的仪器B、D的名称为酒精灯、长颈漏斗,组装制取%的发生装置应选用的仪器为
(4)为收集并准确测量工的体积,在装入药品前,需检杳装置的气密性。
(5)相同条件下%密度比空气小,利用该性质可以通过向下排空气法收集H,,若用图2所示装置测
量生成H2的体积,H?应从乙(填“甲”或“乙”)管通入。
(6)为探究影响Zn与稀硫酸反应快慢的因素,进行以下三组实验,室温下,取颗粒大小相同的锌粒与足
量的稀硫酸反应,测量产生10mLH2(通常状况)所需的时间,下表为实验数据:
实验编号硫酸的质量分数/%硫酸的体积/mL锌粒的质量/g时间/s
第16页共36页
11010178
21010257
3401019
①比较实验1、2的数据,可以得出的结论是在硫酸的质量分数和体积相同时,锌粒质量越大,收集相
同体积氢气所需时间越短。
②由实验数据可知,该实验中对Zn与稀硫酸反应快慢影响较大的因素是硫酸的质量分数。
③比较不同条件下锌粒与稀硫酸反应的快慢有不同的方法,除测量产生相同体积的出所需的时间,还可采
用的测量方法是相同时间内产生氨气的体积(写出一种)。
【解答】解:(1)用浓硫酸配制稀硫酸的操作为将浓硫酸缓缓注入盛有水的烧杯中,用玻璃棒引流,并不
断搅拌,切不可将水直接到浓硫酸中,故答案为:A;
(2)锌和硫酸反应生成硫酸锌和氢气,化学方程式为Zn+H2so产ZnS0“+H2t;故答案为:Zn+H2so产ZnSO/H?
t;
(3)图1所示的仪器B、D的名称为酒精灯、长颈漏斗,实验室中制取氢气采用的是固液常温下进行的反
应,所以组装制取出的发生装置应选用的仪器为ACD;故填:酒精灯;长颈漏斗;ACD;
(4)为收集并准确测量出的体积,在装入药品前,需检查装置的装置的气密性;故答案为:气密性;
(5)相同条件下达密度比空气小,利用该性质可以通过向下排空气法收集玲,氢气的密度比水小,若用
图2所示装置测量生成也的体积,也应从乙管通入,水从甲管排出进入量筒,量筒内水的体积即为收集到
的氢气体积;故答案为:向下排空气;乙;
(6)①实验1和实验2中,硫酸的质量分数和体积相同,锌粒质量不同,比较实验1、2的数据,可以得
出的结论是锌粒质量越大,收集相同体积氢气所需时间越短;故答案为:在硫酸的质量分数和体积相同时,
锌粒质量越大,收集相同体积氢气所需时间越短;
②对比实验1和实验3可知,在硫酸的体积和锌粒质量相同的条件下,硫酸的质量分数越大,收集相同体
积氢气所需时间越短,且对Zn与稀硫酸反应快慢影响较大;故答案为:硫酸的质量分数;
③比较不同条件下锌粒与稀硫酸反应的快慢有不同的方法,除测量产生相同体积的所需的时间,还可采
用的测量方法是相同时间内产生氢气的体积;故答案为:相同时间内产生氢气的体积。
二.二氧化碳的化学性质(共1小题)
3.(2020•扬州)C0?的捕集与资源化利用是化学研究的热点。
(1)控制CO2的排放,是为了减缓温室效应,加压水洗法可捕集CO2,是因为压强增大时CO?在水中
的溶解度增大(填“增大”“不变”或“减小”)。
(2)石灰石循环法可用于捕集烟气中的CO2,该方法以CaO捕集C02,将所得产物在高温下燃烧可重新获
得CaO,高温煨烧时反应的化学方程式为CaCO,向血-CaO+CO?T,生成的CaO疏松多孔,结构与活
性炭相似,其在捕集过程中对CO?具有良好的吸附性。
第17页共36页
(3)对CO2气体加压、降温,可获得干冰。从构成物质的微粒视角分析,该过程主要改变的是分子间
隔。干冰能用于人工降雨,是因为干冰升华吸热。
(4)CO2可用于食品保鲜,实验测得气体中CO?的体积分数与溶液pH的关系如图1所示。
①气体中C02体积分数增大时,造成图示变化的主要原因是溶液中也8,浓度增大(填化学式)。
②智能化食品包装通过颜色变化显示包装内CO2气体含量的变化,举出一种可通过颜色变化用于该智能化
包装的物质石蕊试液。
(5)已知一定条件下C02与上以质量比H:2反应可生成CH”.与该反应类似,不同条件下,C02与友反
m(COo)
应也能生成甲醇(CHQ)。生成甲醇时参加反应的CO2与上的质量比--4-=22:3。
m(H2)
(6)为研究某公园中植物与大气间的碳交换,对该公园一年内每天的气温及光合有效辐射进行测量,结
果见图2和图3.通过测量其一年内每天空气中CO?含量等数据,分析所得碳交换的结果见图4.碳交换以
每月每平方米植物吸收或释放CO?的质量表示,正值为净吸收C02,负值为净释放C02。
光合有效辐射
月份
图4
①由如图可推测,影响公园中植物与大气碳交换的因素有气温、光照强度。
②为进一步研究环境因素对公园中植物与大气碳交换的影响,从光合作用的角度出发,还需测量的重要因
素是其一年内每天水蒸气含量的变化。
【解答】解:(1)大气中二氧化碳的含量过高会加剧温室效应,所以控制CO?的排放,是为了减缓温室效
应,加压水洗法可捕集C02,是因为压强增大时C02在水中的溶解度增大;故填:温室;增大;
第18页共36页
(2)石灰石的主要成分是碳酸钙,在高温的条件下,碳酸钙分解为氧化钙和二氧化碳,化学方程式为CaC03
吉*日
向‘皿CaO+CO2t,生成的CaO疏松多孔,结构与活性炭相似,其在捕集过程中对CO?具有良好的吸附性;
151
故填:CaCO,--Ca0+C02t;吸附;
(3)对CO2气体加压、降温,可获得干冰。从构成物质的微粒视角分析,该过程主要改变的是分子间隔。
干冰升华吸收热量,所以干冰能用于人工降雨,故填:分子间隔;干冰升华吸热;
(4)①气体中CO?体积分数增大时,pH变小,溶液的酸性增强,即溶液中碳酸的浓度增大;故填:H2CO:i;
②酸溶液能使紫色的石蕊试液变红色,所以可使用石蕊试液;故填:石蕊试液;
(5)在一定条件下,CO?与Hz反应能生成甲醇(CH..O)和水,化学方程式为CO?+3H—一无条件CH,O+H?O.
m(COo)
参加反应的CO?与坨的质量比一7―4—=44:(2X3)=22:3;故填:22:3;
(6)①由如图可推测,影响公园中植物与大气碳交换的因素有气温、光照强度;故填:气温、光照强度;
②从光合作用的角度出发,光合作用是植物吸收二氧化碳和水蒸气,释放出氧气,因此还需测量的重要因
素是其一年内每天水蒸气含量的变化;故填:水蒸气含量。
三.酸的化学性质(共1小题)
4.(2021•扬州)水是一种常见的溶剂,也是重要的资源。
(1)实验室用NaCl固体配制50g15%NaCl溶液。
①使用托盘天平称取7.5gNaCl固体。
②溶解过程中需要用到的玻璃仪器有烧杯、量筒、胶头滴管和玻璃棒(填仪器名称)。
(2)大多数天然淡水需要经过处理方可直接饮用。
①工厂锅炉长期使用会形成水垢,可用盐酸去除。写出水垢中Mg2(OH)2a)3溶于盐酸时发生反应的化学方
程式卜底(0H)£O3+4HCl=2MgC12+3I12O+CO2t。
②某家用净水机工作原理如图所示:
净水机中,PP棉净水原理是过滤(填“过滤”或“蒸储”)。颗粒活性炭可去除异味和余氯,是因为
活性炭具有良好的吸附性。
(3)扬州积极推进水环境整治,建设''秀美瘦西湖,文明新扬州”。
①环保部门对水质进行长期监测,将水质从“优”到“劣”分为I〜V类。由如图可知,近年来扬州市II〜
IH类优良水质百分比明显呈上升(填“上升”或“下降”)趋势。由此推断,扬州市主要水域的水质
在变好(填“变好”或“变差
第19页共36页
(
来
)
五
会
皿
茶
林
眼
性
2018-2021年4月扬州全程水质类别百分比变化趋势
②产生这种变化趋势的原因可能是BC(填字母)。
A.夜间排放工业污水
B.清理污染河道的淤泥
C.关停或整改存在污染隐患的企业
(4)污水未经处理直接排入河流,会使水面上藻类物质大量繁殖,水质恶化。某藻类含化学式为
G。6H2630Kl«N/的物质,则污水中导致藻类生长过快的营养元素是氮、磷(填元素名称)。
【解答】解:(1)①配制50gl5%NaCl溶液需要NaCl的质量为:50gX15%=7.5g;故填:7.5;
②溶解过程中需要用到的玻璃仪器有烧杯、量筒、胶头滴管和玻璃棒;故填:玻璃棒;
(2)①Mg?(OH)2c0:;溶于盐酸生成氯化镁、水和二氧化碳,发生反应的化学方程式为Mg2(OH)2co:;+4HCl
=2MgCl2+3II20+C02t;故填:Mg2(OH)2CO3+41IC1=2MgCl2+3Il20+C02t;
②净水机中,PP棉净水原理是过滤。颗粒活性炭可去除异味和余氯,是因为活性炭具有良好的吸附性;故
填:过滤;吸附;
(3)①环保部门对水质进行长期监测,将水质从“优”到“劣”分为I〜V类。由如图可知,近年来扬州
市
温馨提示
- 1. 本站所有资源如无特殊说明,都需要本地电脑安装OFFICE2007和PDF阅读器。图纸软件为CAD,CAXA,PROE,UG,SolidWorks等.压缩文件请下载最新的WinRAR软件解压。
- 2. 本站的文档不包含任何第三方提供的附件图纸等,如果需要附件,请联系上传者。文件的所有权益归上传用户所有。
- 3. 本站RAR压缩包中若带图纸,网页内容里面会有图纸预览,若没有图纸预览就没有图纸。
- 4. 未经权益所有人同意不得将文件中的内容挪作商业或盈利用途。
- 5. 人人文库网仅提供信息存储空间,仅对用户上传内容的表现方式做保护处理,对用户上传分享的文档内容本身不做任何修改或编辑,并不能对任何下载内容负责。
- 6. 下载文件中如有侵权或不适当内容,请与我们联系,我们立即纠正。
- 7. 本站不保证下载资源的准确性、安全性和完整性, 同时也不承担用户因使用这些下载资源对自己和他人造成任何形式的伤害或损失。
最新文档
- 2025版文化产业园项目策划与运营合同范本
- 2025版办公楼半包装修设计与施工合同样本
- 2025版古建筑修复劳务合同规范文本
- 2025版某局数据中心建设项目劳务分包结算执行合同
- 2025版智能仓储厂房租赁及自动化设备集成合同
- 二零二五年度电商企业数字化转型服务合同
- 二零二五年度住宅租赁代理服务全面合作协议
- 2025版加油站加油站设施设备更新改造合同
- 2025年浙江省事业单位招聘考试教师招聘语文教学评价标准学科专业知识试卷
- 二零二五年度房地产股权置换与转让合同规范
- 甲状腺相关性眼病的诊治
- 用人单位职业卫生档案(加油站)
- GB/T 35786-2017机动车电子标识读写设备通用规范
- GB/T 19378-2003农药剂型名称及代码
- 《经济学基础》教案
- DB37T242-2021建筑消防设施检测技术规程
- 供应商库入库资料
- 桥台裂缝加固处理方案
- 脚手架架在楼板上验算书
- ThinkPad X220 拆机解析深入分析
- Toolbox中文使用说明(图例)

评论
0/150
提交评论