



版权说明:本文档由用户提供并上传,收益归属内容提供方,若内容存在侵权,请进行举报或认领
文档简介
1、毕业设计外文资料翻译题 目 30万吨/年MTBE气分装置中 碳四碳五分离过程模拟研究 学院名称化学与制药工程学院 专业班级 化工09-1 学生姓名魏 红 导师姓名张文郁 二一三年五月三十日Journal of Membrane Science178 (2000) 25-34气相转移法合成MFI型沸石分子筛分离丁烷和二甲苯异构体Takaaki Matsufujia,Norikazu Nishiyamaa,Masahiko Matsukatab,Korekazu UeyamabaDivision of Chemical Engineering,Graduate School of Engineer
2、ing Science,Osaka University,bDepartment of Applied Chemistry,Waseda University摘 要 在多孔氧化铝载体上以气相转移法(VPT)制作的MFI型沸石分子筛,纯的或混合丁烷异构体的扩散测定范围在300375K.分离系数范围较理想的选择性更大。这一结果表明二元系统的正丁烷可以被选择性吸附从而得到分离。在303K对二甲苯异构体进行扩散测试.二甲苯在一元系统中最有扩散性。对二元混合物中的邻二甲苯和对二甲苯及三元混合物中邻、间、对甲苯的的扩散测试,邻二甲苯最先被扩散分离出,既而,对二甲苯逐渐减少,含量最终低于其它二甲苯异构体。间
3、二甲苯吸附在分子筛的空隙中对对二甲苯的扩散有阻止作用。2000艾斯维尔有限责任公司保留所有权利。关键词 分子筛;MFI气体分离;吸附;气相蒸馏1 简介近年来,合成沸石分子筛有水热法和气相转移(VPT)两种方法,沸石气孔的分子尺寸大小对烃类混合物的分离起着重要作用。沸石分子筛分离碳氢化合物的报道引人注目。MFI型沸石分子筛分离最常见的线性和支链烃类混合物,例如正异丁烷和正己烷/2,2-二甲基丁烷的分离已有报道。MFI有两种类型相交渠道组成的框架结构这都定义为10元环。在室温下,正异丁烷和正己烷、2,2-二甲基丁烷混合物的分离因子分别为20-60,大于600。除了线性和支链烃类混合物,也有MFI或
4、镁碱沸石分子筛分离芳烃的研究。Baertsch等报道,佐野伊特尔用氧化铝载体的水热法合成制备纯硅分子筛,如果分子筛孔径接近1nm则很难分离邻、对二甲苯,因为芳烃很难扩散过纯硅分子膜。二元及三元系统的扩散与一元系扩散类似。他们用单程转移理论解释上述结果。MFI的孔径太窄,芳烃分子不能通过,因此,扩散速度最慢的分子抑制其他物质的扩散。选择性吸附在孔隙入口似乎发挥重要作用。但是,邻对二甲苯,对二甲苯/乙苯,二甲苯/乙苯、间二甲苯/乙苯的二元混合物在380480K下,没有得到分离。他们的研究结果表明,最易透过的组分在一元系统的选择性吸附很难发生在二元和三元系统中。另外,科泽尔等得到了二甲苯的分离因子,
5、在298K(p-xylene/o-xylene)200,这表明对二甲苯/邻二甲苯二元混合物的分离因子很大程度上取决于操作温度。这也表明了气相扩散对二甲苯异构体混合物分离的可能性。以前报道,在303K下,FER分子筛对二甲苯/邻二甲苯的二元混合物的分离系数为3.1。我们希望二甲苯异构体通量大一点,更深的研究发现MFI型沸石分子筛的分离通量会更大一点,因为MFI的孔径(0.53nm0.56nm和0.51nm0.55nm)比FER的孔径(0.54nm0.42nm和0.46nm0.37nm)大。在研究中,用VPT法制备MFI分子筛。进行了一元气体扩散和丁烷异构体的混合气体分离测试。采用扩散汽化技术研究
6、二甲苯异构体在MFI膜中的扩散性能。2实验2.1初凝胶的制备以膜面积1.010-4m2,平均孔径为0.1m的多孔氧化铝作为载体。在pH值=10的条件下,把氧化铝载体处理为硅溶胶。在303K下,以硅溶胶制备铝硅酸盐溶胶30WT的SiO2、0.04WT的Al2O3和0.4WT的Na2O(日本化工有限公司)及氢氧化钠溶液(4N)(光纯化学工业有限公司)。二氧化硅与氢氧化钠溶液在303K混合,初凝胶的组成为1000二氧化硅 : 1.0氧化铝 : 210氧化钠 : 25000水。在303K下,把载体浸泡在初溶胶里处理1天。然后,把溶胶注入氧化铝载体的孔隙,持续注入1小时。2.2气相转移法结晶干凝胶涂有溶
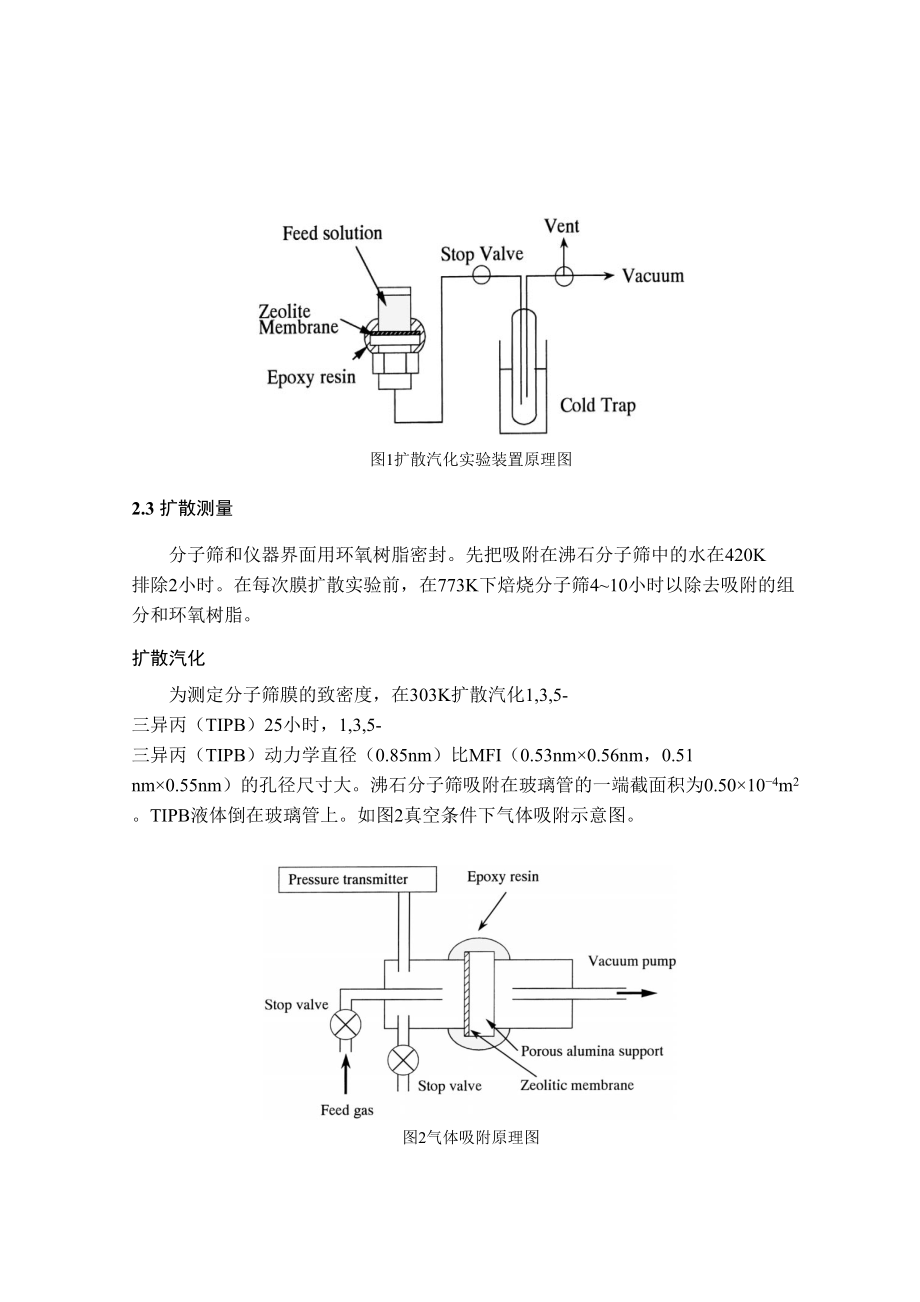
7、胶的载体在298K下放置在高压釜内干燥24小时,高压釜的容积100立方厘米。乙二胺(0.5毫升)、三乙胺(1.0毫升)和水(0.5毫升)的混合物倒入反应釜使产生蒸汽。在453K下和一定压力下结晶4天。然后在773K下,在空气中焙烧10小时。在473773K下控制升温速率0.1Kmin-1。对产品的结晶度和结构进行了X射线衍射(XRD),使用铜嘉辐射(Philips Xs Pert-MRD)分析。所产生的形态用电子显微镜(SEM,HITACHI S-2250)扫描检测。图1扩散汽化实验装置原理图2.3 扩散测量分子筛和仪器界面用环氧树脂密封。先把吸附在沸石分子筛中的水在420K 排除2小时。在每
8、次膜扩散实验前,在773K下焙烧分子筛410小时以除去吸附的组分和环氧树脂。扩散汽化为测定分子筛膜的致密度,在303K扩散汽化1,3,5-三异丙(TIPB)25小时,1,3,5-三异丙(TIPB)动力学直径(0.85nm)比MFI(0.53nm0.56nm,0.51 nm0.55nm)的孔径尺寸大。沸石分子筛吸附在玻璃管的一端截面积为0.50104m2。TIPB液体倒在玻璃管上。如图2真空条件下气体吸附示意图。图2气体吸附原理图在液氮冷却抽集器收集25小时,并配有火焰离子化检测器气相色谱仪分析。在303K下进行二甲苯异构体的扩散汽化。一、二元(邻二甲苯/间二甲苯)和三元(对二甲苯/间二甲苯/邻
9、二甲苯)测试。其组成由气相色谱仪测定。.3.2气体扩散的测量使用压力梯度(PG)法进行气体扩散测量。扩散测量分批进行,如图2所示。压力梯度(PG)法的进料的总压力使用压力变送器测量。扩散侧压力控制到小于50Pa,这种情况称为真空。纯气体,氦气、氮气、正丁烷、异丁烷和SF6在300375K进行扩散测量,这些气体在大气压力下进料侧的扩散率压力从105降到95Pa。理想状态下的选择性根据扩散率计算。丁烷异构体的混合物进行扩散测量温度范围是300375K。进气和出气由带TC的探测器和填充柱气相色谱仪分析。进气组成为52/48正丁烷/异丁烷(摩尔比)。丁烷异构体的扩散率和分离因子(正丁烷/异丁烷)由扩散
10、总量和进气的组成计算。混合气体的分离系数计算式如下:分别代表正、异丁烷的摩尔分数2.4 丁烷异构体在MFI的吸附在1005KPa、303307K温度范围内,用VPT法合成微粒常规容积法进行吸附测量,0.5g的MFI样品在400K下脱气2小时,直到电容绝对压力传感器压力没有压力变化。二元吸附丁烷异构体在303375K的温度范围内吸附测量,同样适于一元系统。摩尔比52/48的正异丁烷异构体的混合物放入有MFI颗粒的密封槽,在吸附过程中压力逐渐减少,当压力达到一个平衡值,用气相色谱仪分析气相组成。3结果与讨论3.1MFI型沸石分子筛的密度据报道,载体内部的FER /氧化铝复合层很紧密。图3显示了VP
11、T法合成(a)MFI 的XRD图谱、(b)分子筛、(c)MFI分子筛。MFI的反射峰在除去顶层后观测到。图4显示前除去顶层和产品的截面前除去顶层和后去除上层的顶面的SEM图像。在MFI沸石分子筛的上表面可以看到沸石晶体之间空隙,如图4(a)所示。刮去上层表面可看到载体内部20毫米厚的/氧化铝复合层支持,如图4(c)。图3 XRD的分子筛图被测分子比沸石孔大似乎是一个有用的技术评估。用TIPB做扩散汽化 MFI分子筛基准,没有TIPB透过分子筛,则扩散通量的TIPB小于1.010-9 molm-2s-1,这是检测极限。因此,得出的结论是MFI分子筛实际上是无孔的。丁烷/异丁烷、N2/SF6可作为
12、选择性良好指标。在300K,N2/SF6和正的选择性分别范围分别为1.6138和1090。有不同选择性的报道,是由于使用不同的扩散方法和扩散条件。图5显示了温度与N2和SF6扩散率的关系,N2和SF6的扩散率随温度升高而增加。在温度303375K,N2/SF6理想选择性为813。图6显示丁烷异构体的扩散结果,丁烷异构体在一元系统的扩散率随着温度的升高而升高。如图6,300K、PG法条件下正丁烷/异丁烷的理想选择性分别为22,335K时为16,375K时是14。以上内容均有文献报道。图4分子筛上表面电子图图5N2、SF6及N2/SF6在不同温度下理想选择性图3.2 正丁烷/异丁烷的分离在二元系统
13、中,丁烷异构体的扩散率也随温度升高而增加。正、异丁烷的分离系数在300K时为28,在335K时为40,375K时为69,见图图6(b)。分离系数始终比选择性大。图6 丁烷异构体通过MFI分子筛的渗透结果图VPT法合成的MFI颗粒在一元和二元系统中的丁烷异构体的吸附进行了测量。表1显示了丁烷异构体在MFI颗粒吸附在一元系统的数量。正丁烷/异丁烷的吸附量随着温度的升高(从300到375K)从1.2升到1.9。表2显示了丁烷异构体二元相在MFI颗粒上的吸附量。分离因子总是比理想的选择性大。这表明,正丁烷优先吸附在MFI分子筛上对丁烷异构体的混合物的选择性分离起着重要作用。丁烷异构体之间的扩散差异可能
14、有助于异构体的分离,因为分离的选择性很大。表1 一元系统中丁异构体的吸附量温度(K)吸附量(molecule u c.-1a)aibn-Butanei-Butane3755.02.61.93356.03.51.73007.26.01.2表2二元系统中丁异构体的吸附量温度(K)吸附量(molecule u c.-1a)aibn-Butanei-Butane3753.40.56.73354.80.86.03006.31.15.63.4二甲苯异构体的分离表3列出了一元系统中的二甲苯异构体的通量。对二甲苯的通量是三种异构体中最大的。其选择性的顺序可以通过规模效应来解释。对二甲苯的动力学直径为0.59n
15、m、间二甲苯和邻二甲苯为0.68nm。表3 在303K下纯二甲苯异构体组分的气相结果Flux(10-7mol m-2s-1)p-Xylene5.53.93.4m-Xylene0-Xylene图7(a)所示为瞬时通量剖面50/50对/间二甲苯混合物的扩散汽化。对二甲苯优先扩散,具有通量的最大值,间二甲苯逐渐增加,间二甲苯稳态通量大于二甲苯。在稳态时对/间二甲苯系统的分离系数为0.43,选择性一般。图7(b),对二甲苯最先扩散,并最终成为三元混合物中扩散最慢的。混合物在MFI分子筛的扩散这表明,动力学直径不是分离二甲苯异构体混合物的一个限制因素。稳态时对二甲苯/M-二甲苯,对二甲苯/邻二甲苯,邻二
16、甲苯/间二甲苯的分离系数分别为0.16,0.18和1.1。图7 在303K下二甲苯异构体通过分子筛结果图.Karsli等报道称,在室温下预加装载二甲苯引起对称性的变化和晶格扭曲增加了间二甲苯和邻二甲苯在毛孔的吸附率。人们认为,对二甲苯吸附在MFI的毛孔打开了MFI的毛孔。因此,间二甲苯和邻二甲苯很容易被扩散到MFI分子筛的各处。图8显示了在一元系统含二甲苯异构体的三元混合物的中间二甲苯扩散汽化结果。间二甲苯的通量逐渐下降。因为流入间二甲苯的浓度变低。邻二甲苯的稳态流量变大,进而达到如图第7(b)几乎相同的值,然而,对二甲苯的流量小于1.010-9molm2s1,是实验中的检测限,表明在MFI的
17、毛孔填塞间二甲苯抑制了对二甲苯的扩散。稳定态的选择性分离表明,间-二甲苯,邻二甲苯吸附比对二甲苯在MFI分子筛的吸附更大。图8 间二甲苯渗透后二甲苯的三元混合物与定组分下的三元混合物渗透结果比较图3.4丁烷异构体和二甲苯异构体分离的比较正丁烷和异丁烷动力学直径分别为0.430.50nm,比二甲苯异构体直径小。在一元系统中,分子直径较小的正丁烷比异丁烷扩散快,同样对二甲苯比其它异构体扩散的也快。小直径的正丁烷优先得到分离,因为正丁烷是一种易吸附组分。但是,分离二甲苯异构体的混合物则相反,虽然对二甲苯是最先扩散组分。人们认为,在MFI的毛孔处,相对于邻二甲苯和间二甲苯对二甲苯是一种扩散速度快但较小
18、吸附速率的组分。然而,由于二甲苯异构体的动力学直径接近的MFI的孔径,选择性发生逆转速度非常缓慢。3.5 焙烧后的扩散数据可重复性我们进行了35焙烧程序以去除吸附在整个分子筛上的实验组分。对焙烧对扩散性能的影响进行了研究。重复使用他作为探针分子的扩散数据。在375K下He的第一次扩散测量的扩散率为1.9109molm-2s-1pa-1,最后扩散测量,He的测量结果是1.8109molm-2s-1pa-1,这表明,He的扩散率可重复性。此外,对丁烷和二甲苯异构体的可重复性测定。可见,MFI分子筛在扩散和焙烧条件下具有很好的的稳定性。结论协同扩散是使用MFI膜分离丁烷异构体的重要原因。在一元系统中
19、对二甲苯在二甲苯异构体中是最易扩散的组分。然而, 在二元和三元系统中间二甲苯和邻二甲苯的扩散速度比对二甲苯快。间二甲苯吸附在MFI的孔隙中似乎抑制对二甲苯的渗透。致谢非常感激NGK Insulators Ltd.提供氧化铝载体, 和Yasuyuki Egashira博士(大阪大学化学工程部)的讲解。同时也对大阪大学的化学工程部提供x射线衍射、扫描电镜测验表示感谢。参考文献1E.R. Geus, H. Bekkum, W.J.W. Bakker, J.A. Moulijin, Hightemperaturestainless steel supported zeolite (MFI) membr
20、anes:preparation, module concentration, and permeationexperiments, Microporous Mater. 1 (1993) 131147.2Y. Yan, M.E. Davis, G.R. Gavalas, Preparation of zeoliteZSM-5 membranes by in-situ crystallization on porousa-Al2O3, Ind. Eng. Chem. Res. 34 (1995) 16521661.3C. Bai, M.D. Jia, J.L. Falconer, R.D. N
21、oble, Preparation andseparation properties of silicalite composite membranes, J.Membr. Sci. 105 (1995) 7987.4 Z.A.E.P. Vroon, K. Keizer, M.J. Gilde, H. Verweij, A.J.Burggraaf, Transport properties of alkanes through ceramicthin zeolite MFI membranes, J. Membr. Sci. 113 (1996) 293300.5 W.J.W. Bakker,
22、 F. Kapteijn, J. Poppe, J.A. Moulijn, Permeationcharacteristics of a metal-supported silicalite-1 zeolitemembrane, J. Membr. Sci. 117 (1996) 5778.6 K. Kusakabe, S. Yoneshige, A. Murata, S. Morooka, Morphologyand gas permeance of ZSM-5-type zeolite membraneformed on porous a-alumina support tube, J.
23、Membr. Sci.116 (1996) 3946.7 K. Kusakabe, A. Murata, T. Kuroda, S. Morooka, Preparationof MFI zeolite membranes and their use in separating n-butaneand i-butane, J. Chem. Eng. Jpn. 30 (1997) 7278.8 J. Coronas, J.L. Falconer, R.D. Noble, Characterization andpermeation properties of ZSM-5 tubular memb
24、ranes, AIChEJ. 43 (1997) 17971812.9 Y. Yan, M.E. Davis, G.R. Gavalas, Preparation of highlyselective zeolite ZSM-5 membranes by a post-syntheticcoking treatment, J. Membr. Sci. 123 (1997) 95103.10 J. Coronas, R.D. Noble, J.L. Falconer, Separation of C4 andC6 isomers in ZSM-5 tubular membranes, Ind.
25、Eng. Chem.Res. 37 (1998) 166176.11 J.M. van de Graaf, F. Kapteijn, J.A. Moulijn, Effect ofoperating conditions and membrane quality on the separationperformance of composite silicalite-1 membrane, Ind. Eng.Chem. Res. 10 (1998) 40714078.12 K. Keizer, A.J. Burggraaf, Z.A.E.P. Vroon, H. Verweij, Twocom
26、ponent permeation through thin zeolite MFI membranes,J. Membr. Sci. 147 (1998) 159172.13 J.M. van de Graaf, F. Kaptaijn, J.A. Moulijn, Methodologicaland operational aspects of permeation measurements onsilicalite-1 membranes, J. Membr. Sci. 144 (1998) 87104.14 T. Sano, M. Hasegawa, Y. Kawakami, Y. K
27、iyozumi, H.Yanagishita, D. Kitamoto, F. Mizukami, Potentials of silicalitemembranes for the separation of alcohol/water mixtures, Stud.Surf. Sci. Catal. 84 (1994) 11751182.15 T. Sano, H. Yanagisita, Y. Kiyozumi, F. Mizukami, K. Haraya,Separation of ethanol/water mixture by silicalite membraneon perv
28、aporation, J. Membr. Sci. 95 (1994) 221.16 H. Kita, Pervaporation through zeolite membranes, Maku(Membrane) 20 (1995) 169182.17 H. Kita, K. Horii, Y. Ohtoshi, K. Tanaka, K. Okamoto,Synthesis of a zeolite NaA membrane for pervaporation ofwater/organic liquid mixtures, J. Mater. Sci. Lett. 14 (1995)20
29、6208.18 M. Nomura, T. Yamaguchi, S. Nakao, Ethanol/water transportthrough silicalite membranes, J. Membr. Sci. 144 (1998) 161171.19 Q. Liu, R.D. Noble, J.L. Falconer, H.H. Funke, Organics/waterseparation by pervaporation with a zeolite membrane, J.Membr. Sci. 117 (1996) 163174.20 J.F. Smetana, J.L.
30、Falconer, R.D. Noble, Separation of methylethyl ketone from water by pervaporation using a silicalitemembrane, J. Membr. Sci. 114 (1996) 127130.21 C.D. Baertsch, H.H. Funke, J.L. Falconer, R.D. Noble,Permeation of aromatic hydrocarbon vapors through silicalitezeolitemembranes, J. Phys. Chem. 100 (1996) 76767679.22 N. Nishiyama, K. Ueyama, M. Matsukata, Synthesis of defectfreezeolite-alumina composite membranes by a vapor-phasetransport method, Microporous Mater. 7 (1996) 299308.23 N. Nishiyama, T. Matsufuji, K. Ueyama, M. Matsukata, FERmembrane synthesized by vapor-phase
温馨提示
- 1. 本站所有资源如无特殊说明,都需要本地电脑安装OFFICE2007和PDF阅读器。图纸软件为CAD,CAXA,PROE,UG,SolidWorks等.压缩文件请下载最新的WinRAR软件解压。
- 2. 本站的文档不包含任何第三方提供的附件图纸等,如果需要附件,请联系上传者。文件的所有权益归上传用户所有。
- 3. 本站RAR压缩包中若带图纸,网页内容里面会有图纸预览,若没有图纸预览就没有图纸。
- 4. 未经权益所有人同意不得将文件中的内容挪作商业或盈利用途。
- 5. 人人文库网仅提供信息存储空间,仅对用户上传内容的表现方式做保护处理,对用户上传分享的文档内容本身不做任何修改或编辑,并不能对任何下载内容负责。
- 6. 下载文件中如有侵权或不适当内容,请与我们联系,我们立即纠正。
- 7. 本站不保证下载资源的准确性、安全性和完整性, 同时也不承担用户因使用这些下载资源对自己和他人造成任何形式的伤害或损失。
最新文档
- 2026年文学创作赏析与创作技巧实践题
- 科技前沿知识竞赛未来科技发展趋势试题库2026版
- 2026年生活用品配送合同
- 青岛分行校园招聘考前自测高频考点模拟试题附答案详解(完整版)
- 2024年辽宁金融职业学院单招职业技能考试题库附答案详解
- 安全员A证考试能力测试备考题附完整答案详解(夺冠系列)
- 安全员A证考试综合提升练习试题附答案详解【黄金题型】
- 单位招聘208人联考工作的笔试模拟试题附答案详解
- 2025年食品安全试题库与参考答案解析
- 2025年上海应用技术大学单招职业技能考试题库及答案详解1套
- 中建“大商务”管理实施方案
- 2024-2030年中国辐射监测仪表行业市场供需态势及投资前景研判报告
- GB/T 14048.11-2024低压开关设备和控制设备第6-1部分:多功能电器转换开关电器
- 2024年国家国防科工局重大专项工程中心面向应届生招考聘用笔试参考题库附带答案详解
- 福建省宁德市2023-2024学年高一上学期期末质量检测物理试题(原卷版)
- 《油气储运安全技术》课件第九章 液化石油气储运安全与管理
- 2023修订版《托育中心、幼儿园建筑设计规范》
- 2018广州一模作文讲练评
- 生物化学:实验七 牛乳中酪蛋白的制备
- 旋磁治疗机前列腺总结报告
- 《自信的秘密》节选

评论
0/150
提交评论